Gasstransformasjoner er prosesser der en gass kan ha en eller flere av parameterne fra press, volum og temperaturendret. Det er spesielle gassformede transformasjoner der minst en av disse mengdene holdes konstant.
Typene gasstransformasjoner er:
isobar transformasjon;
isotermisk transformasjon;
isovolumetrisk transformasjon;
adiabatisk transformasjon.
Se også:Termologi — studiet av fenomener knyttet til varme og temperatur
isotermisk transformasjon
Den isotermiske transformasjonen er en der temperaturen til en gass forblir konstant. I denne typen transformasjon, trykk og volum eromvendtproporsjonal, slik at ved å øke press, reduseres volumet og omvendt.
Isotermiske transformasjoner er beskrevet av Lhei boyle-mariotte. I henhold til denne loven er produktet mellom trykk og volum av en ideell gass konstant:

TILJeg og TILf – innledende og slutttrykk
VJeg og Vf – start- og slutthastighet
K - konstant
isobar transformasjon
Den isobare transformasjonen er preget av en volumvariasjon og temperatur, holde trykket konstant.
Denne typen transformasjon er matematisk beskrevet av loven om Charles og Gay-Lussac. Under en isobar transformasjon er temperatur og volum direkte proporsjonale, det vil si å holde konstant trykket til en gass, vil volumet okkupert av den øke med økningen av temperaturen på gassen. gass.Se formelen brukt av Gay-Lussac-loven:
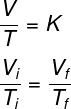
TJeg og Tf – start- og slutttemperatur
Ifølge Gay-Lussacs lov, forholdet mellom volumet og trykket til en gass, under en isobarisk transformasjon, er lik en konstant.
Isovolumetrisk transformasjon
Isovolumetrisk, isometrisk eller isokorisk transformasjon er navnet på prosessen der en ideell gass gjennomgår endringer i trykk og temperatur, og opprettholder seg selv konstant din volum. Denne typen gasstransformasjon, som finner sted inne i beholdere med stive vegger, er matematisk definert av Charles' lov.
I følge denne loven er forholdet mellom trykk og temperatur til en ideell gass alltid konstant. Videre, i denne typen transformasjon, er trykk og temperatur direkte proporsjonal: dobler vi trykket dobler vi temperaturen og omvendt.
Formelen som beskriver oppførselen til ideelle gasser under isovolumetriske transformasjoner er som følger:
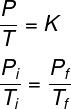
Les også: Termodynamikk - et område av fysikk som studerer fenomener der det er varmeveksling
adiabatisk transformasjon
Adiabatisk transformasjon er navnet på prosessen som gjennomgås av en gass som ikke endres varme med det ytre miljøet eller med veggene i beholderen. Formelen som matematisk forklarer oppførselen til en ideell gass som gjennomgår en adiabatisk transformasjon sier at produktet mellom trykk og volum hevet til en konstant γ er konstant.

Konstanten γ avhenger av graderifrihet av gassen, det vil si antall retninger gassmolekylene kan bevege seg i. Det kan også beregnes ved forholdet mellom spesifikk varme i presskonstant og varmespesifikk i volumkonstant.
Eksempler på gasstransformasjoner
isotermisk transformasjon – enhver langsom ekspansjon eller sammentrekning av en gass som skjer ved konstant temperatur.
isobar transformasjon – avkjøling av gassen i en blære plassert for avkjøling i kjøleskap.
Isovolumetrisk transformasjon – varme opp vanndampen innestengt i en trykkoker fullstendig.
adiabatisk transformasjon – gass som drives ut av en aerosolspray.

Se også: Kalorimetri – formler, begreper og løste oppgaver
Løste øvelser om gasstransformasjoner
Spørsmål 1 - Se gjennom alternativene nedenfor og sjekk svaret som bare inneholder sanne alternativer.
I – Isotermiske transformasjoner er de der gasstemperaturen holdes konstant.
II – Adiabatiske transformasjoner innebærer varmeveksling mellom gassen og det ytre miljøet.
III – Isokorisk transformasjon er en der gasstrykket holdes konstant.
IV – Isobariske transformasjoner skjer med konstant trykk.
Er riktig:
a) I og II.
b) I, II og III.
c) II og III.
d) I og IV.
Vedtak:
Alternativ II og III er feil, siden adiabatiske transformasjoner ikke involverer varmeveksling, og isokoriske transformasjoner er de som skjer i konstante volumer. Dermed er det riktige alternativet bokstaven D.
Spørsmål 2 -En ideell gass gjennomgår en rask transformasjon, slik at dens temperatur, trykk og volum gjennomgår plutselige endringer i løpet av kort tid. I følge hans kunnskap om gasstransformasjoner, var transformasjonen som ble gjennomgått av gassen:
a) isotermisk.
b) isobarisk.
c) adiabatisk.
d) isovolumetrisk.
Vedtak:
Adiabatiske transformasjoner skjer raskt, så det er ikke tid for gassen til å utveksle varme med det ytre miljøet. I denne typen transformasjon endres trykk-, volum- og temperaturparametrene brått. Dermed er det riktige alternativet bokstaven C.
Av Rafael Hellerbrock
Fysikklærer
Kilde: Brasil skole - https://brasilescola.uol.com.br/quimica/transformacoes-gasosas.htm

