Et rent stoff dannes av en enkelt type kjemiske arter, det vil si at dens sammensetning og egenskaper er faste. En blanding inneholder mer enn én type komponent, så organisasjonen varierer.
Dermed kan vi bare skille et rent stoff fra en blanding når vi vet sammensetningen.
Når vi sammenligner et glass vann og et glass oppløst sukker, merker ikke øynene våre noen forskjell. Imidlertid, hvis vi svelger innholdet i de to glassene, vil vi merke at det ene er det rene stoffet og det andre består av en blanding.
rene stoffer
En ren substans er settet med bare en kjemisk art, det vil si at den ikke blandes med andre.
La oss bruke vann som et eksempel. Vannet (H2O) er anerkjent for sine egenskaper, og de spesifikke egenskapene til dette materialet hjelper oss med å identifisere det. Hoved vannegenskaper de er:
| Tetthet | 1,00 g / cm3 |
|---|---|
| Fusjonspunkt | 0 ° C |
| Kokepunkt | 100 ° C |
Når et materiale har faste og uforanderlige egenskaper i sin helhet, sier vi at det er en Ren substans.
Når vi legger bordsalt, natriumklorid (NaCl), i et glass vann og rører, vil det oppstå en forandring.

Resultatet er et produkt med en mellomliggende tetthet mellom vann og salt. Dette er fordi vann ikke lenger er et rent stoff og har blitt et Blande.
Når du prøver å fryse denne blandingen, vil du legge merke til at smeltetemperaturen vil være mindre enn 0 ° C og det også denne blandingen vil ikke koke ved 100 ° C, mer varme vil være nødvendig for å fordampe dette produkt.
Rene enkle og sammensatte stoffer
Rene stoffer klassifiseres som enkle når det i deres sammensetning er atomer med bare ett kjemisk element.
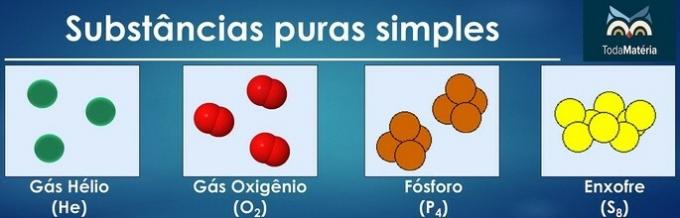
Arrangementet av atomer med to eller flere kjemiske elementer danner rene sammensatte stoffer.

Blandinger
En blanding tilsvarer sammenføyningen av to eller flere rene stoffer, som kalles komponenter.
I motsetning til rene stoffer er egenskapene ikke faste, da de avhenger av andelen komponenter i blandingen.
Se hvordan tetthet, en fysisk egenskap, varierer med mengden salt blandet med vann.
| Andel salt i total masse av blandingen |
Blandingstetthet (g / cm3) ved 20 ° C |
|---|---|
| 1 | 1,005 |
| 8 | 1,056 |
| 12 | 1,086 |
| 16 | 1,116 |
| 26 | 1,197 |
Kilde: FURNISS, B. S. et al. Vogels lærebok for praktisk organisk kjemi. 4. red. London: Longman, 1987. P. 1.312.
Tilsetningen av vann og salt, i noen proporsjon, har derfor en variabel tetthet, og derfor kan vi ikke klassifisere blandingen som verken vann eller salt.
Homogene og heterogene blandinger
Homogene blandinger er de som presenterer komponentene i bare en fase og derfor de samme egenskapene på alle punkter.

Når vi visuelt oppfatter mer enn en fase, blir blandingen klassifisert som heterogen.

Sammendrag om rene stoffer og blandinger
| Rene stoffer og blandinger | |
|---|---|
|
homogent system (bare en fase) |
Ren substans (en komponent) |
|
homogen blanding (mer enn en komponent i samme fase) | |
|
heterogent system (mer enn en fase) |
Ren substans (en komponent i forskjellige fysiske tilstander) |
|
heterogen blanding (mer enn en komponent i mer enn en fase) |
For å lære mer, må du sjekke disse tekstene:
- Atomer
- Kjemiske elementer
- Separasjon av blandinger
Øvelser med kommenterte tilbakemeldinger
1. (UFMG) En prøve av et rent stoff X hadde noen av dets egenskaper bestemt. Alle alternativer har egenskaper som er nyttige for å identifisere dette stoffet, bortsett fra:
a) tetthet.
b) prøvemasse.
c) vannløselighet.
d) koketemperatur.
e) smeltetemperatur.
Feil alternativ: b) prøvemasse.
a) KORREKT. Tetthet er mengden materie i et gitt volum. Som en materialspesifikk egenskap er den nyttig for å identifisere et stoff.
b) FEIL. Masse er mengden materie i kroppen. Ettersom denne egenskapen gjelder alle forhold, uavhengig av dens sammensetning, er det ikke mulig å bruke den til å identifisere et stoff.
c) KORREKT. Løselighet er et stoffs evne til å oppløse, eller ikke, i en gitt væske. Som en materialspesifikk egenskap er den nyttig for å identifisere et stoff.
d) KORREKT. Koketemperatur tilsvarer endringstemperaturen fra væske til gassform. Som en materialspesifikk egenskap er den nyttig for å identifisere et stoff.
e) KORREKT. Smeltetemperatur tilsvarer endringstemperaturen fra væske til fast tilstand. Som en materialspesifikk egenskap er den nyttig for å identifisere et stoff.
2. (Vunesp) Etiketten på en flaske mineralvann er gjengitt nedenfor.
| Sannsynlig kjemisk sammensetning: |
|---|
| Kalsiumsulfat 0,0038 mg / L |
| Kalsiumbikarbonat 0,0167 mg / L |
Basert på denne informasjonen kan vi klassifisere mineralvann som:
a) ren substans.
b) enkel substans.
c) heterogen blanding.
d) homogen blanding.
e) kolloid suspensjon.
Riktig alternativ: d) homogen blanding.
a) FEIL. Vann ville være rent hvis sammensetningen bare hadde H-molekyler2O.
b) FEIL. Et enkelt stoff består av atomer med bare ett kjemisk element. Heller ikke rent vann er et enkelt stoff, da det dannes av hydrogen og oksygenatomer (H2O) den er klassifisert som kompositt.
c) FEIL. En heterogen blanding har mer enn en fase, i så fall kan vi bare observere vann.
d) KORREKT. Siden det bare har en fase, er systemet homogent. Når vi ser på vannflasken, kan vi bare se væsken, da forbindelsene av kalsiumsulfat og kalsiumbikarbonat er oppløselige i vann og er derfor oppløst.
e) FEIL. En kolloid suspensjon er en heterogen blanding hvis komponenter er differensiert ved hjelp av et mikroskop.
3. (UCDB) I et kjemilaboratorium ble følgende blandinger fremstilt:
JEG. vann / bensin
II. vann / salt
III. vann / sand
IV. bensin / salt
V. bensin / sand
Hvilke av disse blandingene er homogene?
a) Ingen.
b) Bare II.
c) II og III.
d) I og II.
e) II og IV.
Riktig alternativ: b) Bare II.
a) FEIL. Vann er en uorganisk forbindelse og bensin en organisk forbindelse. Disse stoffene har ikke evnen til å samhandle, og fordi de har forskjellige tettheter, danner de en heterogen blanding.
b) KORREKT. Saltet, natriumklorid, oppløses i vann og danner en løsning som er en homogen blanding.
c) FEIL. Sand, silisiumdioksid, danner en heterogen blanding med vann.
d) FEIL. Salt er en uorganisk forbindelse og bensin en organisk forbindelse. Disse stoffene har ikke evnen til å samhandle, og fordi de har forskjellige tettheter, danner de en heterogen blanding.
e) FEIL. Sand er en uorganisk forbindelse og bensin en organisk forbindelse. Disse stoffene har ikke evnen til å samhandle og danner derfor en heterogen blanding.
4. (Ufes) I et godt blandet system bestående av sand, salt, sukker, vann og bensin er antall faser:
a) 2.
b) 3.
c) 4.
d) 5.
e) 6.
Riktig alternativ: b) 3.
FASE 1: Salt og sukker er i stand til å samhandle med vann og gjennom intermolekylære krefter binder molekylene og danner en løsning, som er en homogen blanding.
FASE 2: Vann er en uorganisk forbindelse og bensin en organisk forbindelse. Disse stoffene har ikke evnen til å samhandle, og fordi de har forskjellige tettheter, danner de en heterogen blanding.
FASE 3: Sand er et silikat som ikke har noen kjemisk affinitet med vann og bensin, og representerer derfor en fase.
5. (Mackenzie) Blandingen dannet av:
a) isbiter og vandig sukkeroppløsning (glukose).
b) N gasser2 og CO2.
c) vann og aceton.
d) vann og stikkelsbærsirup.
e) parafin og dieselolje.
Riktig alternativ: a) isbiter og vandig sukkeroppløsning (glukose).
a) KORREKT. Det er mulig å observere to faser: isbiter og glukoseoppløsningen, så de er et heterogent system.
b) FEIL. Gasser er alltid en homogen blanding.
c) FEIL. Hydrogenbindinger dannes mellom karbonylen av propanon og vannmolekylet. Siden de er polare stoffer, er aceton i stand til å oppløse seg i vann og danne en homogen blanding.
d) FEIL. Disse to komponentene blandes for å danne et homogent system, da vi bare ser en rød væske fra stikkelsbærsirupen, da en fortynning oppstår ved å tilsette vann.
e) FEIL. Begge er organiske forbindelser, og på grunn av kjemisk affinitet danner de en enkelt fase, som representerer et homogent system.
Test dine kunnskaper med øvelsene:
- Øvelser på homogene og heterogene blandinger
- Øvelser på separasjon av blandinger
- Øvelser på materieegenskaper


