Eksperimenter er en praktisk måte å lære og teste din kunnskap om begrepene studert i kjemi.
Benytt deg av disse kjemiske eksperimentene, som kan gjøres hjemme (under voksenoppsyn) eller jobbes med i klasserommet sammen med læreren, for å utfylle studiene.
Første opplevelse - å avdekke fargene
Begreper involvert: kromatografi og separasjon av blandinger
Materialer
- flerfargede tusjpenner
- alkohol
- kaffefilterpapir
- kopp (glass for å lette overvåking av eksperimentet)
Hvordan lage
- Bruk saks og klipp strimler med filterpapir. Lag et rektangel for hver penn som brukes.
- Nå, i en avstand på ca. 2 cm fra basen, tegner du en sirkel med den valgte fargepennen og maler hele innsiden.
- Lim kanten på papiret lengst fra den trukkede marmoren på en støtte. For dette kan du bruke et bånd og feste det til en blyant.
- Tilsett alkohol i glasset, ikke for mye, da det bare skal berøre enden av papiret nær pennmerket.
- Legg papiret i koppen slik at det er loddrett. Blyanten som støtter den skal hvile på kantene.
- Vent mellom 10 og 15 minutter til alkoholen hever seg gjennom filterpapiret. Fjern deretter papirene og la dem tørke.
Resultat
Når alkohol passerer pennemerket, samhandler det med fargekomponentene og driver dem over papiret. Dermed vil de forskjellige pigmentene skilles fra ved kontakt med alkohol.
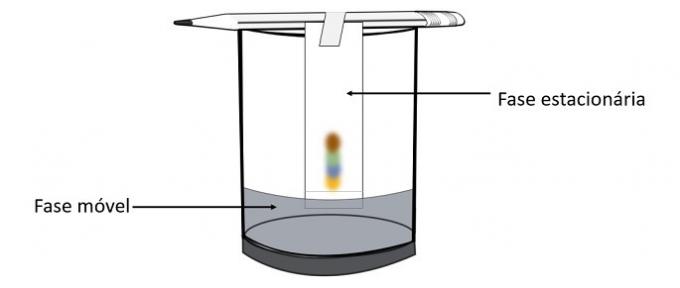
Gjennom dette eksperimentet er det mulig å vite hvilke farger som ble blandet for å lage fargen på pennen.
Forklaring
Kromatografi er en type prosess for å skille blandinger. Filterpapir er den stasjonære fasen og alkohol er den mobile fasen som drar komponentene i blandingen når den passerer gjennom den stasjonære fasen. I denne prosessen, jo større samspillet med alkoholen er, desto raskere vil pigmentet bevege seg med passasjen til løsningsmidlet.
Komponentene i materialet, da de har forskjellige egenskaper, vil samhandle med mobilfasen på forskjellige måter, noe som kan bli lagt merke til av de forskjellige dragetidene i den stasjonære fasen.
Lære mer om kromatografi.
2. opplevelse - matoppbevaring
Begreper involvert: organiske forbindelser og kjemiske reaksjoner
Materialer
- eple, banan eller pære
- sitron eller appelsinjuice
- C-vitamin tablett
Hvordan lage
- Velg en av de tre fruktene og skjær den i tre like store deler.
- Det første stykket vil tjene som en sammenligning med de andre. Så ikke legg til noe i det, bare la det være utsatt for luft.
- Drypp innholdet i en sitron eller en appelsin i en av bitene. Spred slik at hele innsiden av frukten er dekket av juice.
- I den siste delen, spre vitamin C, det kan være en knust tablett, over hele fruktmassen.
- Se på hva som skjer og sammenlign resultatene.
Resultat
Fruktmassen som har blitt utsatt for luften, bør raskt mørkne. Sitron- eller appelsinjuice og vitamin C, et kjemikalie som kalles askorbinsyre, skal bremse frukten.

Forklaring
Når vi kutter en frukt, blir cellene skadet og frigjør enzymer, for eksempel polyfenoloksidase, som i kontakt med luften oksyderer fenolforbindelsene som er tilstede i maten og forårsaker en enzymatisk bruning.
For å hindre virkningen av oksygen, brukes konserveringsmidler som askorbinsyre fordi de fortrinnsvis oksyderes i stedet for fenolforbindelser. I tillegg til vitamin C-tabletten, er askorbinsyre også til stede i naturlige kilder, som sitrus, sitron og appelsin, foreslått i eksperimentet.
Lære mer om oksidasjon.
3. opplevelse - hvem fryser raskere?
Begreper involvert: kolligative egenskaper og kryoskopi
Materialer
- to rør (brukes til festgjenstander)
- glassbolle
- bordsalt
- filtrert vann
- is
- termometer
Hvordan lage
- Tilsett samme mengde filtrert vann til begge rørene. For eksempel 5 ml i hvert rør.
- Tilsett bordsaltet til et av rørene og legg et identifikasjonstape for å skille ut hvilket som er salt.
- Fyll glassbeholderen med knust is og tilsett litt salt.
- Plasser de to rørene samtidig inne i isen og se hva som skjer.
- Registrer frysetemperaturen for hver situasjon.
Resultat
Tilsetning av løsemiddel til vann senker frysetemperaturen. Derfor har vanlig vann en tendens til å fryse mye raskere enn en salt- og vannoppløsning når de utsettes for de samme forholdene.
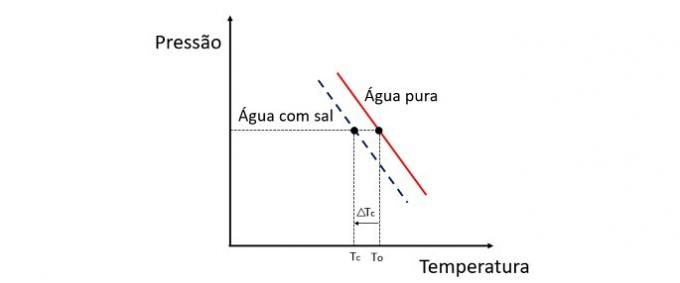
Forklaring
Kryoskopi er en kolligativ egenskap som studerer temperaturvariasjonen til et løsningsmiddel når forskjellige mengder oppløst stoff er oppløst i det.
Senking av frysetemperaturen på vann er forårsaket av en ikke-flyktig løsemiddel, og dette fenomenet har mange praktiske anvendelser. Derfor, jo større konsentrasjon av løsemiddel i løsningen påvirker den kryoskopiske effekten.
Hvis for eksempel vann fryser ved 0 ° C og vi tilsetter salt i det, vil faseskiftetemperaturen være negativ, dvs. mye lavere.
Dette er grunnen til at sjøvann ikke fryser på steder der temperaturen er under 0 ° C. Salt oppløst i vann har en tendens til å senke frysetemperaturen ytterligere. På steder der det er snø, er det også vanlig å kaste salt på veiene for å smelte isen og unngå ulykker.
Lære mer om kolligative egenskaper.
4. eksperiment - nedbrytning av hydrogenperoksid
begreper involvert: kjemisk reaksjon og katalysator
Materialer
- En halv rå potet og en halv kokt
- Et stykke rå lever og et annet kokt stykke
- Hydrogenperoksid
- 2 retter
Hvordan lage
- Tilsett mat, poteter sammen og lever sammen i hver tallerken.
- I hvert av de fire materialene tilsettes 3 dråper hydrogenperoksid.
- Se på hva som skjer og sammenlign resultatene.
Resultat
Hydrogenperoksid, en hydrogenperoksidoppløsning, når den kommer i kontakt med rå matvarer, begynner å sprute nesten umiddelbart.
Dette eksperimentet kan også gjøres ved å tilsette et stykke mat i en beholder med hydrogenperoksid for å gjøre reaksjonen mer merkbar.
Forklaring
Brusingen presentert av hydrogenperoksid når den kommer i kontakt med rå mat karakteriserer forekomst av en kjemisk reaksjon, som er spaltning av hydrogenperoksid og frigjøring av gassen oksygen.
Nedbrytningen av hydrogenperoksid skjer gjennom virkningen av katalaseenzymet, som finnes i peroksisomorganellen, til stede i dyre- og planteceller.
Det er viktig å fremheve at nedbrytningen av hydrogenperoksid skjer spontant i nærvær av sollys, men i en veldig langsom reaksjon. Imidlertid fungerer katalase som en katalysator, og øker hastigheten på den kjemiske reaksjonen.
Hydrogenperoksid kan være et giftig stoff for celler. Derfor bryter katalase forbindelsen og produserer vann og oksygen, to stoffer som ikke skader kroppen.
Når maten tilberedes, gjennomgår komponentene endringer. Modifikasjonene forårsaket av matlaging kompromitterer også virkningen av katalase ved å denaturere proteinet.
Den samme handlingen vi ser med mat er hva som skjer når vi setter hydrogenperoksid på et sår. Catalase virker, og det er dannelse av bobler, som består i frigjøring av oksygen.
Lære mer om kjemiske reaksjoner.
Bibliografiske referanser
SAINT, W. L. P.; MOL, G. S. (Koordinater.). Citizen Chemistry. 1. red. São Paulo: Ny generasjon, 2011. v. 1, 2, 3.
BRASILISK KJEMISK SAMFUNN (org.) 2010. Kjemi i nærheten av deg: Rimelige eksperimenter for K-12-klasserommet. 1. red. São Paulo.

