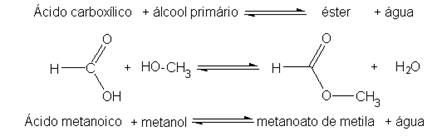
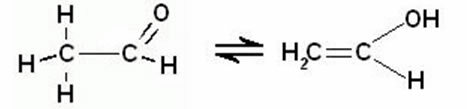DE destillasjon det er en av prosessene for separering av homogene blandinger som foregår ved koking, der væsken fordampes og deretter kondenseres. Dermed har blandingene som skal skilles fra forskjellige kokepunkter.
Destillasjon er med andre ord en fysisk-kjemisk prosess for separasjon av blandinger som skjer gjennom oppvarming og avkjøling av blandingene. Når blandingen oppvarmes, fordampes stoffet som har det laveste kokepunktet, det vil si den mest flyktige, først.
Destillasjon utføres i kjemiske laboratorier og industrier ved bruk av spesifikt utstyr (kondensator, termometer, destillasjon, bunsenmunnstykke, begerglass, varmekappe, fraksjoneringskolonne), for eksempel når du skiller vann fra alkohol eller vann fra salt.
Et naturlig eksempel på destillasjonsprosessen ses når vanndråper kondenserer på kaldere dager. I tillegg produseres de såkalte destillerte drikkene (cachaça, vodka, konjakk, tequila, rum, whisky) gjennom den fraksjonelle destillasjonsprosessen, brukt siden antikken.
Typer destillasjon
Destillasjon kan foregå på to måter, avhengig av arten av de separate blandingene:
Enkel destillasjon
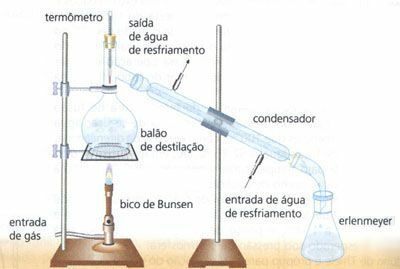 Enkel destillasjon
Enkel destillasjon
Separasjon av en homogen blanding av fast og flytende, f.eks. Vann (H2O) av saltet (NaCl). På denne måten fordampes vannet gjennom oppvarming, som passerer gjennom kondensatoren i form av væske (vanndråper), der saltet holdes tilbake og skilles i en beholder kalt a destillasjon.
Fraksjonert destillasjon
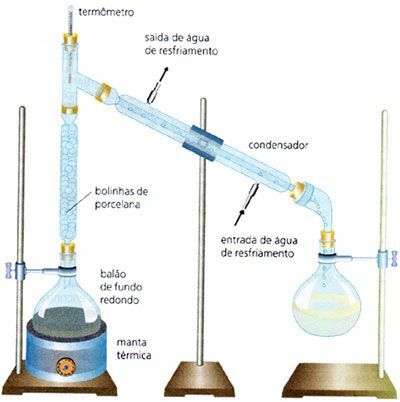 Fraksjonert destillasjon
Fraksjonert destillasjon
Mye brukt i industrien, er det separasjonen av en homogen blanding av væske og væske, av for eksempel vann og alkohol (Kokepunktet for vann er 100 ° C og kokepunktet for etylalkohol er 78 ° C). Det utføres gjennom blandinger som har veldig nær kokepunkter. I motsetning til den enkle destillasjonsprosessen, er det i dette tilfellet en fraksjoneringskolonne.
Oljedestillasjon
For å skaffe petroleumsprodukter (bensin, parafin, parafin, asfalt), destillasjonsprosessen fraksjonert brukes der væske med laveste kokepunkt skilles først til væske med høyest kokepunkt når. kokende.
husk at den Petroleum det er et naturlig stoff som består av flere organiske komponenter, spesielt hydrokarboner (karbon- og hydrogenmolekyler).
azeotrop destillasjon
Azeotrop destillasjon oppstår når separasjonen av blandinger danner en azeotrop, det vil si at de har lav flyktighet og punkt konstante kokepunkter, som ikke kan skilles fra ved den enkle destillasjonsmetoden, f.eks. saltsyre (HCL) og vann (H2O).
Morsomme fakta: Visste du det?
Destillert vann (demineralisert vann) er et rent stoff oppnådd ved destillasjon og brukes vanligvis i laboratoriet. Merk at vannet vi drikker ikke er rent, det vil si at det inkluderer mineralsalter. Destillert vann kan imidlertid brukes til konsum så vel som til behandling av noen sykdommer, for eksempel nyrestein.
Utfyll forskningen din ved å lese artiklene:
- Smeltepunkt og kokepunkt
- Væske eller kondens
- Fordampning
- Separasjon av blandinger
Sjekk opptakseksamen spørsmål med tilbakemeldinger kommentert: øvelser på å blande separasjon.