Adsorpsjon er en fysisk-kjemisk egenskap av molekyler av flytende, gassformige og faste stoffer.
Prosessen skjer når flytende eller gassformige partikler blir fanget på overflaten av faste stoffer. Hvis de faste stoffene er porøse, øker adsorpsjonskapasiteten enda mer.
Det er to klassifiseringer for komponentene som deltar i prosessen:
- Adsorberer: Det er den flytende eller gassformige substansen som holdes på overflaten av et adsorberende fast stoff.
- Adsorbenter: Det er det faste stoffet som fremmer retensjonen av andre stoffer.
DE desorpsjon det er den omvendte adsorpsjonsprosessen, det vil si frigjøring av adsorbat fra overflaten av adsorbenten.
Typer
Avhengig av arten av kreftene som er involvert i prosessen, kan adsorpsjon være av to typer: fysisorpsjon og kjemisorpsjon.
I noen tilfeller kan begge typer adsorpsjon forekomme i samme prosess.
fysisorpsjon
Den fysiske fysisorpsjonen eller adsorpsjonen mellom adsorbatet og adsorbenten skjer gjennom Van der Waalls-krefter (dipol-dipol eller indusert dipol).
I dette tilfellet er det ingen type molekylær endring i stoffene som er involvert i prosessen. Det vil si at stoffet beholder sin kjemiske natur.
Fysisk adsorpsjon er en reversibel prosess.
Kjemisorpsjon
Kjemisorpsjon eller kjemisk adsorpsjon består av en kjemisk reaksjon. Ved å involvere elektroner, regnes som en sterkere kjemisk binding enn fysisorpsjon.
I kjemisorpsjon er det en molekylær endring av stoffene som er involvert i prosessen. Det vil si at stoffet kan transformeres til et annet.
Siden dette er en kjemisk reaksjon, må komponentene i adsorbenten og adsorbatet ha spesifisitet. De må kunne gjenkjenne og reagere.
Kjemisk adsorpsjon er en irreversibel prosess.
Les også om:
- Intermolekylære styrker
- Kjemiske bindinger
Adsorpsjon og absorpsjon
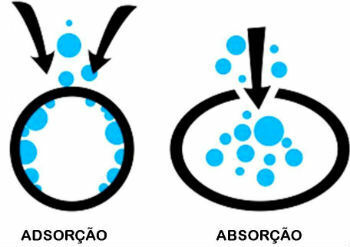
Forskjell mellom adsorpsjon og absorpsjon
Adsorpsjon og absorpsjon er to forskjellige prosesser. Kjenn forskjellen mellom dem:
- adsorpsjon: Et stoff holdes på overflaten av et annet, uten å være en del av volumet.
- Absorpsjon: Ett stoff er absorbert av et annet, noe som forårsaker volumendring.
Et vanlig eksempel på absorpsjon er svampen som absorberer vann. Ved å gjøre dette blir vannvolumet innlemmet i svampvolumet.
Aktivt kull
Aktivt karbon er et eksempel på et bedre kjent adsorberende stoff. I strukturen er det mange porer som forsterker retensjonen av stoffer og øker deres adsorpsjonskapasitet.
Derfor brukes aktivt karbon for å fjerne organiske stoffer, oljer, farger og lukt. Det brukes også til vannbehandling og produksjon av kosmetikk og medisiner.

Aktivt kull
Les også:
- Kromatografi
- Separasjon av blandinger
- Løsemiddel og løsemiddel
- Materialer brukt i kjemilaboratoriet