Gallium er et kjemisk element med et atomnummer (Z) lik 31 og dets symbol er Ga. Den tilhører familie 13 (eller gruppe IIIA, i henhold til den gamle nummereringen), som er familien til bor, som er et "sølvfarget metall som ligner på aluminium.
En av de mest interessante egenskapene er smeltepunktet, som er lavt sammenlignet med nesten alle metaller (unntatt kvikksølv) som tidligere er kjent, omtrent 29,76 ° C. Under omgivelsesbetingelser er det derfor vanligvis tilstand. På varmere dager smelter den imidlertid til flytende tilstand. Derfor, hvis vi holder dette metallet i hendene, vil det begynne å smelte, fordi temperaturen vår er høyere enn smeltepunktet.

Når du lagrer gallium, kan den ikke fylle hele beholderen ettersom den utvides når den stivner
Det er mange videoer på internett som viser en skje som smelter når den legges i et glass vann. Faktisk er disse skjeene laget av gallium, ikke andre vanligere metaller eller metalllegeringer som aluminium eller stål. stål. Når galliumskjeen plasseres i varmt vann, blir den således flytende. Se mer om dette i teksten “
Forslag til en eksperimentell klasse om smeltepunkt”.Gallium har også en annen funksjon, som er det enorme området mellom smelte- og koketemperatur. Som allerede nevnt er smeltepunktet rundt 29,76 ° C, men kokepunktet er rundt 2204 ° C.
Gallium ble oppdaget mellom klokka 3 og klokka fire den 27. august 1875 av den franske kjemikeren Paul Lecoq de Boisbaudran. Et interessant aspekt er at russisk kjemiker Dimitri Ivanovitch Mendeleyev år tidligere, i 1868 (1834-1907) foreslo det periodiske systemet, men etterlot et gap for et element som til da var ukjent. Mendeleyev kalte det eka-aluminium, fordi han på en spektakulær måte forutsa at i den horisontale boreraden, mellom aluminium og uran, ville dette elementet lyve.

Fransk kjemiker Paul Lecoq de Boisbaudran - oppdageren av gallium
Mendeleyev spådde til og med egenskapene til dette elementet, for eksempel dets atomvekt, som ville være 68, og dens egenvekt, som ville være 5,9. Dermed oppdaget Lecoq et element med en atomvekt på 69 og en egenvekt på 4,7, noe som indikerer at Mendeleyev tok feil. Imidlertid sa Mendeleyev at prøven til Lecoq ikke var ren nok, og at han skulle gjenta eksperimentene.
Det var det Lecoq gjorde, og overraskende hadde Mendeleyev rett, den spesifikke tyngdekraften til dette nye elementet var 5,9. Så det var virkelig eka-aluminiumet som Mendeleyev hadde sett for seg.
Lecoq ga navnet “Gallium” til det oppdagede elementet med henvisning til det latinske navnet for Frankrike, som er Gallia. Men det er noen som sier at deres mål faktisk var annerledes, fordi på fransk betyr Le coq "hanen" og på latin er det gallus.
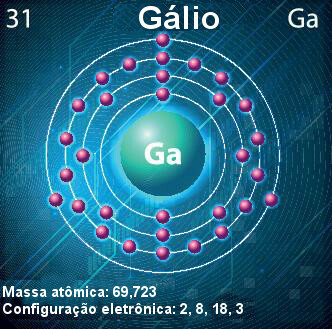
Galliumatom - symbol, atomnummer, atommasse og elektronkonfigurasjon
En annen egenskap ved gallium er at den tærer på andre metaller. På internett er det noen videoer som viser plassering av litt flytende gallium på toppen av en aluminiumskanne. Etter noen timer er det mulig å bryte det med hendene veldig enkelt.
Blant anvendelsene av gallium kan vi fremheve:
* Den brukes til fremstilling av speil;
* Det er en halvleder og leder varme dobbelt så mye som jern. Derfor brukes den til produksjon av dioder, lysdioder, transistorer og temperatur-, lys- og magnetfeltsensorer;
* I termometre som brukes til veldig høye temperaturer;
* Ved produksjon av metalllegeringer som trenger lave smeltepunkter;
* Å skaffe hydrogengass gjennom kontakt mellom aluminium galliumlegering og vann;
* Ga-37-isotopen er radioaktiv og brukes som sporstoff i tester for å oppdage sykdommer og svulster.
Av Jennifer Fogaça
Uteksamen i kjemi


