Karbon er et kjemisk element med et atomnummer (Z) som er lik 6, noe som betyr at atomene som danner det har seks protoner i kjernen. Dens molære masse er 12.011 g / mol, og i naturen er det tre isotoper av karbon, som er: o karbon-12, karbon-13 og karbon-14. C-12 har seks protoner og seks nøytroner i kjernen og er den mest utbredte.
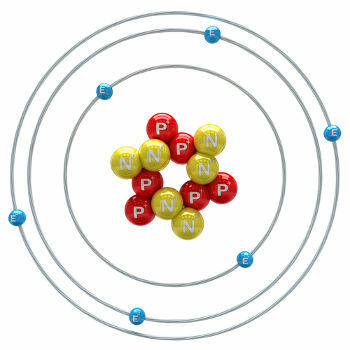
karbonatom-12 illustrasjon
C-13 har syv nøytroner og er minst forekommende (1,01 til 1,14%). C-14 har åtte nøytroner og er en radioaktivt element som avgir β-partikler (elektroner), som dannes i jordens stratosfære når kosmiske strålneutroner bombarderer nitrogen-14 som er tilstede i disse øvre lagene i atmosfæren. Den er innlemmet av alle planter og dyr, og vel vitende om at halveringstiden er ca 5730 år, brukes den til å bestemme alderen på fossiler mellom 100 og 40.000 år. Flere detaljer om C-14 og dateringsteknikken kan sees i teksten. Hva er Carbon-14?
Karbon er tetravalent, det vil si at det trenger fire flere protoner i valenslaget (det ytterste laget) for å adlyde oktettregelen. Derfor lager det vanligvis fire kovalente bindinger, som deler fire par elektroner med andre elementer så vel som andre karbonatomer. Disse bindingene kan være enkle, doble eller tredoble og resultere i dannelsen av millioner av forskjellige forbindelser. Av den grunn ble det opprettet et kjemiområde,
Organisk kjemi, som studerer hovedforbindelsene avledet fra karbon, med unntak av noen tilfeller som er av mineralsk opprinnelse, som f.eks karbondioksid (CO2), O karbonmonoksid (CO), O kalsiumkarbonat (CaCO3), natriumhydrogenkarbonat eller natriumbikarbonat (NaHCO3), mellom andre. Disse forbindelsene er studert i Uorganisk kjemi.Karbon utfører allotropi og danner enkle stoffer, det vil si stoffer som bare dannes av bindinger mellom karbonatomer. Det er minst syv allotroper av karbon, som er grafitt (alfa og beta), diamant, lonsdaleite (sekskantet diamant), chaoite, karbon (VI) og fullerener. Det er faktisk flere typer fullerener, som er syntetiske allotrope former for karbon. De har en polyhedral struktur med et karbonatom ved hvert toppunkt, og et eksempel er Ç60 kalt buckminsterfullerene, og strukturen ser ut som en fotball.
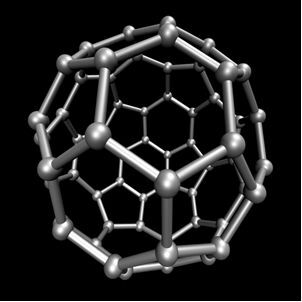
Carbon-60 (buckminsterfullerene)
Imidlertid er det bare to av disse allotropene av karbon som er naturlige. grafittDet er fra Diamant. De skiller seg bare ut fra det krystallinske arrangementet av atomer i verdensrommet, som vist i figuren nedenfor, og dette resulterer i helt forskjellige fysisk-kjemiske egenskaper. Les teksten karbonallotropi for mer informasjon.

De to naturlige allotrope karbonformene er grafitt og diamant.
En annen syntetisk allotropisk form for karbon er nanorør (bildet nedenfor) som har brede biologiske anvendelser, inkludert medisinsk diagnostikk og behandlinger.

Illustrasjon av et mikroskopisk karbon nanorør
Og dermed, karbon er til stede i alt rundt oss og i oss, fordi han komponerer naturlige organiske forbindelser - som fossile brensler, som inkluderer olje, kull og naturgass, og andre drivstoff som etanol og biodrivstoff - blant annet landbruksprodukter. form også syntetiske organiske forbindelser, for eksempel syntetiske fibre som utgjør stoffer, medisiner, polymerer som utgjør plast og gummi, insektmidler, fargestoffer og mye mer. Innenfor oss, dyr og grønnsaker, danner karbon veldig viktige forbindelser, slik som karbohydrater, som sukker, glukose og cellulose; proteinene som danner for eksempel DNA, og sammen med lipider danner membranene i røde blodlegemer og hvite blodlegemer.
Alt dette viser karbonens betydning for å opprettholde livet. Men det har også vært assosiert med negative aspekter, som intensivering av drivhuseffekt og det påfølgende global oppvarming, dette er fordi den viktigste skurken av disse problemene er karbondioksidforbindelsen (CO2). Hovedsakelig på grunn av den store forbrenningen av fossile brensler som frigjør denne gassen, konsentrasjonen av CO2 i atmosfæren har økt. Som klimagass forårsaker det de ovennevnte problemene. På den annen side er karbondioksid også til stede i vitale reaksjoner som fotosyntese og respirasjon.
Av Jennifer Fogaça
Uteksamen i kjemi
Kilde: Brasilskolen - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-carbono.htm


