En gass er preget av tre egenskaper, kalt tilstandsvariabler, som er: trykk, volum og temperatur. Når en eller flere av disse variablene endres, a gass transformasjon, som kan klassifiseres som isotermisk, isovolumetrisk eller isobarisk.
er kalt isoterm transformasjon gassomdannelsen der systemtemperaturen forblir konstant, variasjoner som bare forekommer i press og i volumet av gass.
Denne transformasjonen kalles ogsåBoyle-Mariottes lov - navn gitt til ære for Boyle, en irsk kjemiker som i 1660 vedtok en lov om at i et gitt utvalg av ideell gass, produktet av trykket og volumet som gassen bruker er konstant når temperaturen ikke varierer, og også til ære for Mariotte, en fransk fysiker som i 1676 uavhengig oppdaget den samme loven.
Oppsummert kan loven som beskriver oppførselen til en gass under en isoterm transformasjon, angis som følger:
“I isotermisk transformasjon er trykket som utøves av en ideell gassprøve omvendt proporsjonal med volumendringen. "
Ikke stopp nå... Det er mer etter annonseringen;)
Fra denne loven kan vi konkludere med at når du øker trykket til en gassmasse, vil det være en reduksjon i volumet okkupert av den og omvendt. Derfor vil produktet mellom disse to mengdene forbli konstant.
Matematisk kan Boyle-Mariottes lov beskrives ved uttrykket:
P. v = konstant
Ettersom produktet mellom trykk og volum er konstant, kan vi konkludere med at:
P1. V1 = s2 . V2
I tillegg er denne loven også grafisk representert:
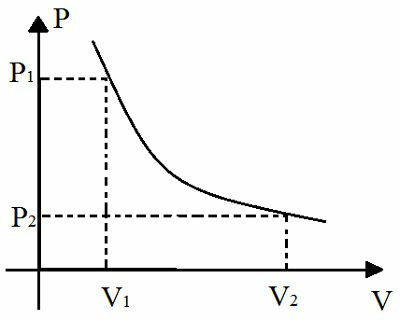
Denne grafen representerer forholdet mellom trykkendring og temperaturendring under en isoterm transformasjon
Den grafiske representasjonen av den isotermiske transformasjonen er en hyperbola. Jo større produkt s. V av denne transformasjonen, jo lenger unna vil denne hyperbola være fra aksene i grafen. Navnet gitt til denne kurven representert i grafen er isoterm.
Av Mariane Mendes
Uteksamen i fysikk
Vil du referere til denne teksten i et skole- eller akademisk arbeid? Se:
TEIXEIRA, Mariane Mendes. "Hva er isotermisk transformasjon?"; Brasilskolen. Tilgjengelig i: https://brasilescola.uol.com.br/o-que-e/fisica/o-que-e-transformacao-isotermica.htm. Tilgang 28. juni 2021.

