Inntil 1824 ble det antatt at de termiske maskinene som ble bygget, kunne fungere perfekt, det vil si at man trodde at de kunne nå 100% avkastning, eller noe i nærheten av det verdi. Med andre ord trodde forskere den gangen at de kunne benytte seg av all termisk energi levert til disse maskinene - det vil si at de trodde de kunne forvandle all den energien til arbeid.
Ingeniør Sadi Carnot var den gang ansvarlig for å gjøre demonstrasjoner der det var umulig å oppnå 100% avkastning. Sadi foreslo at en ideell teoretisk termisk maskin ville fungere gjennom en bestemt syklus, nå kalt Carnot-syklus.
I sin demonstrasjon konseptualiserte Carnot to postulater, som ble foreslått allerede før termodynamikkens første lov ble uttalt. Se hva Carnots postulater uttaler:
1. postulat av Carnot
- Ingen maskiner som opererer mellom to faste temperaturer kan gi større enn Carnots ideelle maskin som opererer mellom de samme temperaturene.
2. postulat av Carnot
- Når du bruker mellom to temperaturer, må maskinen ideell av Carnot har samme ytelse, uansett driftsvæske, og er fullstendig reversibel, uten å tilsette energi.
I følge postene som er fremlagt av Carnot, kan vi se garantien for at effektiviteten til en termisk motor er en funksjon av temperaturene i de varme og kalde kildene. Imidlertid, ved å fikse temperaturene til disse kildene, er Carnots teoretiske maskin den som klarer å ha høyest effektivitet.
Carnot-syklusen er en idealisert, reversibel syklus der driftsvæsken er en perfekt gass, som tilsvarer to transformasjoner. isotermer det er to adiabatisk, ispedd. Prosessene beskrevet av gassen i denne syklusen er:
Ikke stopp nå... Det er mer etter annonseringen;)
1.°) isoterm ekspansjon DA, hvor gassen er i kontakt med TA (varmekilde) med konstant temperatur, og mottar en mengde varme QA fra den.
2.°) adiabatic expansion AB, hvor det ikke er varmeutveksling med miljøet. Systemet utfører arbeid med en reduksjon i intern energi og derfor i temperatur.
3.°) BC isotermisk sammentrekning, hvor gassen er i kontakt med systemet med konstant temperatur TB (kald kilde), noe som gir den en mengde varme QB.
4.°) adiabatisk sammentreknings-CD, hvor gassen ikke bytter varme med miljøet. Systemet mottar arbeid, som tjener til å øke sin indre energi og dermed temperaturen.
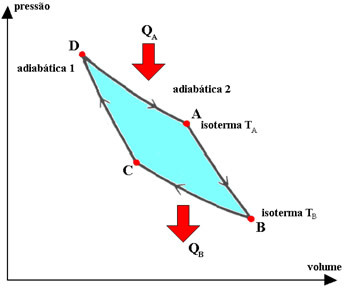
I Carnot-syklusen, varmevekslet (SpørsmålDE og QB) og termodynamiske temperaturer (TDE og TB) av varme og kalde kilder er proporsjonale, forholdet er:

Ved å erstatte effektivitetsligningen til en termisk maskin får vi for Carnot-maskinen:
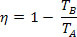
Med tanke på temperaturen på den kalde kilden (TB) lik null kelvin (absolutt null), har vi η = 1 eller η = 100%. Imidlertid strider dette faktum med den andre loven om termodynamikk, som garanterer at en inntekt på 100%, noe som får oss til å konkludere med at ingen fysiske systemer kan ha en temperatur lik null absolutt.
Av Domitiano Marques
Uteksamen i fysikk
Vil du referere til denne teksten i et skole- eller akademisk arbeid? Se:
SILVA, Domitiano Correa Marques da. "Carnot Machines"; Brasilskolen. Tilgjengelig i: https://brasilescola.uol.com.br/fisica/maquinas-carnot.htm. Tilgang 27. juni 2021.



