På forbrenningsreaksjoner de er til stede i mange aspekter av vårt daglige liv. For eksempel er hovedkildene for energiproduksjon resultatet av forbrenning eller forbrenning av visse drivstoff, som etanol, bensin, kull, blant andre. Videre er energien vi trenger for å overleve og for å gjøre arbeid resultatet av forbrenningsreaksjoner som foregår i cellene når vi "brenner" maten vi spiser.
Men hva skal til for å få en forbrenningsreaksjon?
Det er behov for tre ting:
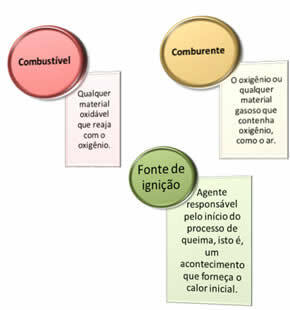
Disse tre faktorene utgjør brann trekant, fordi når forbrenningsreaksjonen begynner, opprettholder den frigjorte energien reaksjonen og lar den fortsette til drivstoff, oksidasjonsmiddel eller varme (frigitt energi) er borte. Dette betyr at det vil være en Kjedereaksjon.
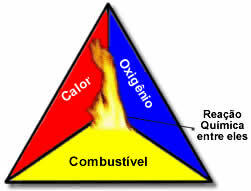
For eksempel, hvis noen kaster en tent sigarett i en skog, vil det være brann (forbrenningsreaksjon). I dette tilfellet vil Busk det er brensel, O oksygen i luften atmosfærisk er oksidasjonsmiddel det er sigarett tent var den antennelseskilde. Denne brenningen vil fortsette til en av de tre faktorene er eliminert. Hvis brannmenn kaster vann, vil varmen bli eliminert. Men selv om ingenting er gjort for å stoppe denne brenningen, vil det slutte på et tidspunkt, det vil si når drivstoffet (skogen) går tom.
Som allerede nevnt frigjøres varme i disse reaksjonene, slik at forbrenning er en eksoterm reaksjon. Imidlertid er denne typen reaksjon ufullstendig forbrenning. For å forstå hvorfor, se forskjellen mellom fullstendig og ufullstendig forbrenning:
Ikke stopp nå... Det er mer etter annonseringen;)
Fullstendig forbrenning:
Når vi analyserer organiske forbindelser som drivstoff, må vi:
| DE fullstendig forbrenning det vil oppstå når karbonkjeden brytes og alle karbonatomer i karbonkjeden er fullstendig oksidert. |
| Du dannede produkter av hydrokarboner vil være CO2 (karbondioksid) og H2O (Vann). |
Observer fullstendig forbrenning av isoktan, som er en av komponentene i bensin.
Ç8H18 (g) +25/2 O2 (g) → 8 CO2 (g) + 9 am2O(1)
Ufullstendig forbrenning
| I dette tilfellet er det ikke nok oksidasjonsmiddel, det vil si nok oksygen til å forbrenne alt drivstoff. |
| Dermed er produktene som dannes CO (karbonmonoksid) og H2O. |
Observer samme forbrenning av isoktan, men nå ufullstendig:
Ç8H18 (g) + 17/2 O2(g) → 8 CO (g) + 9 am2O(1)
Brenning av skog er et eksempel, da de resulterende utslippene består av CO og bestemt materiale, som sot (C), samt aske og andre enkle og komplekse organiske forbindelser. Nitrogenoksid, ozon og aldehyder kan også dannes som et resultat av sekundære reaksjoner på grunn av tilstedeværelsen av andre komponenter i luften.
Ç8H18 (g) + 9/2 O2 (g) → 8C (g) + 9 am2O(1)
Av Jennifer Fogaça
Uteksamen i kjemi
Brasil skolelag
Vil du referere til denne teksten i et skole- eller akademisk arbeid? Se:
FOGAÇA, Jennifer Rocha Vargas. "Komplett og ufullstendig forbrenning"; Brasilskolen. Tilgjengelig i: https://brasilescola.uol.com.br/quimica/combustao-completa-incompleta.htm. Tilgang 27. juni 2021.