Spesifikk varme er en mengde som er studert av fysikk som relaterer mengden varme mottatt av et stoff og dets termiske variasjon.
Også kalt termisk kapasitet, indikerer denne størrelsen mengden varme som trengs for et gram av et hvilket som helst stoff for å gjennomgå en variasjon temperatur tilsvarende 1 ° C, i tillegg til å indikere materialets oppførsel når den utsettes for en varmekilde.
Spesifikk varme er direkte knyttet til det fysikkområdet som kalles Kalorimetri, som studerer energioverføringer fra en kropp med høyere temperatur til en annen kropp med lavere temperatur.
I denne studien er den spesifikke varmen til stede i definisjonen av den fornuftige varmen og den termiske kapasiteten til et materiale, da noen fenomener kan forstås bedre fra definisjonen av varme spesifikk.
Og jo større spesifikk varme, jo større mengde varme som må tilføres eller fjernes fra stoffet, slik at den har den termiske variasjonen.
Vann, for eksempel, sammenlignet med andre stoffer, har den høyeste spesifikke varmen, tilsvarende 1 cal / g.ºC.
Sammenligningstabell med spesifikke varmen
Andre stoffer og materialer har også sine egne spesifikke varmeverdier, som vist i tabellen nedenfor:
| Substans | Spesifikk varme (kal / g.ºC) |
| Vann | 1 kal / g. ° C |
| Etyl alkohol | 0,58 cal / g. ° C |
| Aluminium | 0,22 cal / g. ° C |
| Luft | 0,24 cal / g. ° C |
| Sand | 0,2 cal / g. ° C |
| Karbon | 0,12 cal / g. ° C |
| Lede | 0,03 cal / g. ° C |
| Kobber | 0,09 cal / g. ° C |
| Jern | 0,11 cal / g. ° C |
| Is | 0,50 cal / g. ° C |
| Hydrogen | 3,4 cal / g. ° C |
| tre | 0,42 cal / g. ° C |
| Nitrogen | 0,25 cal / g. ° C |
| Oksygen | 0,22 cal / g. ° C |
| Glass | 0,16 cal / g. ° C |
Spesifikk varmeformel
For å vite den spesifikke varmen til stoffer, er det nødvendig å bruke følgende formel:
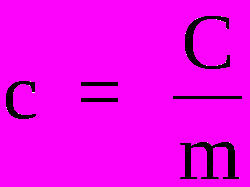
Hvor,
ç - spesifikk varme (cal / g ° C eller J / Kg. K)
Ç - termisk kapasitet (cal / ° C eller J / K)
m - masse (g eller kg)
I International System (SI) måles spesifikk varme i J / Kg. K (joule per kilo og per kelvin). Imidlertid er det mest brukte målet i cal / g ° C (kalori per gram og per grad celsius).
Se også betydningen av varme og temperatur.
