DE opprinnelse til Periodiske tabell skjedde tidlig på 1800-tallet, rundt 1829, da kjemikere på den tiden bestemte seg for å foreslå måter å organisere kjemiske elementer kjent til da.
På begynnelsen av 1800-tallet hadde kjemikere kunnskap om flere egenskaper (tetthet, atommasse, reaktivitet, smeltepunkt, kokepunkt, fysisk tilstand) av tretti kjemiske elementer. Denne kunnskapen fungerte som utgangspunkt for opprinnelsen til det periodiske systemet.
Over 200 år prøvde flere kjemikere å foreslå måter å organisere de kjemiske elementene, det vil si Det periodiske systemet vi kjenner i dag, hadde faktisk forskjellige opprinnelser, som gjennom historien var mange forsøk utført.
Tankekart: Opphavet til det periodiske systemet
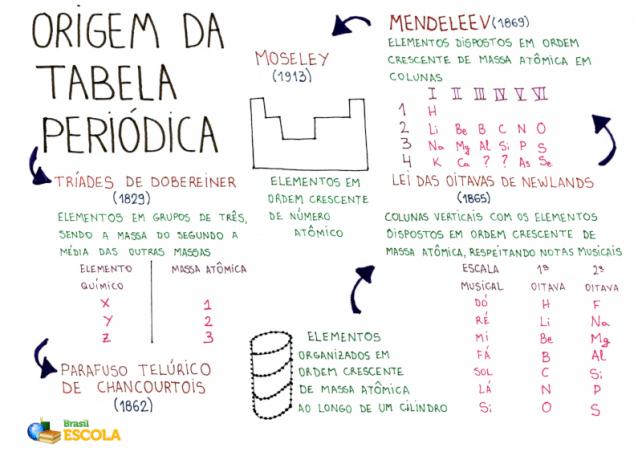
* For å laste ned dette tankekartet, Klikk her!
Her er noen av kjemikerne som har utmerket seg i å prøve å organisere elementene i et bord.
Dobereiner triader

Illustrasjon av Johann Wolfgang Dobereiner *
I år 1829 organiserte den tyske kjemikeren Johann Wolfgang Dobereiner det første periodiske systemet i historien. Den inneholdt de tretti kjemiske elementene som var kjent til da, og ble av ham kalt Dobereiner-triadene.
DE Dobereiner periodiske tabell det ble kalt en triade fordi elementene var organisert i grupper på 3. Hver gruppe hadde grunnstoffer som hadde lignende kjemiske egenskaper.
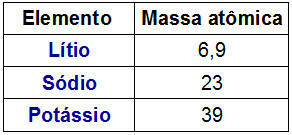
Representasjon av en Dobereiner-triade
Et interessant faktum om Dobereiner-triader er at atommasse av det sentrale elementet i triaden var nøyaktig resultatet av det aritmetiske gjennomsnittet mellom atommassene til de andre to elementene i triaden.

Tellurisk skrue av Alexandre de Chancourtois
I år 1862, den franske geologen og mineralogen Alexandre de Chancourtois han bestemte seg for å foreslå en organisering av de kjemiske elementene som den gang var kjent for å lette deres anvendelse i mineralogi. DE Chancourtois bord det ble kalt tellurskrue.

Representasjon av Chancourtois tellurskrue
Chancourtois distribuerte de kjemiske elementene (mørke flekker på bildet) i stigende rekkefølge av atommasse langs et spiralbånd som eksisterer i en sylinder. Med denne organisasjonen observerte Chancourtois at elementer plassert på samme vertikale linje hadde lignende kjemiske egenskaper.
Loven om oktaver
Ikke stopp nå... Det er mer etter annonseringen;)
Loven om oktaver var navnet som ble foreslått av den engelske kjemikeren J.A.R. Newlands, i året 1865, til det periodiske systemet. Fordi Newlands også er musiker, dekket han opp bordet i henhold til notene (do, there, re, mi, fa, sol, there, si).
Newlands organiserte de 61 kjemiske elementene som var kjent på den tiden i stigende rekkefølge av atommassen og plasserte dem i vertikale kolonner. Hver av de vertikale kolonnene hadde syv elementer.
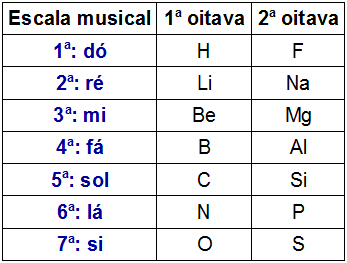
To oktav representasjon av Newlands
Newlands observerte at kjemiske elementer i samme horisontale linje med forskjellige oktaver hadde lignende kjemiske egenskaper. Dermed hadde det første elementet i en oktav lignende egenskaper som det første elementet i den andre oktaven, og så videre.
Mendeleevs periodiske system

Illustrasjon av kjemikeren Mendeleev **
Mendeleev, under arbeidet med de kjemiske elementene, hadde han for vane å skrive ned egenskapene til hver av dem på kort. På et tidspunkt, i år 1869, bestemte han seg for å plassere disse tokens i stigende rekkefølge av atommassen.
Rett etter å ha ordnet elementene i stigende rekkefølge av atommassen, beholdt Mendeleev mønsteret, men posisjonerte elementene i horisontale og vertikale kolonner, med respekt for egenskapene og likhetene til elementer.
Moseley periodiske system
I året 1913 var den engelske kjemikeren HenryMoseley, basert på tabellen foreslått av Mendeleev, samlet det periodiske bordet i mønstrene vi kjenner til i dag.
I motsetning til Mendeleev ordnet Moseley elementene i stigende rekkefølge av atomnummer, holdt organisasjonen i horisontale og vertikale kolonner, men plasserte elementene med de samme kjemiske egenskapene i de samme vertikale kolonnene.
gjeldende periodiske tabell
Etter 1913 gjennomgikk ikke det periodiske systemet som Moseley foreslo, noen større endringer, det gjennomgikk faktisk noen oppdateringer ettersom noen kjemiske elementer ble oppdaget.
Sammenlignet med den nåværende tabellen, viste ikke Moseley-tabellen for eksempel de kjemiske elementene med atomnummer mellom 110 og 118. Også aktinidserien var plassert over lantanidserien.
DE siste oppdatering utført i det periodiske systemet var i 2016, da elementene 113, 115, 117 og 118 offisielt ble en del av det.
* Bildekreditt: Yangchao/ shutterstock. Inc.
** Bildekreditt: Olga Popova/ shutterstock. Inc.
Av meg. Diogo Lopes Dias