osmoskopi er felleseie (de andre er tonoskopi, ebullioskopi og kryoskopi) som studerer forekomsten av osmose mellom to løsninger med forskjellige konsentrasjoner, hvorav den ene er mer konsentrert enn den andre.
Merk: Colligative egenskaper oppstår når en ikke-flyktig løsemiddel tilsettes et løsningsmiddel.
Som for eksempel osmoskopi studere osmose, er det viktig å vite Hva er dette fenomenet. For dette vil vi bruke løsningene nedenfor, som er atskilt med en semipermeabel membran:
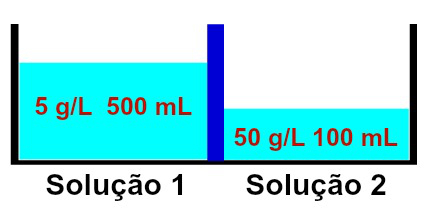
Representasjon av løsninger som har forskjellige konsentrasjoner
Det observeres at løsning 1 inneholder en konsentrasjon på 5 g / L og et volum på 500 ml, mens løsning 2 har en konsentrasjon på 50 g / l og et volum på 100 ml, atskilt med en membran semipermeable. Løsning 2 er mer konsentrert enn løsning 1, og derfor må osmose forekomme mellom dem.
Osmose må nødvendigvis skje fra løsning 1 til løsning 2, siden løsning 1 er mindre konsentrert. Under denne forekomsten krysser en del av løsningsmidlet den semipermeable membranen, noe som gjør løsningen til volum 2 øke og volumet av løsning 1 reduseres, til begge løsningene begynner å ha samme konsentrasjon, det vil si isotoni.

Endring i høyden på løsning 1 og 2 på grunn av forekomst av osmose
Merk: Isotoniske medier er de som har samme konsentrasjon.
Ifølge osmoskopiosmose finner sted fordi det maksimale damptrykket til løsningsmidlet i den mindre konsentrerte løsningen er større enn det til løsningsmidlet i den mer konsentrerte løsningen. Nå, hvis vi ønsker å forhindre forekomst av osmose, er det bare å utøve press på den mest konsentrerte løsningen:
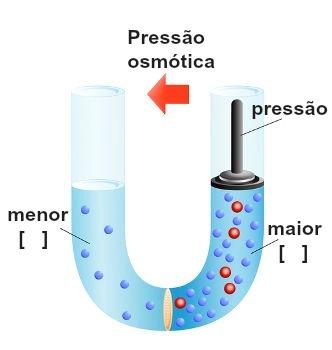
Representasjon av utførelsen av press på den mest konsentrerte løsningen
Dette trykket, som utøves på den mest konsentrerte løsningen for å blokkere eller til og med reversere osmose, kalles osmotisk trykk og er representert med symbolet π. Den skal være direkte proporsjonal med konsentrasjonen av løsningen.
Mulige tolkninger av osmotisk trykk
I følge konklusjonene fra osmoskopi, hver løsning har et osmotisk trykk, siden dette er relatert til konsentrasjonen, en karakteristikk som er tilstede i hver løsning.
Ikke stopp nå... Det er mer etter annonseringen;)
Når vi sammenligner ett medium eller en løsning med et annet, kan vi bruke følgende ord:
Hypertonisk: når det ene mediet har et osmotisk trykk som er større enn det andre;
hypotonisk: når det ene mediet har et osmotisk trykk lavere enn det andre;
Isotonisk: når de to mediene eller løsningene har samme osmotiske trykk.
Når man sammenligner det osmotiske trykket til to løsninger A og B, representert av πDE og πB, kan vi si at:
Hvis det osmotiske trykket til A og B er likt, vil midlene eller løsningene være isotoniske:
πDE = πB
Hvis det osmotiske trykket til A er større enn det osmotiske trykket til B, vil medium A være hypertonisk i forhold til B:
πDE> πB
Hvis det osmotiske trykket til B er lavere enn det osmotiske trykket til A, vil medium B være hypotonisk i forhold til B:
πB< πDE
Formel for beregning av osmotisk trykk
π = M.R.T
I denne formelen:
π = er det osmotiske trykket
M = er konsentrasjon i mol / l
R = er den generelle gasskonstanten (0,082 for trykk i atm; 62,3 for trykk i mmHg)
T = temperatur i Kelvin
Da konsentrasjonen i mol / L har en bestemt formel, som vist nedenfor:
M = m1
M1.V
Vi kan erstatte den i den osmotiske trykkformelen:
π = m1.R.T
M1.V
Merk: Hvis løsemidlet i løsningen er ionisk, må vi bruke Van't Hoff korreksjonsfaktor (i) i uttrykket for osmotisk trykkberegning:
π = M.R.T.i
Eksempel på osmotisk trykkberegning
Eksempel: (UF-PA) En løsning som inneholder 2 mg av et nytt antibiotikum, i 10 ml vann, ved 25 ºC, gir et osmotisk trykk på 0,298 mmHg. Så molekylmassen til dette antibiotikumet er omtrent:
a) 3000
b) 5200
c) 7500
d) 12500
e) 15300
Dataene som ble gitt av øvelsen var:
π = 0,298 mmHg
T = 25 OC eller 298 K (etter tilsetning med 273)
m1 = 2 mg eller 0,002 g (etter divisjon med 1000)
V = 10 ml eller 0,01 l (etter divisjon med 1000)
R = 62,3 mmHg
For å løse denne øvelsen, bruk bare tilgjengelige data i uttrykket for å beregne det osmotiske trykket, som følger:
π = m1.R.T
M1.V
0,298 = 0,002.62,3.298
M1.0,01
0.298.M1.0,01 = 37,1308
0.00298.M1 = 37,1308
M1 = 37,1308
0,00298
M1 = 12460 u
Av meg. Diogo Lopes Dias
Vil du referere til denne teksten i et skole- eller akademisk arbeid? Se:
DAGER, Diogo Lopes. "Hva er osmoskopi?"; Brasilskolen. Tilgjengelig i: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-osmoscopia.htm. Tilgang 28. juni 2021.