dobbelt salt er navnet gitt til en av klassifiseringene som uorganiske salter kan motta. De andre klassifiseringene er: enkle, alun, hydroksylert, hydrogenert og hydrert. For å bli karakterisert som et dobbelt salt, må et uorganisk salt ha en av kombinasjonene beskrevet nedenfor:
En kation (Y) og to anioner (X og W), og er representert med følgende formel:
YXW
Et anion (X) og to kationer (Y og Z), og er representert med følgende formel:
YZX
Merk: Disse saltene dannes når en nøytraliseringsreaksjon utføres mellom to baser annerledes og en syre, eller mellom to forskjellige syrer og en base.
Navngivningsregel for dobbelt salt
Å nevne et dobbelt salt, det er først og fremst nødvendig å kjenne dens konstitusjon, fordi det for hver type dobbeltsalt er en spesifikk navneregel, som kan sees nedenfor:
a) Nomenklaturregel for dobbeltsalt med to kationer
Når en dobbelt salt har to kationer, må vi bruke følgende regel:

Nomenklaturregel brukt for dobbeltsalter med to kationer
Følgende er to eksempler på anvendelse av denne navngivningsregelen:
Første eksempel: Linje4s
Dette saltet består av:
Anion: sulfid (S-2);
Mer elektropositivt kation: litium (Li+1);
Mindre elektropositivt kation: ammonium (NH4+1).
Derfor er navnet litium (dobbelt) ammoniumsulfid.
2. eksempel: RbCaBO3
Dette saltet består av:
Anion: borat (BO3-3);
Mer elektropositivt kation: rubidium (Rb+1);
Mindre elektropositivt kation: kalsium (Ca+2).
Dermed er navnet borat (dobbelt) av rubidium og kalsium.
b) Nomenklaturregel for dobbeltsalt med to anioner
Når en dobbelt salt har to anioner, må vi bruke følgende regel:
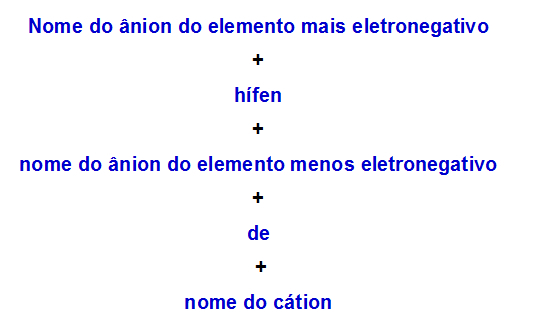
Nomenklaturregel brukt for dobbeltsalter med to anioner
Ikke stopp nå... Det er mer etter annonseringen;)
Her er to eksempler på bruk av denne regelen:
Første eksempel: MgFI
Dette saltet består av:
Kation: magnesium (Mg+2);
Mest elektronegative anion: fluor (F-1);
Mindre elektronegativ anion: jodid (I-1).
Derfor heter navnet magnesiumfluoridjodid.
2. eksempel: ZnNO2br
Dette saltet består av:
Kation: sink (Zn+2);
Mer elektronegativ anion: nitritt (NO2-1);
Mindre elektronegativ anion: bromid (Br-1).
Derfor er navnet sinksnitritbromid.
Montering av formelen til et dobbelt salt fra nomenklaturen
a) For dobbelt salt med to kationer
Konstruksjonen av formelen til a dobbelt salt det avhenger av å kjenne navnet sitt, som er standardisert som i alt salt, det vil si først kationen og deretter anionet. Siden dobbeltsaltet kan ha to kationer, følger rekkefølgen og plasseringen i formelen det gitte navnet.
Første eksempel: barium nikkel pyrofosfat II
Dette saltet inneholder fosfat (P2O7), barium (Ba+2) og nikkel II (Ni+2), kationer skrevet i den sekvensen. Så formelen er BaNiP2O7.
2. eksempel: kobber II fosfat og gull I
Dette saltet har fosfat (PO4-3), kobber II (Cu+2) og gull I (Au+1), kationer skrevet i den sekvensen. Derfor er formelen CuAuPO4.
b) For dobbelt salt med to anioner
I tilfelle dobbelt salt med to anioner følger vi også når vi plasserer anionene i formelen, rekkefølgen slik de vises i det gitte navnet.
Første eksempel: nikkel sulfat-jodid III
Dette saltet har sulfationer (SO4-2) og jodid (I-1), skrevet i denne sekvensen, og nikkel III-kationen (Ni+3). Så formelen er NiSO4JEG.
2. eksempel: blycyanidfosfat IV
Dette saltet har fosfatanioner (PO4-3) og cyanid (CN-1), skrevet i denne sekvensen, og blykation IV (Pb+4). Så formelen er PbPO4CN.
Av meg. Diogo Lopes Dias
Vil du referere til denne teksten i et skole- eller akademisk arbeid? Se:
DAGER, Diogo Lopes. "Hva er et dobbelt salt?"; Brasilskolen. Tilgjengelig i: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-um-sal-duplo.htm. Tilgang 28. juni 2021.
Saltnomenklatur, saltklassifisering, anionnavn, kationnavn, jernsulfat, jernholdig sulfat, nitrat av sølv, kaliumklorid, natriumklorid, kalsiumklorid, sølvnitrat, kobbersulfat, karbonat kalsium.
Kjemi

Hverdagssalter, kalsiumkarbonat, natriumklorid, natriumfluorid, kaliumnitrat, natriumnitrat natrium, natriumkarbonat, natriumbikarbonat, natriumbikarbonat, natriumsulfitt, saltpeter, soda.