Zuren en basen zijn twee chemische functies die als tegengestelden worden beschouwd., dit komt omdat hun eigenschappen meestal omgekeerd zijn. Als we bijvoorbeeld voedingsmiddelen in ons dagelijks leven beschouwen die zuur zijn, zullen we zien dat hun smaak over het algemeen zuur is, zoals bij citroen. Basisvoedingsmiddelen hebben echter een samentrekkende smaak (die de mond "bindt"), zoals een groene banaan.
Maar het identificeren van een stof als zuur of basisch alleen op basis van smaak, maar ook als een methode die veel kans heeft om te falen, het is ook zeer gevaarlijk omdat er veel zuren en basen zijn die sterk, giftig en zelfs dodelijk zijn, zoals zuur. zwavelzuur (H2ENKEL EN ALLEEN4), gebruikt in autobatterijen, en natriumhydroxide (NaOH), in de handel bekend als bijtende soda.
Organoleptische eigenschappen (eigenschappen die onze zintuigen betreffen, zoals smaak en geur) zijn dus niet degene die worden gebruikt om zuren en basen te identificeren. Noteer hieronder andere eigenschappen van deze organische functies die dienen om ze te vergelijken en te onderscheiden:
- Oplosbaarheid in water:
U zuren meestal gezond zijn oplosbaar in water, terwijl de meeste basissen é onoplosbaar. Alkalimetaalbasen zijn oplosbaar, aardalkalimetaalbasen zijn slecht oplosbaar en basen van andere metalen zijn onoplosbaar (een uitzondering is ammoniumhydroxide, NH4OH, dat alleen in waterige oplossing bestaat, waardoor het ammoniakgas in water borrelt en daarom daarin oplosbaar is).
Als we zeggen "onoplosbaar", bedoelen we dat deze stoffen praktisch onoplosbaar zijn, omdat geen enkele stof volledig onoplosbaar is in water.
- Structuur:
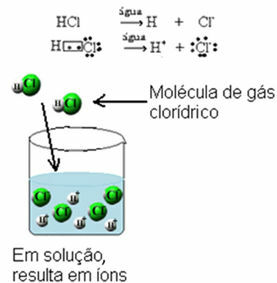
Al de zuren zijn moleculair, dat wil zeggen, gevormd door covalente bindingen waarin elektronen worden gedeeld. Een voorbeeld is zoutzuur, dat wordt gevormd door een elektronenpaar te delen tussen waterstof en chloor:

al de basen kunnen ionisch of moleculair zijn. Die met alkali- en aardalkalimetalen zijn ionisch en de andere zijn moleculair.
Voorbeelden:
NaOH: ionische base gevormd door Na-ionen+ en oh-;
NH4OH: moleculaire basis van ammoniak in water.
- Elektrische geleidbaarheid:
Alle zuren geleiden alleen elektrische stroom als ze in water zijn opgelost, omdat wanneer ze zich in een waterig medium bevinden, ze ionisatie ondergaan, dat wil zeggen dat ze ionen afgeven.
Voorbeeld:
Alle de basen geleiden ook elektrische stroom in oplossing., aangezien de ionische dissociatie ondergaan (de ionen die al in de formule aanwezig zijn vrijgeven) en de moleculaire ionisatie ondergaan, reageren met water en ionen vrijgeven. Bij Alkalimetaalbases geleiden ook elektrische stroom wanneer ze in vloeibare (gesmolten) toestand zijn.
- Actie op indicatoren:
U zuur-base indicatoren zijn natuurlijke of synthetische stoffen die een kleurverandering ondergaan wanneer ze in contact komen met een zuur of een base. Als een zuur ervoor zorgt dat de indicator van kleur verandert, zal de base de indicator terugbrengen naar zijn oorspronkelijke kleur en vice versa.
Fenolftaleïne is bijvoorbeeld een veelgebruikte zuur-base-indicator en in een basisch medium wordt het een zeer intens roze; al in een zuur medium wordt het kleurloos. Lakmoespapier is ook een goede indicator, omdat het in een zuur rood wordt; en op één basis wordt het blauw.
Dit dient ook om het pH-verschil aan te geven dat bestaat tussen zuren en basen.
- PH:
Een medium dat als neutraal wordt beschouwd, heeft een pH die gelijk is aan 7, zoals het geval is met gedestilleerd water.
Zuren hebben een pH van minder dan 7, terwijl de basen hebben een pH groter dan 7.
Voorbeelden van oplossingen met een pH in de buurt van die aangegeven door de schaal:
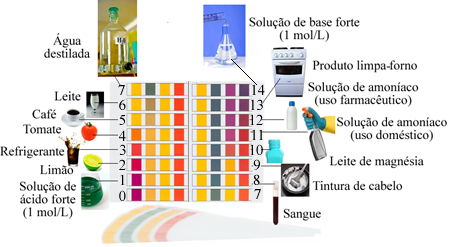
- Wederzijdse actie:
Wanneer ze in contact worden gebracht, reageren zuren en basen met elkaar, waarbij ze elkaar neutraliseren, dat wil zeggen, de pH van het medium neutraal maken. Dit komt omdat het H-kation+ van het zuur reageert met het OH-anion- van de basis en vormt water. Dit type reactie wordt a. genoemd neutralisatie-reactie en het produceert ook een zout.
Door Jennifer Fogaça
Afgestudeerd in scheikunde
Bron: Brazilië School - https://brasilescola.uol.com.br/quimica/comparacao-entre-acidos-bases.htm

