U metalen het zijn chemische elementen die als hun belangrijkste fysieke kenmerk het vermogen hebben om elektronen te verliezen en bijgevolg metallische kationen te vormen. Om deze reden kunnen ze twee soorten chemische bindingen maken: de ionische binding en de metalen binding.
DE ionbinding treedt op wanneer een metaal interageert met een element van metaalachtige aard, wat a ametaal of waterstof. In dit type binding hebben we het verlies van elektronen door de metalen en de winst van elektronen door de niet-metalen of waterstof.
al de metalen binding ontstaat tussen de atomen van een enkel metallisch element. Dit type binding komt alleen voor tussen de atomen van een enkel metaal en uitsluitend omdat een metaal geen chemische binding tot stand kan brengen met een ander ander metallisch element.
Algemene kenmerken van metalen
vaste stoffen bij kamertemperatuur, met uitzondering van kwik;
Ze zijn briljant;
Ze hebben hoge smelt- en kookpunten;
Ze zijn over het algemeen zilver van kleur, met uitzondering van goud, dat goudkleurig is, en koper, dat roodachtig is;
Zuivere metalen worden gevormd door clusters van atomen (van een enkel chemisch element) die kristalroosters worden genoemd.
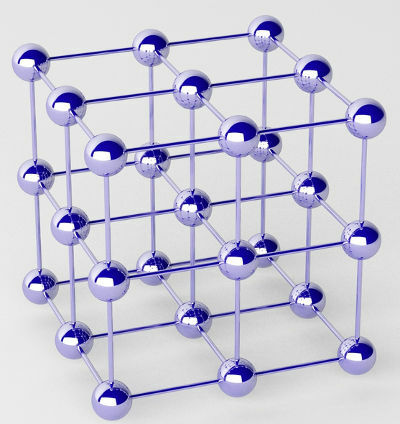
Weergave van het kristalrooster van een metaal
Principes van metaalverlijming
Bij metalen binding, zijn de kristallijne roosters die de metalen vormen eigenlijk een ionencluster (alleen samengesteld uit kationen en elektronen). De elektronen die aanwezig zijn in de valentielaag van de metaalatomen worden gedelokaliseerd, dat wil zeggen, ze verlaten de valentielaag, waardoor het atoom een kation wordt (deficiënt aan elektronen).
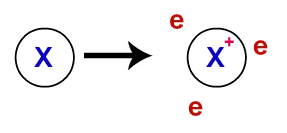
Vertegenwoordiging van gedelokaliseerde elektronen uit de valentieschil
Nadat ze zijn gedelokaliseerd, beginnen de elektronen van de metaalatomen de kationen te omringen en een echte "elektronenzee" te vormen. Elk van de elektronen die in deze zee aanwezig zijn, heeft het vermogen om vrij door het kristalrooster van het metaal te bewegen.

Vertegenwoordiging van het elektronenzeemodel
OPMERKING: Elektronen "uit de zee" kunnen het kristalrooster niet verlaten en er doorheen bewegen.
Eigenschappen van metalen gerechtvaardigd door metallische binding
a) Kneedbaarheid
Door middel van een metaal is het mogelijk om platen van verschillende diktes en platen te produceren. Het is dankzij deze eigenschap van metalen dat we verschillende objecten kunnen bouwen, zoals messen, zwaarden, enz.

Het blad van een zwaard is gemaakt van een metaal
b) Geleidbaarheid
Metalen zijn over het algemeen goede geleiders van elektrische stroom en warmte. Wanneer een metaal in contact is met een warmtebron of een bron van elektrische stroom, kan het deze geleiden.

Een aluminium pan in de vlam van een kachel wordt door geleidbaarheid helemaal heet.
c) Vervormbaarheid
Door een metaal kunnen we draden produceren. Het gebruik van een metaal in de vorm van draden vergemakkelijkt het gebruik ervan, vooral met betrekking tot elektrische geleidbaarheid.

Een metaal, zoals koper, kan worden gebruikt om draden te produceren.
Door mij Diogo Lopes Dias
Bron: Brazilië School - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-ligacao-metalica.htm
