Wanneer de benzeenring al een substituent heeft, zal dit radicaal alle andere H-substituties op de ring beïnvloeden. Deze substituent kan ortho- en para-director of meta-director zijn. Maar de vragen rijzen:
| Wat zorgt ervoor dat de groep die aan de benzeenring is bevestigd de richting en reactiviteit van de substitutiereactie beïnvloedt? |
| Wat maakt bepaalde groepen doeladviseurs (uitschakelen) en anderen ortho-para (activeren)? |
Deze twee vragen worden beantwoord door de roepingen te begrijpen. elektronische effecten dat deze groepen sporten in de ring. Dit effect treedt op als gevolg van de elektronegativiteitsverschil tussen de elementen, zoals de substituent zal polariseren de bindingen van de aromatische kern, afwisselend een positief karakter inducerend voor sommige ringkoolstofatomen, terwijl andere een negatief karakter behouden.
| Er zal een nieuwe substitutie plaatsvinden in de koolstofatomen die karakter hebben negatief. |
Laten we eens kijken hoe deze elektronische effecten optreden in de aromatische ring, rekening houdend met de volgorde van elektronegativiteit van de elementen: F > O > N > Cl > Br > S > C > I > H.
1e geval: Radicaal activeren of ortho-naar-director:
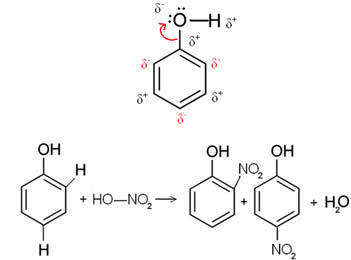
In het geval onder het benzol (fenol) molecuul is zuurstof bijvoorbeeld het meest elektronegatieve element, dus het trekt elektronen naar zich toe, waardoor de koolstof een gedeeltelijk positieve lading krijgt, wat leidt tot alternerende ringpolarisatie. De posities die negatief zijn, zijn precies de ortho- en paraposities. Dat is de reden de -OH-groep is een activerend radicaal of ortho-naar-directors. Dit is te zien in de onderstaande fenolnitratiereactie, die aanleiding geeft tot o-nitrofenol en p-nitrofenol als producten:
2e geval: radicale of meta-leider deactiveren:
Beschouw nu het geval van nitrobenzeen:
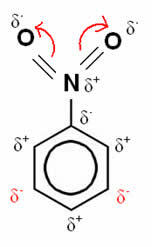
In dit voorbeeld blijft zuurstof het meest elektronegatieve element, dus het trekt de bindingen met stikstof naar zich toe, die gedeeltelijk positief geladen is, waardoor het eraan gehechte koolstofatoom negatief wordt gepolariseerd en zo achtereenvolgens. Dus de positie die negatief wordt en het meest vatbaar voor vervanging is de positie the doel, zijnde daarom een uitschakelen.
Bekijk nu in meer detail dit elektronische effect, dat resonantie-effect.
| resonantie-effect het is de aantrekking of afstoting van elektronen op π (pi) bindingen van dubbele of driedubbele bindingen, wanneer ze resoneren met de benzeenring zelf. |
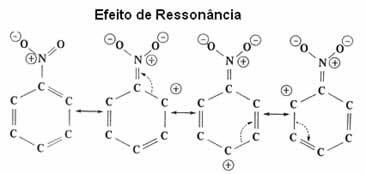
Zoals te zien is, deactiveert de NO2-groep de ring, omdat deze er elektronen uit haalt en de elektronendichtheid verlaagt. Dus de groep die zal aanvallen en de substitutie zal maken (elektrofiel) is positief, dus het zal bij voorkeur de metapositie aanvallen die een negatieve lading heeft gekregen.
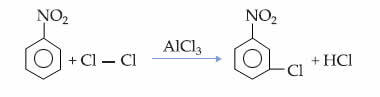
Dit feit is te zien in de monochloreringsreactie van nitrobenzeen, waarbij de substitutie alleen plaatsvindt in de meta-positie:
Door Jennifer Fogaça
Afgestudeerd in scheikunde
Brazilië School Team
Bron: Brazilië School - https://brasilescola.uol.com.br/quimica/efeitos-eletronicos-radicais-meta-orto-para-dirigentes.htm