Het atomaire volume is niet het volume dat een atoom inneemt, maar verwijst naar de volume ingenomen door een vaste hoeveelheid van een bepaald aantal atomen van een chemisch element.
In de tekst Chemish element, werd aangetoond dat een element overeenkomt met een reeks atomen met hetzelfde atoomnummer, dat wil zeggen hetzelfde aantal protonen in de kern. De hoeveelheid die is vastgesteld om het atomaire volume te berekenen, is de waarde van constante van Avogadro, wat gelijk is aan 6,02. 1023 atomen, wat overeenkomt met 1 mol van het element.
Dus dat kunnen we zeggen het atomaire volume is het volume dat 1 mol atomen (of 6,02). 1023 atomen) van een element inneemt.
Deze hoeveelheid kan worden berekend als we de dichtheid van het vastestofelement en de massa van 1 mol atomen van dat element kennen. Bedenk bijvoorbeeld dat de dichtheid van natrium (Na) gelijk is aan 0,97 g/cm3 en dat 6.02. 1023 natriumatomen hebben een massa gelijk aan 23,0 g. We kunnen dan, uit de formule van dichtheid, komen tot het atomaire volume van natrium. Zie hoe:
dichtheid = pasta
volume
atoomvolume = massa van 6,02. 1023 element atomen
solid state element dichtheid
Atoomvolume natrium = 23,0 gram
0,97 g/cm3
Atoomvolume natrium = 23,71 cm3
De atomaire volumewaarde heeft niet alleen betrekking op de grootte van de atomen, maar ook op de afstand ertussen. Omdat het dus ook gaat om lege ruimtes, we kunnen niet neem de atomaire volumewaarde en deel deze door het aantal atomen (6.02. 1023) om het volume te vinden dat elk atoom inneemt.
Het is belangrijk om het atomaire volume te bestuderen omdat het een periodieke eigenschap is, dat wil zeggen, het varieert volgens het atoomnummer van het element. Kijk naar de afbeelding hieronder. Het atomaire volume van de elementen groeit van boven naar beneden, wat betekent dat wanneer we de elementen analyseren die tot dezelfde familie van het periodiek systeem behoren, naarmate het atoomnummer groeit, het atoomvolume ook toeneemt. Dit komt omdat, in die zin, de perioden toenemen, wat betekent dat de elektronische lagen van de atomen toenemen en bijgevolg ook het volume dat ze innemen. Dit is hetzelfde gevoel van groei als atoomstraal.
Aan de andere kant zien we horizontaal dat het atomaire volume neemt toe van het midden naar de randen. Wanneer we van links beginnen en rechts naar het midden van het periodiek systeem gaan, neemt het atomaire volume af omdat de periode hetzelfde, dat wil zeggen, de elementen van dezelfde lijn hebben hetzelfde aantal elektronische lagen, maar het atoomnummer zal toenemen. Dit betekent dat de hoeveelheid elektronen in deze richting toeneemt, wat resulteert in een grotere kracht van aantrekking van elektronen tot de kern van het atoom, waardoor de atoomstraal en bijgevolg het volume afneemt atomair. Maar vanuit het centrum naar rechts gebeurt dit niet verder, omdat, in het geval van elementen die zich in deze regio bevinden, vooral in het geval van niet-metalen is de afstand tussen hun atomen relatief groot, wat het atomaire volume beïnvloedt, het vergroten.
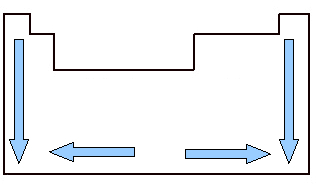
Variatie in atoomvolume in het periodiek systeem tussen families en perioden
Door Jennifer Fogaça
Afgestudeerd in scheikunde
Bron: Brazilië School - https://brasilescola.uol.com.br/quimica/volume-atomico.htm

