Als we het woord 'siliconen' horen, denken we meteen aan borstimplantaten die via plastische chirurgie zijn geplaatst. Siliconen is echter een materiaal dat verschillende doelen heeft, waaronder het gebruik in producten die we in ons dagelijks leven vaak consumeren.
Maar voordat u naar deze toepassingen kijkt, moet u kijken wat de chemische samenstelling van siliconen is en hoe het wordt geproduceerd.
O siliconen het is een condensatie polymeer, dat wil zeggen, hun lange moleculaire ketens worden gevormd door condensatiepolymerisatiereacties, waarbij de monomeren, wanneer ze verenigd zijn, water of een andere eenvoudige stof afgeven.
DE structuur basis van siliconen wordt hieronder weergegeven. Merk op dat we in plaats van koolstof (C) silicium (Si) als centraal element hebben, aangezien de hoofdketen van silicium bestaat uit siliciumatomen afgewisseld met zuurstofatoom. Dit is mogelijk omdat silicium tot dezelfde familie behoort, in het periodiek systeem, als koolstof, dat in de periode direct na koolstof komt. Daarom heeft silicium eigenschappen die vergelijkbaar zijn met die van koolstof en kan het daarom binden aan organische groepen (R).
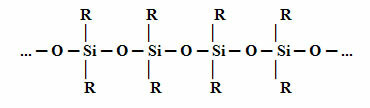
In het geval van siliconen zijn de meest gebruikte monomeren bij de productie ervan dichloordimethylsilaan of dichloordifenylsilaan. Deze monomeren worden verkregen door de reactie tussen silica, voornamelijk aanwezig in zand, met cokeskool, om eerst silicium te verkrijgen:
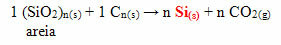
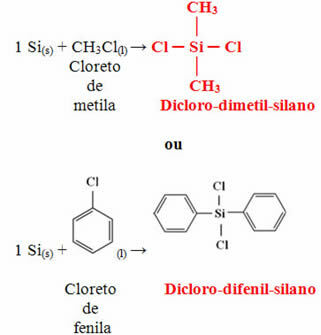
De volgende stap is om dit verkregen silicium te laten reageren met methylchloride of met fenylchloride om een van de twee bovengenoemde monomeren te vormen:
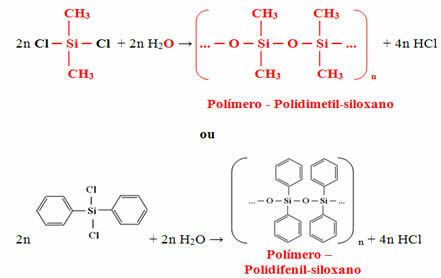
Het verkregen monomeer zal uiteindelijk reageren met water om het polymeer (siliconen) te vormen en zoutzuur als bijproduct af te geven:
Silicone is een zeer stabiel polymeer en heeft een grote weerstand tegen hitte, aangezien alleen de organische verbindingen die aan het silicone gebonden zijn, bij contact met warmte beginnen te ontbranden. Wanneer deze radicalen echter uitgereageerd zijn, blijft er alleen silica (zand) over, waardoor de verbranding niet doorgaat.
Omdat het deze eigenschappen heeft, is het niet giftig, heeft het een grote chemische inertie en presenteert het zich op manieren die verschillen van de extreem vloeibaar vloeibaar tot rubberachtig vast, deze polymeren worden gebruikt in de meest uiteenlopende gebieden. Hieronder vindt u enkele van deze toepassingen:

Door Jennifer Fogaça
Afgestudeerd in scheikunde
Bron: Brazilië School - https://brasilescola.uol.com.br/quimica/silicone-constituicao-aplicacoes.htm

