polymerisatie is de naam van het chemische proces dat resulteert in de vorming van macromoleculen (grote moleculen) genaamd polymeren, door de combinatie van kleinere moleculen, de monomeren.
de reactie van polymerisatie het komt veel voor in de natuur, zoals we kunnen zien in koolhydraten (zoals zetmeel) en eiwitten (zoals caseïne in melk). Het komt ook synthetisch voor, aangezien de overgrote meerderheid van de polymeren die door mensen in hun dagelijks leven worden gebruikt, kunstmatig worden gemaakt.
Het eerste polymeer geproduceerd uit polymerisatie synthetisch was bakeliet, in 1909, door de Belgische chemicus Leo Hendrik Baekeland.
In het algemeen, om een monomeer te combineren met een ander (ongeacht of ze hetzelfde of verschillend zijn) in een reactie van polymerisatie, is het noodzakelijk het bestaan van vrije valentie (chemische binding die moet worden uitgevoerd) in beide monomeren.
Deze valenties ontstaan als gevolg van het verbreken van bindingen, door het gebruik van katalysatoren (zoals nikkel), externe omstandigheden zoals licht en warmte, of door het fenomeen van resonantie in de structuur (verschuiving van elektronen).
Bij de vorming van polypropyleen (PP-polymeer), dat bijvoorbeeld wordt gebruikt in huishoudelijk gebruiksvoorwerpen en speelgoed, pi-link (π) in elk molecuul wordt als volgt onderverdeeld:
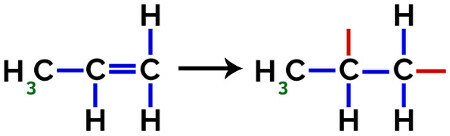
Breuk van pi-binding in propyleen
Zo kan elk propyleenmonomeer binden met twee andere propyleenmonomeren en het polymeer PP of polypropyleen vormen (het voorvoegsel poly geeft verschillende monomere eenheden aan). De meest voorkomende manier om een polymeer weer te geven, is het monomeer tussen haakjes en, aan de buitenkant, de letter n, die verschillende monomeren aangeeft, zoals we kunnen zien in het geval van het PP-polymeer:
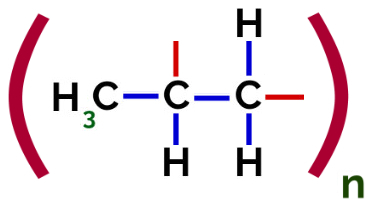
Vertegenwoordiging van PP-polymeer
de reactie van polymerisatie kan op verschillende manieren, zoals we hieronder zullen zien:
a) Reactie van additie polymerisatie
In deze polymerisatie, is er altijd een breuk van een pi-binding in het monomeer, waardoor twee vrije valenties in de structuur verschijnen, zoals bij de vorming van de polyethyleen, polymeer dat veel wordt gebruikt in farmaceutische verpakkingen.
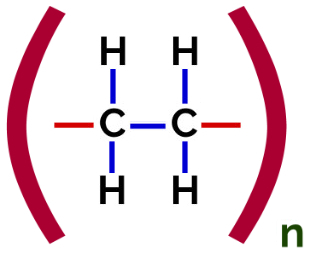
Polyethyleen Toevoeging Polymeer Structuurformule
Bij polymerisatie van polyethyleen, worden moleculen van ethyleen (etheen), die een pi-binding hebben tussen de twee koolstofatomen, als monomeer gebruikt. Wanneer deze binding wordt verbroken, verschijnen er twee vrije valenties, één op elk koolstofatoom dat betrokken was bij de pi-binding. De monomeren verenigen zich precies in elk van deze valenties, dat wil zeggen, de valentie van de ene is gekoppeld aan de valentie van de andere, enzovoort.
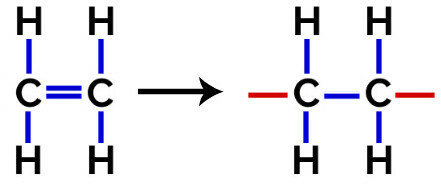
Polyethyleen vormingsvergelijking:
b) Toevoeging polymerisatiereactie 1.4
Bij deze polymerisatie vertonen de monomeren twee afwisselende dubbele bindingen (een pi en een sigma), wat het fenomeen bevordert van resonantie (afwisselen van de positie van de pi-elektronen van de pi-binding), zoals bij de vorming van synthetisch rubber (polybutadieen)

Structuurformule van polybutadieen
De monomere eenheid van dit polymeer is butadieen, dat twee afwisselende dubbele bindingen heeft. Bij resonantie heeft de structuur een dubbele binding tussen koolstof 2 en 3, en twee vrije valenties op koolstof 1 en 4. Het is precies in deze vrije valenties van koolstof 1 en 4 dat de monomeren combineren.

butadieen resonantie
c) Reactie van condensatie polymerisatie of eliminatie
Het is een reactie van polymerisatie waarin, verplicht, twee monomeren (dezelfde of verschillende) tegelijkertijd atomen of groepen verliezen, wat resulteert in twee vrije valenties in elk van hen. Op deze manier is er altijd de eliminatie van waterstof uit een monomeer, dat vervolgens samenkomt met een halogeen (F, Cl, Br, I), OH, NH2, of aan de CN van het andere monomeer.
Dus, in de polymerisatie door eliminatie is er altijd de vorming van water, gehalogeneerd zuur (HCl, HI, HF, HBr), ammoniak (NH3) of blauwzuur (HCN) naast het polymeer. Zie bijvoorbeeld de weergave van de vorming van polyester, een materiaal dat als stof wordt gebruikt:

Polyestervormingsvergelijking:
Polyestervormende monomeren zijn p-benzeendizuur en ethaan-1,2-diol. Dat kunnen we hierin zien polymerisatie de eliminatie van watermoleculen vindt plaats, omdat de twee monomeren twee hydroxylen hebben. In dit proces verliest het zuur de twee hydroxylen en de dialcohol verliest alleen de waterstof van zijn hydroxylen:

polyester structuur
Polyestermonomeren worden verbonden door de zuurstof in de alcohol en de koolstof in het carboxylzuur.
Door mij Diogo Lopes Dias
Bron: Brazilië School - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-polimerizacao.htm

