Sublimatie is de overgang van de vaste toestand naar de gasvormige toestand en vice versa, zonder door de vloeibare toestand te gaan.
Om een stof het sublimatieproces te laten ondergaan, moet deze worden onderworpen aan bepaalde waarden van temperatuur en druk.
Mottenballen en CO2 vast (droogijs) zijn voorbeelden van stoffen die onder omgevingsomstandigheden sublimatie ondergaan.

Fasen diagram
We kunnen de fysieke toestand van een stof ontdekken door de waarden van temperatuur en druk te kennen waaraan deze wordt onderworpen.
Hiervoor hebben we diagrammen gebruikt die voor elke stof zijn gemaakt, van experimenteel gevonden waarden.
genaamd "Fasen diagram", het is verdeeld in drie regio's die de vaste, vloeibare en gasvormige toestanden vertegenwoordigen. De lijnen die deze gebieden afbakenen, geven de punten aan waarop de stof van fase verandert.
Het tripelpunt in het diagram geeft de temperatuur en druk aan waarbij de stof in de drie fasen naast elkaar kan bestaan. Onder dit punt bevindt zich de sublimatiecurve.
De punten op deze curve bepalen de druk- en temperatuurwaarden waarbij sublimatie zal plaatsvinden.
Wanneer een vaste stof wordt onderworpen aan een druk lager dan het tripelpunt, zal deze bij verhitting direct in een gasvormige toestand overgaan.
De verandering van de directe vaste toestand naar de gasvormige toestand kan ook gebeuren door de druk te verlagen wanneer de temperatuur lager is dan die van het tripelpunt.
Meer informatie op: Veranderingen in fysieke toestand.
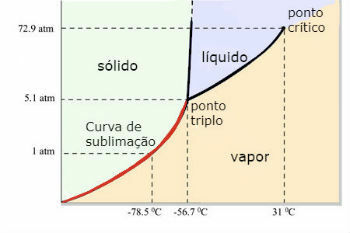
Kooldioxide (CO) Fasediagram2 )
Het CO-tripelpunt2 treedt op wanneer de druk 5 atm is. Dit feit rechtvaardigt dat het gebruikelijk is om het optreden van sublimatie in droogijs te zien, aangezien de omgevingsdruk 1 atmosfeer is.
Om deze reden wordt onder omgevingsomstandigheden geen vloeibaar kooldioxide verkregen. Onder deze omstandigheden bevindt het zich in vaste toestand of in dampvorm.
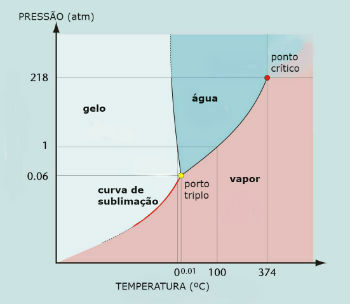
Waterfasediagram (H2O)
Het tripelpunt van water treedt op wanneer de druk slechts 0,06 atm is. Onder omgevingsomstandigheden is het dus niet gebruikelijk dat water sublimeert.
Lees voor meer informatie ook:
- Fysische toestanden van water
- Fysieke toestanden van materie
- Liquefactie of condensatie
- Eigenschappen van materie
- stollen
- Fusie
- Verdamping
- kokend
- Verdamping


