Het periodiek systeem is een manier om alle chemische elementen te ordenen op basis van hun eigenschappen en enige informatie over hen te tonen.
In het dagelijks leven is organisatie erg belangrijk om ons leven gemakkelijker te maken. Stel je bijvoorbeeld voor dat je kast rommelig is, met sokken vermengd met shirts en broeken. Het zou heel moeilijk zijn en het zou langer duren om een specifieke sok te vinden die je wilde dragen, nietwaar?! Maar als je je kledingkast ordent en al je sokken in één lade stopt, neem dan een lade. voor t-shirts, een andere voor korte broeken enzovoort, het zal veel gemakkelijker zijn om te vinden wat nodig hebben. En hoe meer kleding je bezit, hoe meer organisatie er nodig is.
Evenzo hebben wetenschappers in de loop van de tijd veel chemische elementen ontdekt. Om u een idee te geven, in 1850 waren er ongeveer 60 elementen bekend, maar vandaag weten we van het bestaan van 118. Zo ontstond de behoefte om deze chemische elementen zo te organiseren dat het gemakkelijker zou worden om hun eigenschappen te begrijpen. Dit is de rol van het periodiek systeem van de chemische elementen.
Het periodiek systeem dat we vandaag gebruiken, is gerangschikt in horizontale lijnen in oplopende volgorde van atoomnummer.
U moet het periodiek systeem raadplegen alsof u een normale tekst leest, dat wil zeggen dat u altijd begint met de eerste rij en van links naar rechts en gaat dan door naar de volgende lijnen.De chemische elementen werden in afzonderlijke vierkanten op het periodiek systeem geplaatst, waarbij het elementsymbool in de. staat de helft en de waarde van het atoomnummer wordt meestal bovenaan geschreven, zoals weergegeven in het onderstaande waterstofvoorbeeld:

Waterstofsymbool en het atoomnummer zoals weergegeven in het periodiek systeem
Het atoomnummer is de hoeveelheid protonen of positieve ladingen die de atomen van het element hebben. Deze waarde is gelijk aan het aantal elektronen wanneer het atoom zich in zijn grondtoestand bevindt.Waterstof is een element dat maar 1 proton heeft, dat wil zeggen dat het atoomnummer 1 is. Daarom is waterstof het eerste element dat in de tabel wordt geplaatst. Het volgende element dat op dezelfde lijn staat als waterstof is helium, omdat het een atoomnummer heeft dat gelijk is aan 2.
Als we naar de onderste rij gaan, is de eerste Lithium met een atoomnummer gelijk aan 3, ernaast zit beryllium met atoomnummer 4 enzovoort.Kijk naar de eerste regels van het periodiek systeem hieronder en zie dat de volgorde van het atoomnummer precies goed groeit.
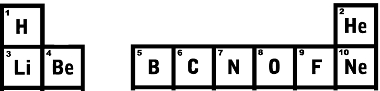
Eerste twee regels van het periodiek systeem
Er zijn zeven regels in het periodiek systeem en deze regels heten menstruatie. Kijken:

Periodieke Tabel Perioden
Er zijn 18 kolommen die worden genoemd gezinnen of groepen. Een belangrijk aspect is dat elementen die tot dezelfde familie behoren, zijn die met vergelijkbare fysische en chemische eigenschappen.

Periodieke Tabel Families of Groepen
Eens kijken of je het begrijpt? Vertel me welk scheikundig element behoort tot de 4e periode en familie 16?
Als je Se (selenium) zei, heb je gelijk! Vertel me nu wat zijn atoomnummer is. Dat klopt, het is 34.
In elk vierkantje dat het element ziet, staat ook andere belangrijke informatie, zoals de atoom massa en de elektronen die zich in elke elektronische laag van atomen bevinden. Zie bijvoorbeeld in de volgende afbeelding dat neon Ne als symbool heeft, het atoomnummer is gelijk aan 10, de atoommassa is gelijk aan 20.1797 u en zijn elektronen zijn als volgt verdeeld in hun lagen: 2 - 8, dat wil zeggen, in de laag die zich het dichtst bij de kern bevindt, zijn er twee elektronen en in de verste zijn er acht elektronen.

Neonsymbool op het periodiek systeem en zijn atoom
Let nu op twee interessante aspecten: (1) de neon heeft alleen twee banen of lagen waar je elektronen zijn, daarom hij bezet de 2e periode (2e regel);en (2) hij heeft acht elektronen op de laatste laag, daarom heeft hij is familie 18.
Dit laat ons het volgende zien:
* De elementen die zich in dezelfde periode van het periodiek systeem bevinden, hebben hetzelfde aantal elektronische lagen en kunnen er maximaal zeven hebben;
* Chemische elementen die in het periodiek systeem tot dezelfde familie behoren, hebben hetzelfde aantal elektronen in de laatste elektronenschil:
*Familie 1: alles hebben 1 elektron in de laatste elektronische laag;
*Familie 2: alles hebben 2 elektronen in de laatste elektronische laag;
*Familie 13: alles hebben 3 elektronen in de laatste elektronische laag;
*Familie 14: alles hebben 4 elektronen in de laatste elektronische laag;
*Familie 15: alles hebben 5 elektronen in de laatste elektronische laag;
*Familie 16: alles hebben 6 elektronen in de laatste elektronische laag;
*Familie 17: alles hebben 7 elektronen in de laatste elektronische laag;
*Gezin 18: alles hebben 8 elektronen in de laatste elektronische laag.
Sommige groepen of families in het periodiek systeem krijgen specifieke namen, zie enkele:
Familie 1: Alkalimetalen;
Familie 2: Aardalkalimetalen;
Familie 16: Chalcogenen;
Familie 17: Halogenen;
Familie 18: Edele gassen.

Organisatie van periodieke tabelfamilies
Laten we nogmaals uw kennis testen. Beantwoord de volgende vragen door het periodiek systeem te raadplegen:
1- Wat is de naam van de chloorfamilie?
2- Wat is het atoomnummer en de atoommassa?
3- Hoeveel elektronische lagen heeft een chlooratoom?
4- Hoeveel elektronen heeft een chlooratoom in zijn laatste elektronenschil?
antwoorden:
1- Halogenen (familie 17).
2- Het atoomnummer van chloor is 17 en de atoommassa is gelijk aan 35,45 u.
3- Een chlooratoom heeft drie elektronische lagen omdat het tot de 3e periode van de tabel behoort.
4- Een chlooratoom heeft zeven elektronen in de valentieschil omdat het tot familie 17 behoort.
Er is nog andere belangrijke informatie die het Periodiek Systeem ons geeft en waar we het in latere teksten beter over zullen hebben. Maar degenen die hier worden besproken, zijn de belangrijkste voor u om te beginnen te begrijpen hoe de elementen erin zijn georganiseerd. Onthoud dat een tafel niet gemaakt is om te decoreren, maar je moet hem goed kennen om er indien nodig naar te kunnen verwijzen.
Door Jennifer Fogaça
Afgestudeerd in scheikunde
Maak van de gelegenheid gebruik om onze videolessen over het onderwerp te bekijken: