een substitutie reactie het is gebaseerd op de uitwisseling tussen componenten van twee verschillende reagentia. Verbindingen met een grotere stabiliteit (verzadigd, dat wil zeggen, met alleen eenvoudige bindingen tussen koolstoffen) zullen dit proces eerder ondergaan. Benzeen kan het echter ook.
We weten dat in de structuur van de benzeen er zijn drie dubbele bindingen (drie pi-bindingen), dat wil zeggen, deze verbinding is onverzadigd, maar deze dubbele bindingen ondergaan de hele tijd het fenomeen van resonantie (afwisseling van positie van de drie pi-bindingen). Om deze reden heeft de structuur een grotere stabiliteit, omdat de bindingen door alle koolstoffen gaan.
De substitutiereacties die kunnen optreden in benzeen zijn:
Halogenering;
nitratie;
sulfonering;
alkylering;
Acylering.
a) Halogenering
In deze reactie interageert benzeen met halogenen (Br2, Cl2 Hallo2), altijd met de aanwezigheid van een katalysator, die een anorganisch zout kan zijn (AlCl3, FeCl3 en februari3). Het proces vindt plaats met de uitwisseling van een benzeenwaterstof voor een halogeenatoom. Het resultaat is de
vorming van een organisch halide en een gehalogeneerd hydride. Zie een voorbeeld: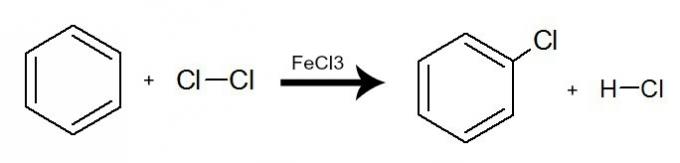
Vergelijking die een halogenering van benzeen weergeeft door het gebruik van moleculair chloor (Cl2)
b) Nitratie
Bij deze reactie interageert benzeen met salpeterzuur (HNO3), altijd met de aanwezigheid van de zwavelzuurkatalysator (H2ENKEL EN ALLEEN4) en verwarming. Het proces vindt plaats met de uitwisseling van waterstof uit benzeen voor de NO-groep2 van het zuur. Het resultaat is de vorming van a nitroverbinding en water.
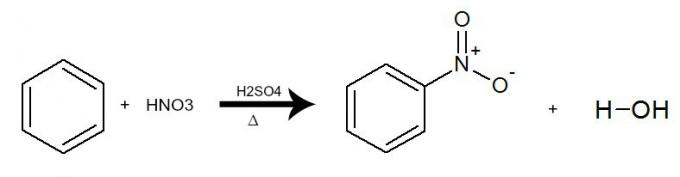
Vergelijking die de nitrering van benzeen weergeeft door het gebruik van salpeterzuur
c) Sulphonation
Bij deze reactie interageert benzeen met zwavelzuur (H2ENKEL EN ALLEEN4), altijd met de aanwezigheid van de zwaveltrioxidekatalysator (SO3) en verwarming. Het proces vindt plaats met de uitwisseling van waterstof uit benzeen door de SO-groep3H van zuur. Het resultaat is de vorming van zuur sulfonzuur en water.
Niet stoppen nu... Er is meer na de reclame ;)
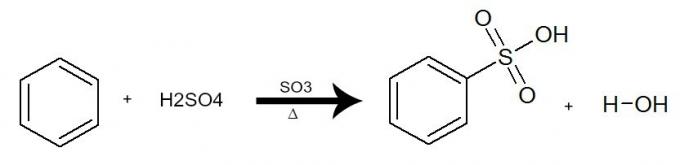
Vergelijking die een sulfonering van benzeen weergeeft met behulp van zwavelzuur
d) Alkylering
In deze reactie interageert benzeen met a organisch halide (R-X), altijd met de aanwezigheid van de katalysator aluminiumtrichloride (AlCl3) en verwarming. Het proces vindt plaats met de uitwisseling van een waterstof uit benzeen door de R-groep (organische substituent) van het halogenide. Het resultaat is de vorming van een vertakte aromatische koolwaterstofen een anorganisch zuur (HX).
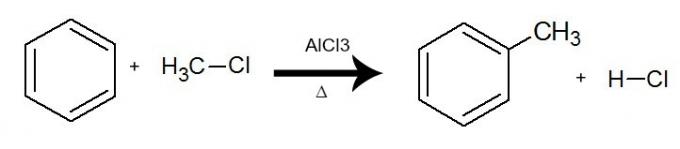
Vergelijking die een alkylering van benzeen weergeeft met behulp van chloormethaan
e) Acylatie
In deze reactie interageert benzeen met een zuurhalogenide, dat kan worden weergegeven door ethanoylchloride:
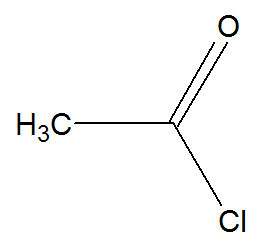
Structuurformule van ethanoylchloride
De reactie gebeurt met de aanwezigheid van de katalysator aluminiumtrichloride (AlCl3) en er is een uitwisseling van één waterstof uit benzeen voor de gehele zuurhalogenidegroep (met uitzondering van X-halogeen). Het resultaat is de vorming van a keton en een anorganisch zuur (HX). Zie een voorbeeld:
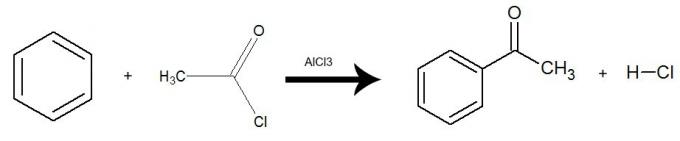
Vergelijking die een acylering van benzeen weergeeft met behulp van ethanoylchloride
Door mij Diogo Lopes Dias
Wil je naar deze tekst verwijzen in een school- of academisch werk? Kijken:
DAGEN, Diogo Lopes. "Substitutiereacties in benzeen"; Brazilië School. Beschikbaar in: https://brasilescola.uol.com.br/quimica/reacoes-substituicao-no-benzeno.htm. Betreden op 27 juni 2021.
Chemie

Aromatische verbindingen, arenen, polariteit, onoplosbare, oplosbare, niet-polaire oplosmiddelen, ether, tetrachloorkoolstof, koolwaterstoffen, insecticiden, kleurstoffen, oplosmiddelen, explosieven, kankerverwekkende stoffen, tolueen, methylbenzeen, medicijnen, lijm schoenmaker.
Chemie

Klik hier en leer meer over substitutiereactie, een chemisch proces waarbij de gebruikte reagentia (organische en anorganische) een van de componenten met elkaar uitwisselen, waardoor nieuwe stoffen worden gevormd. Tot de stoffen die het meest worden gebruikt als reagentia behoren alkanen, benzeen en organische halogeniden.


