Er is een tak van wetenschap die de snelheid van chemische reacties bestudeert en de factoren die daarop van invloed zijn, het heet Chemical Kinetics. Chemische reacties kunnen worden gedefinieerd als een reeks verschijnselen waarbij twee of meer stoffen met elkaar reageren, waardoor verschillende verbindingen ontstaan. Een chemische vergelijking is een grafische weergave van een chemische reactie, waarbij reactanten in het eerste lid voorkomen en producten in het tweede lid.
A + B  C + D
C + D
Reagentia Producten
De kennis en studie van reacties zijn niet alleen in industrieel opzicht van groot belang, maar ook gerelateerd aan ons dagelijks leven.
De snelheid van een reactie is hoe snel reactanten worden verbruikt of hoe snel producten worden gevormd. Het branden van een kaars en de vorming van roest zijn voorbeelden van langzame reacties. In dynamiet is de ontleding van nitroglycerine een snelle reactie.
De snelheden van chemische reacties worden bepaald door middel van empirische wetten, de zogenaamde wetten van snelheid, afgeleid van het effect van de concentratie van reactanten en producten op de snelheid van reactie.
Chemische reacties vinden plaats met verschillende snelheden en deze kunnen worden gewijzigd, omdat naast: concentratie van reactanten en producten, reactiesnelheden zijn ook afhankelijk van andere factoren Leuk vinden:
Reagensconcentratie:: hoe hoger de concentratie van de reactanten, hoe sneller de reactie zal verlopen. Om een reactie tussen twee of meer stoffen te laten plaatsvinden, is het nodig dat de moleculen botsen, zodat de bindingen worden verbroken met als gevolg de vorming van nieuwe. Het aantal botsingen hangt af van de concentraties van A en B. Zie de foto:
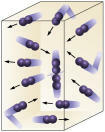
Moleculen botsen vaker als
we verhogen het aantal reagerende moleculen.
Niet stoppen nu... Er is meer na de reclame ;)
Het is gemakkelijk te zien dat door een hogere concentratie er een toename van botsingen tussen moleculen zal zijn.
contactoppervlak: een toename van het contactoppervlak verhoogt de reactiesnelheid. Een voorbeeld is wanneer we een gebroken sonrisal-tablet oplossen en het sneller oplost dan als het geheel zou zijn, gebeurt dit omdat we het contactoppervlak vergroten dat reageert met de Water.
Druk: wanneer je de druk van een gasvormig systeem verhoogt, neemt de reactiesnelheid toe.
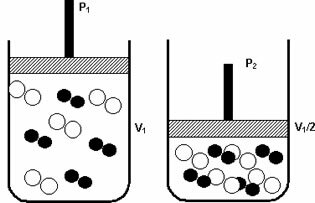
Een verhoging van de druk van P1 naar P2 verminderde het volume van V1 naar V1/2, waardoor de reactie versnelde door de nadering van de moleculen.
De bovenstaande figuur illustreert dat, net als bij de afname van het volume in de tweede container, er een toename zal zijn in de druk die de botsingen van de moleculen intensiveert en als gevolg daarvan een toename van de snelheid van de reactie.
Temperatuur: wanneer de temperatuur van een systeem wordt verhoogd, is er ook een toename van de reactiesnelheid. Het verhogen van de temperatuur betekent het verhogen van de kinetische energie van moleculen. In onze dagelijkse praktijk kunnen we deze factor waarnemen tijdens het koken en we verhogen de vlam van het fornuis zodat het voedsel sneller de kookgraad bereikt.
Katalysatoren: Katalysatoren zijn stoffen die het mechanisme versnellen zonder permanent te worden gewijzigd, dat wil zeggen dat ze tijdens de reactie niet worden verbruikt. Katalysatoren zorgen ervoor dat de reactie een alternatief pad volgt, waarvoor minder activeringsenergie nodig is, waardoor de reactie sneller verloopt. Het is belangrijk om te onthouden dat een katalysator de reactie versnelt, maar de opbrengst niet verhoogt, dat wil zeggen dat hij dezelfde hoeveelheid product produceert, maar in een kortere tijd.
Door Liria Alves
Afgestudeerd in scheikunde
Wil je naar deze tekst verwijzen in een school- of academisch werk? Kijken:
SOUZA, Liria Alves de. "Chemische kinetica"; Brazilië School. Beschikbaar in: https://brasilescola.uol.com.br/quimica/cinetica-quimica.htm. Betreden op 27 juni 2021.

