Vladimirs Vasiļjevičs Markovņikovs (1838-1904) bija Maskavas ķīmiķis, kurš 1869. gadā sāka pētīt dažas reakcijas, kā halogēnūdeņražus pievienot alkēniem un alkīniem.
Šajās reakcijās alkēns reaģē ar halogēnūdeņraža atomu vai halogēnūdeņražskābi, piemēram, ūdeņraža hlorīdu (HCl), bromūdeņraža atomu (HBr) un ūdeņraža jodīdu (HI). Produkts, kas veidojas no alkēna, ir alkilhalogenīds, jo ūdeņradis saistās ar vienu no pāra ogļiem un halogēna savienojums ar otru. Skatiet piemēru zemāk:
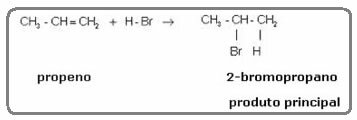
Kaut kas līdzīgs notiek arī alkēnu hidratācijas reakcijā skābā vidē; kurā iegūtais produkts ir spirts:
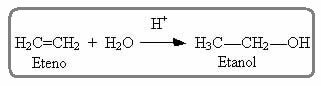
Iepriekš minētā etilēna molekula ir simetriska; tāpēc nav svarīgi, kuram ogleklim attiecīgi tiks pievienots ūdeņradis un halogēns. Tomēr asimetriskās molekulās, piemēram, propēnā, varētu sagaidīt divu iespējamo produktu veidošanos. Tomēr Markovņikovs redzēja, ka tas nenotika praksē. Lai saprastu, apskatiet zemāk redzamo reakciju:
Nepārtrauciet tūlīt... Pēc reklāmas ir vēl vairāk;)
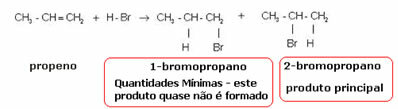
Praktiski viens pats izveidojies produkts ir 2-brompropāns. Un Markovņikovs redzēja, ka tas attiecas arī uz citām vielām. Tāpēc viņš formulēja šādu noteikumu:

Tas pats attiecas uz ūdens pievienošanu. Tā kā gan ūdens molekula, gan halogēnūdeņraži ir polāri, šo molekulu ūdeņradis iegūst elektropozitīvu raksturu.
Hδ+_ X δ- un Hδ+_ ak δ-
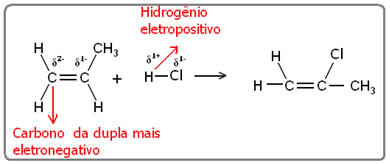
Būdams elektropozitīvs, ūdeņradis saistīsies ar visvairāk elektronegatīvo oglekli, kas būs saistīts ar vislielāko ūdeņraža daudzumu. Tātad mums ir:
Autore Jennifer Fogaça
Beidzis ķīmiju
Brazīlijas skolu komanda
Vai vēlaties atsaukties uz šo tekstu skolas vai akadēmiskajā darbā? Skaties:
FOGAÇA, Jennifer Rocha Vargas. "Markovņikova likums"; Brazīlijas skola. Pieejams: https://brasilescola.uol.com.br/quimica/regra-markovnikov.htm. Piekļuve 2021. gada 28. jūnijam.