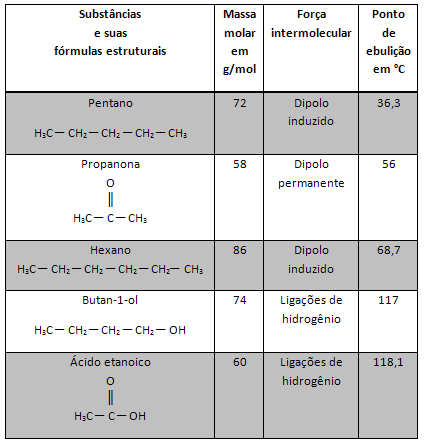
O pH šķīduma norāda hidronija jonu (H3O+) atrodas vidū. Šis saturs nosaka, vai analizētajam šķīdumam ir skāba, bāziska vai neitrāla īpašība.
Novērošana: Jāatzīmē, ka hidronija saturs (H3O+ vai H+) var iegūt vienkārši laboratorijā, izmantojot pH indikatora lentes - kurām tomēr nav lielas precizitātes mērījumā - vai ar aprīkojumu, ko sauc par peagometru, kuram, gluži pretēji, ir liela precizitāte, mērot pH risinājums.
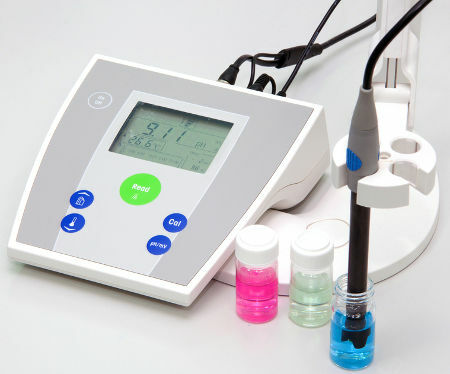
Pedometrs vai potenciometrs šķīduma pH mērīšanai
Lai veiktu aprēķini, kas saistīti ar pH risinājuma, mēs varam izmantot šādu logaritmisko vienādojumu:
pH = - log [H3O+]
vai
pH = - log [H+]
SVARĪGS: Aprēķinos, kas saistīti ar šķīduma pH, mēs vienmēr izmantojam bāzes 10 logaritmu.
Prāta karte: Risinājumu PH aprēķināšana

* Lai lejupielādētu domu karti PDF formātā, Noklikšķiniet šeit!
No iepriekš minētā logaritmiskā vienādojuma mēs joprojām varam izmantot šo vienādojumu ar šādu vienkāršojumu (kas iegūts, pielietojot logaritmisko funkciju):
[H3O+] = 10-H
Novērošana: Iepriekš minēto vienkāršoto izteicienu var izmantot tikai tad, ja pH vērtība ir vesels skaitlis; pretējā gadījumā jāizmanto logaritmiskā funkcija.
Ir svarīgi uzsvērt, ka aprēķini, kas saistīti ar šķīduma pH, vienmēr ir saistīti ar pOH (hidroksiljonu potenciāls / OH-), jo abas spējas balstās uz ūdens pašjonizāciju (K.w = 10-14, parādība, kurā ūdens rada tik daudz H+ cik ak-) un Ostvalda atšķaidīšanas likums (jo vairāk atšķaidīts šķīdums, jo lielāks ir H katijonu daudzums+ ). Tādējādi:
par ūdens autoionizācija:
Kw = [H+]. [ak-], tātad pH + pOH = 14
likums Ostvalda atšķaidīšana(Caur to mēs varam zināt, cik daudz konkrēts materiāls ūdenī jonizējas vai disociējas):
Ki = M.α2
Ki = vielas jonizācijas konstante ūdens vidē;
M = vielas molaritāte vai molārā koncentrācija ūdens vidē;
α2 = materiāla jonizācijas vai disociācijas pakāpe barotnē.
Šķīduma klasificēšanai par skābu, bāzi vai neitrālu būs šādi kritēriji (25 OÇ):
-
viens risinājums būs neitrāls kad H koncentrācija+ ir vienāds ar OH koncentrāciju- vai pH ir 7.
Nepārtrauciet tūlīt... Pēc reklāmas ir vairāk;)
[H+] = [OH-]
viens šķīdums būs skābs kad H koncentrācija+ ir lielāka par OH koncentrāciju- vai pH ir no 0 līdz 7.
[H+]> [OH-]
viens risinājums būs pamata kad H koncentrācija+ ir mazāka par OH koncentrāciju- vai pH ir starp 7 un 14.
[H+] -]
Skatiet dažus aprēķinu piemērus, kas saistīti ar šķīdumu pH:
1º)Zinot, ka hidronija koncentrācija kafijā ir vienāda ar 1,10-5, kāds būs pH līmenis šajā šķīdumā?
kā vingrot nodrošināja hidronija koncentrāciju pēc kafijas mēs varam izmantojiet vienkāršoto pH formulu:
[H3O+] = 10-H
1.10-5 = 10-H
10-5 = 10-H
-5 = -pH
pH = 5
Tā kā pH ir mazāks par 7, šķīdums ir skābs.
2º) (NLO) Kāds ir 0,045 mol / L etiķskābes šķīduma pH, pieņemot, ka tā Ki = 1,.10-5? Dati: log 2 = 0,3; log 3 = 0,48.
Vingrinājumu dati:
M = 0,045 mol / l
Ki = 1,8.10-5
log 2 = 0,3
log 3 = 0,48
Kā vingrinājums nodrošināja molaritāte (M) un jonizācijas konstante (Ki),sākumā noteiksim minētās skābes jonizācijas pakāpi, jo hidronija (H3O+ vai H+) vienmēr ir molārā un jonizācijas pakāpes reizināšanas rezultāts. Drīz:
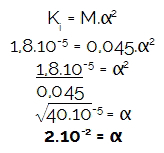
Tālāk aprēķināsim hidronija daudzums, reizinot molaritāti skābes pēc konstatētās jonizācijas pakāpes:
[H3O+] = M.α
[H3O+] = 0,045.2.10-2
[H3O+] = 0,09.10-4
[H3O+] = 9.10-4 mol / L
Visbeidzot, mēs ieliekam hidronija koncentrācijas vērtība logaritmiskajā pH vienādojumā:
pH = - log [H3O+]
pH = - log 9.10-4
pH = 4 - log 9
pH = 4-log 32
pH = 4 - 2. (3. žurnāls)
pH = 4 (2,0,48)
pH = 4-0,96
pH = 3,04
Tā kā pH ir mazāks par 7, šķīdums ir skābs.
3º)(Cefet-PR) A 45 OC, neitrāla šķīduma Kw ir vienāds ar 4,10-4. Tātad, kāda ir šī šķīduma pH vērtība šajā temperatūrā? 2. žurnāla dati = 0,3.
Kā vingrinājums stāsta risinājumu neitrāls, drīz [H3O+] ir vienāds ar [OH-]:

Visbeidzot, mēs ieliekam hidronija koncentrācijas vērtība logaritmiskajā pH vienādojumā:
pH = - log [H+]
pH = - log 2,10-7
pH = 7 - log 2
pH = 7-0,3
pH = 6,7
Tā kā pH ir gandrīz 7, šķīdums ir neitrāls (kā norādīts vingrinājuma paziņojumā), jo temperatūra ir 45 ° C OÇ.
Autors: Diogo Lopes Dias
Vai vēlaties atsaukties uz šo tekstu skolas vai akadēmiskajā darbā? Skaties:
DIENAS, Diogo Lopes. "Aprēķini ar šķīdumu pH līmeni"; Brazīlijas skola. Pieejams: https://brasilescola.uol.com.br/quimica/calculos-envolvendo-ph-solucoes.htm. Piekļuve 2021. gada 28. jūnijam.
Ostvalda likums, jonizācijas konstante, molārā koncentrācija, jonizācijas pakāpe, vājš elektrolīts, jonizēto molu skaits, Frīdrihs Vilhelms Ostvalds, monoskābes, monobāzes.