Oglekļa atoms ir četrvērtīgs, tas ir, tas spēj izveidot četras kovalentās saites, kas var būt vienas, divkāršas vai trīskāršas. Turklāt šīs saites var rasties ar citiem oglekļa atomiem vai citu ķīmisko elementu atomiem. Pateicoties šim īpašumam, ogleklim ir unikāla jauda, kas turpina veidot šos savienojumus un veidot īsas vai garas ķēdes.
Tiek saukts šis kopā savienoto ogļu un heteroatomu kopums, kas veido organisko molekulu "skeletu" oglekļa ķēdes.
Tā kā ogleklis spēj veidot ļoti lielu skaitu savienojumu, tos klasificēja pēc dažas tās ķēžu pazīmes, lai atvieglotu viņu izpēti un lai mēs labāk izprastu tās īpašības.
Šo savienojumu galvenā klasifikācija ir:
1. Atvērtas vai acikliskās ķēdes: Vai tie ir divi vai vairāk brīvi. Atomu ķēde netiek slēgta. Skatiet dažus piemērus:
H3Ç? CH2? CH2? CH3 H3Ç? CH? CH? CH3 H3Ç? CH? CH3
?
CH3
2. Slēgtas ķēdes: Tie ir tie, kuriem nav brīvu galu, jo atomi savienojas kopā, veidojot gredzenu vai ciklu. Piemēri:

Slēgtu oglekļa ķēžu piemēri
Novērojums: Tiek sauktas arī atvērtas un slēgtas ķēdes, kurām nav aromātiska gredzena (apakšējā rindas pirmā struktūra augšējā attēlā)
alicikliskas vielas.3. Jauktas ķēdes: Tie ir tie, kuriem ir vismaz viens brīvais gals un cikls, tas ir, viņiem ir vismaz viena atvērta un viena slēgta daļa. Piemēri:
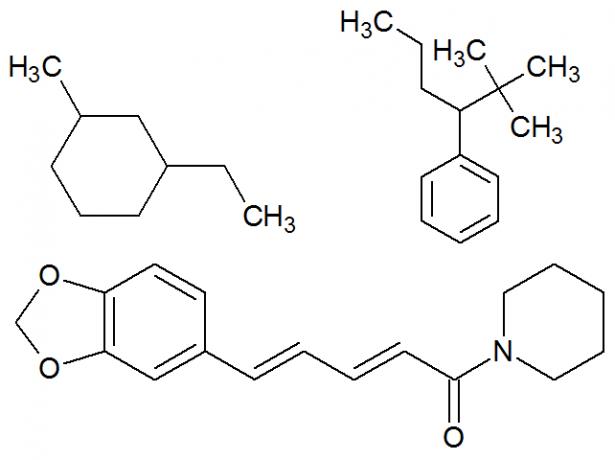
Jauktu oglekļa ķēžu piemēri
Šīs trīs galvenās grupas klasificē arī pēc citām apakšnodaļām, kā parādīts zemāk redzamajā diagrammā:
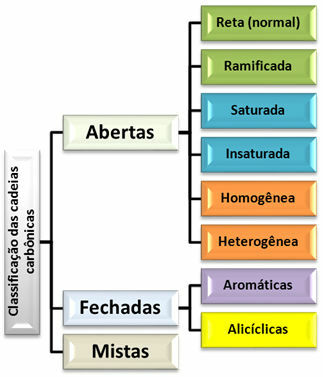
Oglekļa ķēžu klasifikācijas shēma
Ja vēlaties uzzināt vairāk par katru no šīm klasifikācijām, izlasiet tekstu Oglekļa ķēžu klasifikācijasadaļā Organiskā ķīmija.
Autore Jennifer Fogaça
Beidzis ķīmiju
Avots: Brazīlijas skola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-classificacao-das-cadeias-carbonicas.htm


