Iekš pievienošanas reakcijasiekšā alkēni(ogļūdeņraži, kuriem ir divkārša saite starp diviem oglekļa atomiem), starp diviem ogļiem tiek pārtraukta pi saite un katrs no ogļiem pievienojas jaunam atomam. Skaties:
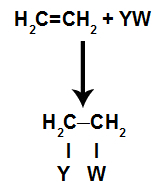
Pievienošanas reakcijas vispārējais shematiskais modelis
Pievienošanas reakcijas principi
a) pi saites pārrāvums
Pī saite ir viegli sadalāma, jo tā ir vājāka saite nekā sigmas saite. Tomēr, lai tas notiktu, ir nepieciešams, lai alkēns būtu pakļauts apstākļiem, kas nodrošina šo pārtraukumu. Pēc pi saites pārtraukšanas starp diviem oglekļiem pie katra iesaistītā oglekļa vienmēr parādās saistīšanās vieta (jauniem atomiem).
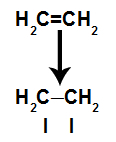
Shematisks attēlojums pi saites pārrāvumam
b) Pi saites pārtraukšanas nosacījumi
Faktori, kas veicina pi saites pārtraukšanu, ir:
Katalizatoru izmantošana;
Apkure;
Skābes klātbūtne reakcijas vidē.
c) Pievienošanās reakcijas rašanās
Saistīšanās vietas, kas izveidotas pēc pi-saites pārtraukšanas, vienmēr aizņem reaģenta atomi, kas atrodas tajā pašā traukā kā alkēns. Pievienošanas reakcija ir nosaukta pēc reaģenta veida, kas sajaukts ar alkēnu.
Pievienošanas reakciju veidi alkēnos
a) Hidrogenēšana
Alkēnu sajauc ar ūdeņraža gāzi (H2) traukā un pakļauts cieta katalizatora (niķeļa, platīna vai palādija) iedarbībai un karsēšanai (Δ).
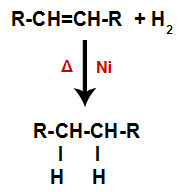
Alkēnu hidrogenēšanas reakcijas vispārējā shēma
Katalizatora klātbūtne un karsēšana izraisa alkēna pi saiti un sigma saiti starp H ūdeņražiem2 ātrāk salauzt. Līdz ar to mums ir izveidotas divas saistīšanās vietas alkēnā un divi brīvie ūdeņraža atomi reakcijas vidē.

Atomu saistīšanās un atdalīšanas vietu izveide
Tādējādi tūlīt pēc tam katrs brīvais ūdeņraža atoms aizņem vienu no saistīšanās vietām, kas izveidojušās alkēnā. Tā kā izveidotajā vielā ir tikai ogļūdeņraži un ūdeņraži, kā arī starp ogļiem ir tikai vienkāršas saites, tas ir a alkāns.
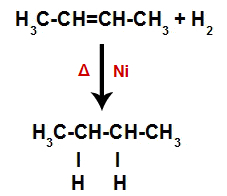
Vienādojums, kas attēlo alkāna veidošanos hidrogenēšanā
B) Halogenēšana
Alkēnu sajauc ar vienkāršām vielām (F2, Cl2, br2 Hei2) veidoja halogēni (hlors, fluors, jods un broms) traukā un pakļauti gaismas (λ) un karsēšanas (Δ) iedarbībai.

Alkēnu halogenēšanas reakcijas vispārējā shēma
Gaismas un karsēšanas ietekmē alkēna pi saite un sigmas saite starp vielām, kuras veido halogēns, tiek ātrāk sadalīti. Līdz ar to mums ir izveidotas divas saistīšanās vietas alkēnā un divi brīvie halogēna atomi reakcijas vidē.

Atomu saistīšanās un atdalīšanas vietu izveide
Tādējādi tūlīt pēc tam katrs brīvais halogēna atoms aizņem vienu no saistīšanās vietām, kas izveidojušās alkēnā. Tā kā izveidotajai vielai ir halogēns, kas saistīts ar struktūru, kas sastāv no oglekļiem un ūdeņražiem, tā ir a organiskais halogenīds.

Vienādojums, kas attēlo organisko halogenīdu veidošanos halogenēšanā
c) Hidratācija
Alkēnu sajauc ar ūdeni (H2O) traukā un pakļauts katalizatora (šajā gadījumā sērskābes) iedarbībai.
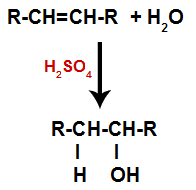
Alkēnu hidrēšanas reakcijas vispārējā shēma
Sērskābes klātbūtne reakcijā padara alkēna pi saiti un sigmas saiti starp ūdeņraža (H) un hidroksilgrupas (OH) ātrāku pārtraukumu. Līdz ar to mums ir izveidotas divas saistīšanās vietas alkēnā un viens brīvais ūdeņradis un viens hidroksils reakcijas vidē.
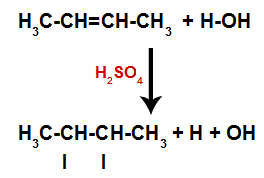
Atomu saistīšanās un atdalīšanas vietu izveide
Tādējādi neilgi pēc tam ūdeņradis un hidroksilgrupa aizņem vienu no alkēnā izveidotajām saites vietām. Tā kā izveidojušās vielas hidroksilgrupa ir saistīta ar piesātinātu oglekli (tā veido tikai vienkāršas saites), tas ir alkohols.
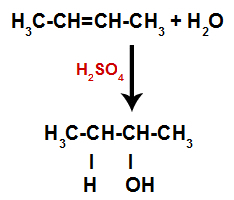
Vienādojums, kas attēlo spirta veidošanos hidratācijā
d) Pievienošana ar halogēnūdeņražiem
Alkēnu traukā sajauc ar halogenētu neorganisko skābi (HF, HI, HCl, HBr).

Skābes halogenīda reakcijas vispārējā shēma alkēnos
Skābes klātbūtne reakcijā izraisa alkēna pi saites ātrāku pārtraukumu. Viena saite skābē ir sadalīta, jo šīs vielas dabiski jonizējas. Tādējādi alkēnā tiek izveidotas divas saistīšanās vietas, un reakcijas vidē ir brīvs ūdeņradis un halogēns.
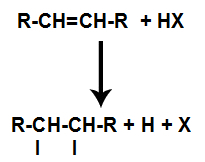
Atomu saistīšanās un atdalīšanas vietu izveide
Tādējādi neilgi pēc tam ūdeņradis un halogēns aizņem vienu no alkēnā izveidotajām saitēm. Tā kā izveidotajai vielai ir halogēns, kas saistīts ar struktūru, kas sastāv no oglekļiem un ūdeņražiem, tas ir organiskais halogenīds.
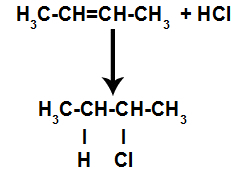
Vienādojums, kas attēlo organisko halogenīdu veidošanos halogenēšanā
Autors: Diogo Lopes Dias
Avots: Brazīlijas skola - https://brasilescola.uol.com.br/quimica/reacoes-adicao-alcenos.htm
