ģeometriskais izomērs ir sava veida kosmosa izomērija kas novērtē un salīdzina ķēdē esošo divu oglekļa atomu ligandu stāvokli telpā. Šis novērtējums tiek veikts, iedomājoties plakni starp iesaistītajiem ogļiem.
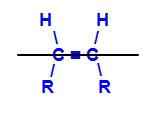
Iedomāta plakne, kas dala molekulu
Iedomātā plakne augšējā struktūrā sadala molekulu augšējā un apakšējā plaknē. Ar to mēs varam novērtēt un salīdzināt oglekļa ligandus, kas iesaistīti katrā no šīm plaknēm. Skatiet ģeometrisko izomēru tipus:
→ Cis-trans ģeometriskais izomērs
Savienojumam ir cis-trans ģeometriskais izomērijs kad ķēde parāda:
Atvērt ķēdi ar dubultu saiti starp diviem oglekļiem, kuriem ir vienādas saites viena ar otru. Skatiet piemēru:
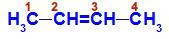
But-2-ene strukturālā formula
Struktūrā mēs varam novērot, ka gan oglekļa 2, gan oglekļa 3 ligandas ir vienādas, kas ir ūdeņradis (H) un metilgrupa (CH3).
Slēgta ķēde ar diviem ogļiem, kuriem ir vienādi ligandi viens otram. Skatiet piemēru:
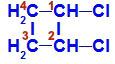
1,2-dihlorciklobutāna strukturālā formula
Struktūrā mēs varam novērot, ka gan ogleklim 1, gan ogleklim 2 ir vienādi ligandi, kas ir ūdeņradis (H) un hlors (Cl).
Lai izskaidrotu cis-trans izomerismu, mēs izmantosim but-2-enu:
a) Cis izomērs: ir ģeometriskais izomērs, kurā vieni un tie paši ligandi aizņem vienu un to pašu plakni. Zemāk redzamajā piemērā ūdeņraži atrodas vienā plaknē, tāpat kā metilgrupas.

Cis-but-2-ene strukturālā formula
b) transizomērs: ir ģeometriskais izomērs, kurā dažādi ligandi aizņem vienu un to pašu plakni. Tālāk sniegtajā piemērā mums vienā un tajā pašā plaknē ir ūdeņradis un metilgrupa (CH3).
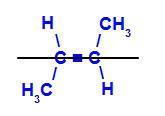
Trans-but-2-ene strukturālā formula
→ E-Z ģeometriskais izomērs
Savienojumam ir E-Z ģeometriskais izomērijs, ja ķēdei ir:
Atvērta ķēde ar dubultu saiti starp diviem ogļiem, kuriem ir visas vai dažas atšķirīgas saites. Skatiet piemēru:
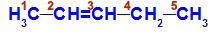
Pent-2-ene strukturālā formula
Struktūrā mēs varam redzēt, ka ogleklim 2 ir metilligands (CH3) un ūdeņradim (H), un ogleklim 3 ir ūdeņraža (H) un etilgrupa (H) ligands3C-CH2).
Slēgta ķēde ar diviem ogļiem, kuriem visi vai daži ligandi atšķiras viens no otra. Skatiet piemēru:
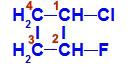
1-hlor-2-fluor-ciklobutāna strukturālā formula
Struktūrā mēs varam novērot, ka ogleklim 1 ir ūdeņradis un hlors kā galvenie ligandi, un ogleklim 2 ir ūdeņradis un fluors kā galvenie ligandi.
PIEZĪME: Starp dažādiem ligandiem ģeometriskā izomērijā mēs novērtējam liganda sarežģītību (atomu skaitu) vai atomu skaitu.
Lai izskaidrotu E-Z izomēru, mēs izmantosim gan pent-2-enu, gan 1-hlor-2-fluor-ciklobutānu:
a) E-izomērs
ģeometriskais izomērs kur sarežģītāki ligandi vai tie, kuriem ir vislielākais atomu skaits, atrodas pretējās plaknēs. Šajā piemērā vissarežģītākais ligands uz oglekļa 2 ir metils, un vissarežģītākais ligands uz oglekļa 3 ir etils, kas izvietoti dažādās plaknēs.
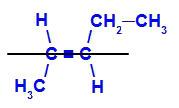
E-pent-2-ene strukturālā formula
b) Z izomērs
ģeometriskais izomērs kur sarežģītāki ligandi vai tie, kuriem ir vislielākais atomu skaits, atrodas vienā plaknē. Nākamajā piemērā vislielākais oglekļa 1 atomu skaitļa ligands ir hlors (Z = 17), un vislielākais oglekļa 2 atomu skaitļa ligands ir fluors (Z = 9), kas atrodas vienā plaknē.
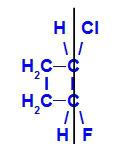
Z-1-hlor-2-fluor-ciklobutāna strukturālā formula
Autors: Diogo Lopes Dias
Avots: Brazīlijas skola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-isomeria-geometrica.htm

