Plkst parastās baterijas tiek saukti Leklanša baterijas nosaukts tā izgudrotāja, franču ķīmiķa Džordža Leklanē (1839-1882) vārdā.

Džordžs Leklančs (1839–1882)
Leklanša šāda veida akumulatorus izveidoja 1866. gadā. Viņu sauc arī sausa šūna jo līdz tam bija tikai baterijas, kurās izmantoja ūdens šķīdumus, piemēram, Daniela kaudze.
Divi citi nosaukumi, kurus šāda veida kaudzes saņem sava konstitūcijas dēļ, ir skābes kaudze vai cinka oglekļa akumulators. To galvenokārt veido cinka apvalks, kas atdalīts no citām ķīmiskajām sugām, kas veido kaudzi, ar porainu papīru.
Šis cinks atbilst šūnas vai anoda negatīvajam polam, jo tas oksidējas, zaudējot divus elektronus, saskaņā ar zemāk redzamo pusreakciju:
Negatīvais pols - anods: Zn s) → Zn2+(šeit) + 2 un-
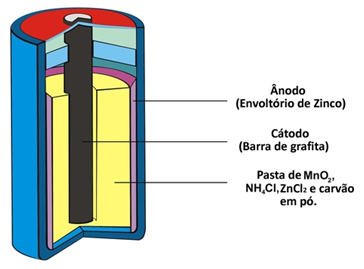
Šai kaudzei ir arī pozitīvs stabs - katods, kas ir grafīta josla, kas uzstādīta kaudzes vidū, ko ieskauj mangāna dioksīds (MnO2), ogļu pulveris (C) un mitra pasta, kas satur amonija hlorīdu (NH4Cl), cinka hlorīds (ZnCl2) un ūdeni (H2O).
Amonija hlorīds un cinka hlorīds ir sāļi ar skābu raksturu, tāpēc nosaukums ir “skābā šūna”.
Grafīta josla vada elektronus, kurus cinks zaudē mangānam, samazinot mangāna dioksīdu (MnO)2) līdz mangāna trioksīdam (Mn2O3) saskaņā ar šādu pusreakciju:
Pozitīvais stabs - katods: 2 MnO2 (aq) + 2 NH41+(šeit) + 2e- → 1 Mn2O3s) + 2NH3. punkta g) apakšpunkts + 1 stunda2O(1)
Mitrā pasta darbojas kā sāls punkts, ļaujot migrēt hidroksilanjonus (OH-) no grafīta līdz cinkam.
Vispārējo reakciju sniedz:
Zn s) + 2 MnO2 (aq) + 2 NH41+(šeit) → Zn2+(šeit) + 1 milj2O3s) + 2NH3. punkta g) apakšpunkts
Šīs baterijas kā tādas nav uzlādējamas, jo viss mangāna dioksīds tiek pārveidots par mangāna trioksīdu. Kad akumulators vairs nedarbojas, tas jāiznīcina.
Šo bateriju ddp ir 1,5 V. Tomēr amonjaks (NH3. punkta g) apakšpunkts), kas izveidojusies pie katoda, var noglabāt uz grafīta stieņa, kavējot elektronu pāreju un samazinot akumulatora spriegumu. Lai atgrieztos normālā darbībā, vienkārši atstājiet akumulatoru atpūtai ārpus ierīces, jo cinka katjons (Zn2+(šeit)), kas izveidojusies pie anoda, reaģē ar amonjaku, atstājot grafīta stieni brīvu.
Turklāt var palīdzēt arī kaudzes ievietošana ledusskapī, jo temperatūras pazemināšana veicina amonjaka šķīdību kaudzes mitrajā pastā.
Vēl viens svarīgs Leclanché sauso šūnu faktors, kas mums jāņem vērā, ir tas cinka korpuss var korozēt un tādējādi noplūst kodīgo materiālu un sabojāt ierīci.. Tāpēc vislabāk ir neatstāt akumulatorus ierīcēs, kuras netiek nepārtraukti izmantotas.
Sausas baterijas ir paredzētas iekārtām, kurām nepieciešama viegla un nepārtraukta izlāde, piemēram, tālvadības pults, sienas pulkstenis, pārnēsājamais radio un rotaļlietas.
Autore Jennifer Fogaça
Beidzis ķīmiju
Avots: Brazīlijas skola - https://brasilescola.uol.com.br/quimica/pilha-seca-leclanche.htm

