O tehnēcijs ir elements atomskaitlis 43, kas pieder periodiskās tabulas 7. grupai. Tas ir pārejas metāls un bija pirmais mākslīgi ražotais elements cilvēces vēsturē. Joprojām tiek apspriests, vai metālu var atrast dabiski Zemes garoza.
Šo elementu plaši izmanto kodolmedicīnā, jo tam ir izotops, kas spēj radīt attēlus, ko izmanto audzēju diagnosticēšanai dažādos orgānos. Cilvēka ķermenis. Lai gan tā ķīmija nav tik attīstīta, interese par to ir saistīta ar kodolmedicīnu.
Izlasi arī:Niobijs - vēl viens pārejas metāls
Kopsavilkums par tehnēciju
- Tehnēcijs bija pirmais mākslīgi ražotais elements.
- Ķīmiski šis metāls ir ļoti līdzīgs rēnijs, arī no 7. grupas.
- Tiek spekulēts par tehnēcija klātbūtni zemes garozā, taču tā ražošana joprojām ir pilnībā mākslīga.
- Elementu plaši izmanto kodolmedicīnā audzēju diagnosticēšanai un dažādu orgānu attēlveidošanai.
- To atklāja itāļu zinātnieka Emilio Segrē grupa 1937. gadā.
Tehnēcija īpašības
- Simbols: Tc.
- Atomu skaits: 43.
- Atomu masa: 98 c.u.
- Elektroniskā konfigurācija: [Kr] 5s2 4d5.
- Sadales punkts: 2157°C.
- Vārīšanās punkts: 4265°C.
- Blīvums: 11,50 g.cm-3.
- Ķīmiskā sērija: pārejas metāls; 7. grupa.
Nepārtrauciet tagad... Pēc sludinājuma ir vēl kas ;)
Tehnēcija īpašības
Tehnēcijs sākotnēji ir elements mākslīgs, pirmais, ko radījusi cilvēce. Tehnēcijs metālisks kilogramu diapazonā jau ir ražots, sākotnēji samazinot Tc2s7 1100 °C temperatūrā ar gāzi ūdeņradis. Pašlaik tiek samazināts amonija pertehnetāts (NH4TcO4), arī ar ūdeņraža gāzi.
Metāliskā formā tehnēcijs ir sudrabaini pelēks un, saskaroties ar gaisu, lēnām kļūst tumšāks. Jāatzīmē, ka jūsu ķīmija ir līdzīgs rēnijam, elements, kas atrodas tieši zem 7. grupas. Piemēram, sadalot, abi var sadegt saskarē ar gaisu aptuveni 370 °C temperatūrā. Viņiem ir arī kopīgs spēja reaģēt ar halogēni.
Tehnēcijs tajā nešķīst sālsskābe bez koncentrācijas, bet šķīst:
- skābe slāpekļa;
- aqua regia (slāpekļskābes un sālsskābes maisījums augstā koncentrācijā);
- sērskābe.
štati oksidēšanās Visizplatītākās tehnēcija vērtības svārstās no 0 līdz +7, bet lielākajai daļai tehnēcija ķīmijas ir pertehnetāta anjons (TcO4-) kā prekursoru.
Šobrīd tie ir kataloģizēti 43 izotopi tehnēcija, kura masas svārstās no 86 līdz 113. Starp dažiem šo izotopu piemēriem ir 97Tc, ar Pus dzīve no 2,6 x 106 gadi, un 98Tc, ar pussabrukšanas periodu 4,2 x 106 gadus vecs. Ķīmiski visvairāk izmantotais izotops ir 99Tc, ar pussabrukšanas periodu 2,1 x 105 gadus vecs.
Skatīt arī: Bārijs - vēl viens sudraba krāsas elements
Tehnēcija rašanās
Mēdz teikt, ka tehnēcijs uz mūsu planētas dabā nenotiek, tas ir tikai sintētiski sagatavots. Tomēr 1956. gadā japāņu ķīmiķis Pols Kuroda prognozēja, ka sava veida dabiskais kodolreaktors varēja pastāvēt gada dziļumos planēta.
Piecus gadus vēlāk, 1961. gadā, Kuroda ziņoja klātbūtne 99Tc piķa maisījuma paraugā (ar urānu bagāts minerāls), kura saturs būtu aptuveni 2 x 10-10 grami izotopu uz kilogramu minerālvielu.

Vēlāk, 1962. gadā, franču pētnieki apstiprināja Kuroda teorijas, novērtējot iežu paraugus Gabona un pat norādīja uz tehnēcija pēdu klātbūtni paraugos. Tātad, Ideja, ka nav dabiskā tehnēcija, ir pretrunīga, par ko notiek lielas diskusijas zinātnieku aprindās.
Attiecībā uz telpu tehnēcijs tika konstatēts izsaukumos zvaigznes milzu sarkans, 1950. gados, bet ne Saule, kas palīdz pierādīt, ka Saule ir salīdzinoši jauna zvaigzne. Tehnēcija noteikšana šajās zvaigznēs bija ļoti svarīga, jo elementa pussabrukšanas periods ir daudz īsāks. nekā šo zvaigžņu vecums, kas liecina, ka šajos ķermeņos faktiski tiek ražots tehnēcijs debesu.
Tehnēcija iegūšana
Lai gan notiek diskusijas par tehnēcija dabisko klātbūtni vai neesamību uz mūsu planētas, tas ir fakts, ka Tehnēcija ražošana notiek ar mākslīgiem līdzekļiem atomelektrostacijās. Tas atbilst aptuveni 6% no sadalīšanās produktiem urāns, kas tika atgūts pēc daudziem gadiem.
Tā atgūšana notiek tādā veidā, kas dod laiku produktiem skaldīšana īss pussabrukšanas periods un ir ļoti radioaktīvi. Parasti tehnēciju atdala no citiem skaldīšanas produktiem, izmantojot jonu apmaiņas sveķus vai ekstrakciju ar šķīdinātāju.
Zināt arī: Dubnijs ir ļoti radioaktīvs mākslīgais elements
Tehnēcija lietojumi
Tehnēcija galvenais lietojums ir kodolmedicīna, īpaši audzēju diagnostikā.Tam izmanto izotopu sabrukšanu 99 mTc, kas atbilst metastabilajam izotopam 99Tc. Metastabila forma ir tradicionālā izotopa ierosinātā forma, tas ir, enerģiskāka, ar izteiktām kodolīpašībām.

Medicīniskiem nolūkiem, 99 mTc pacientam formā a risinājums fizioloģiskais šķīdums, kas tiks absorbēts orgāns jānovērtē. Šo izotopu ražo no molibdēna-99 (99Mo), arī sintētisks, veido anjonu [99MoO4]2-, kas sadalās, izdalot β daļiņas un rada [99 mTcO4]-, ķīmiskā forma, ko mēdza injicēt pacientam.
Šis metastabilais izotops ir ļoti piemērots šim nolūkam, jo pēc injicēšanas tas parasti sadalās līdz izotopam. 99Tc, izstaro starojums pietiekami daudz gamma (enerģijas), lai iegūtu rezultātu, ja tiek izmantots ļoti maz metastabilā izotopa, apmēram 1 x 10-9 1x10-12 kurmji
Kaut kas vienlīdz izdevīgs ir pussabrukšanas periods 99 mTc — sešu stundu diapazonā. Šis pusperiods ir pietiekami ilgs, lai paraugu varētu injicēt pacientam pirms jebkura sabrukšana, bet pietiekami maza, lai emisijas varētu izmērīt pie mazām koncentrācijām izotops.
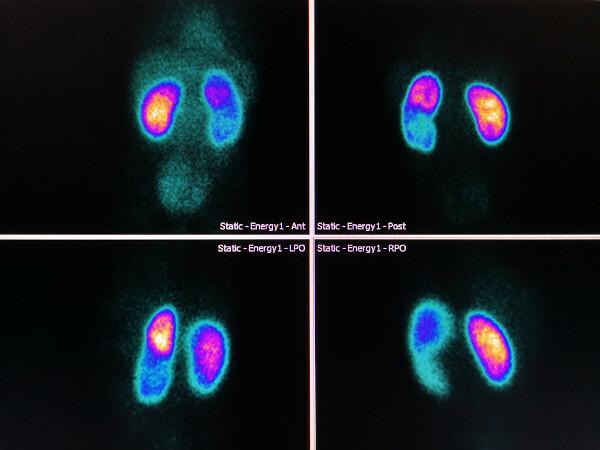
Viss atbrīvotais gamma starojums tiek izmantots attēla ģenerēšanai, kas var būt:
- divdimensiju (lai novērtētu audzēji un metastāzes);
- trīsdimensiju (lai izveidotu attēlus no sirds, kauli, aknas, nieres un smadzenes).
Piesardzības pasākumi ar tehnēciju

Ir nepieciešams pievērst uzmanību radioaktivitāte tehnēcija, galvenokārt tā, lai ar to būtu atbilstoša apstrāde. Nelielos daudzumos, piemēram, mazāk par 0,05 gramiem, radītie riski nav tik nopietni, lai gan ir nepieciešami piesardzības pasākumi. Piemēram, bīstamāks gamma starojums gandrīz nepastāv, bet beta emisijas viegli ierobežo stikls.
Jāatceras arī, ka tehnēcija izotopiem ir ilgs pussabrukšanas periods. Tāpēc radītā starojuma daudzums īsā laika intervālā ir neliels, kas vēl vairāk pastiprina nepieciešamību strādāt nelielos daudzumos.
Viens no veidiem, kā manipulēt ar tehnēciju, ietver cimdu kapuces lietošana, lai paraugs būtu izolēts un operators netiktu pakļauts ar radiāciju saistītiem riskiem.
Uzziniet vairāk: Kuri periodiskās tabulas elementi ir radioaktīvi?
tehnēcija vēsture
7. grupa Periodiskā tabula ilgu laiku piesaistīja uzmanību, jo, izstrādājot Dmitrija Mendeļejeva oriģinālo tabulu, tikai viens elements ķīmisks tajā ietverts: mangāns. Tādējādi 20. gs. ir veikti daudzi mēģinājumi atklāt 7. grupas elementus, vairums no tiem acīmredzami ir neefektīvi.
Tomēr 1925. gadā Otto Bergs, Valters Noddaks un Ida Take (vēlāk Ida Noddaka) apgalvoja, ka ir atklājuši nevis viens, bet divi jauni 7. grupas elementi, kurus viņi nosauca par masurium (Z = 43) un rēniju (Z = 75). Otrais tika pieņemts, bet 43. elementam nebija tādas pašas cieņas, jo tas ir daudzu strīdu objekts.
Saskaroties ar daudziem strupceļiem, oficiālā 43. elementa atklāšana ir itālis Emilio Segrè, kuram palīdzēja viņa pētnieku grupa, 1937. g. Segrè un viņa komanda guva panākumus, manipulējot ar molibdēna paraugu, ko vairākus mēnešus bombardēja deitērijs.
Pēc vairākām analīzēm Itālijas komandai izdevās identificēt šo jauno elementu, ko varēja atdalīt, vārot ar nātrija hidroksīds un neliels daudzums ūdeņraža peroksīds.
Tehnēcija nosaukums cēlies no grieķu valodas tehnetos un nozīmē "mākslīgs". |
Uz tehnēcija risināti vingrinājumi
jautājums 1
(ESCS-DF 2011) Kodolmedicīnā radiofarmaceitiskos preparātus izmanto dažādu slimību diagnostikā un ārstēšanā. Daži radiofarmaceitiskie preparāti izmanto tehnēciju-99m (Tc-99m), kam ir noderīgas īpašības kā marķieris. gamma-emitera nuklīds, un to var izmantot smadzeņu, miokarda, vairogdziedzera, plaušu un citi.
Radioizotopa izmantošana ir atkarīga no tā ķīmiskajām un bioloģiskajām īpašībām, tostarp tā pussabrukšanas perioda. 99mTc izotopa pussabrukšanas periods ir sešas stundas, kas ir pietiekams, lai tas uzkrātos pētāmajā orgānā un lai tas ilgstoši nepaliktu organismā.
99mTc masa, kas nepieciešama konkrēta testa veikšanai, atbilst 500 mg. Ņemot vērā, ka pacientam šī izmeklēšana tiks veikta 12 stundas pēc radionuklīda ievadīšanas, minimālais radiofarmaceitiskā preparāta daudzums, kas pacientam jāsaņem, ir vienāds ar:
A) 2 g
B) 1 g
C) 500 mg
D) 250 mg
E) 125 mg
Izšķirtspēja:
Alternatīva A
Pussabrukšanas periods ir laiks, kas nepieciešams, lai radioaktīvā parauga daudzums samazinās uz pusi. Pacients veiks izmeklēšanu 12 stundas pēc ievadīšanas 99 mTc, kura pussabrukšanas periods ir sešas stundas.
Ja nepieciešami 500 mg, tas nozīmē, ka pēc 12 stundām tikai 500 mg no 99 mTc būs pieejams. 12 stundu laikā bija pagājuši divi pussabrukšanas periodi, kas nozīmē, ka paraugs tika dubultots uz pusi, t.i., sākotnējais daudzums tika dalīts ar četriem.
Tādējādi sākotnējais radiofarmaceitiskā līdzekļa daudzums, kas pacientam jāsaņem, ir vismaz 2 grami, jo pēc 12 stundām parauga paliks vairs tikai 500 mg.
2. jautājums
(Fameca-SP 2014) Attēlā parādīts 99mTc (metastable tehnēcijs-99) ģenerators, ko Brazīlijā ražo Ipen. Šis radionuklīds, ko izmanto kodolmedicīnā, tiek nepārtraukti ražots, sabrūkot “sākuma” radionuklīdam, kas ir 99Mo (molibdēns-99). Diagrammā ir parādīta šo ģeneratoru tipiskā 99 Mo darbība kā laika funkcija dienās.

Kodolvienādojumā, kas attiecas uz 99Mo, “sākotnējā” nuklīda, sabrukšanu līdz 99mTc, “meitas” nuklīdam, ir izdalīšanās
A) alfa daļiņas.
B) negatīvās beta daļiņas.
C) pozitīvas beta daļiņas.
D) neitroni.
E) protoni.
Izšķirtspēja:
Alternatīva C
gan 99Cik daudz 99 mTc ir vienāda masa. "m" iekšā 99 mTc tikai nozīmē, ka tas ir metastabils izotops, tas ir, tas atrodas augstākā enerģijas līmenī nekā izotops 99Parastais Tc, bet bez jebkādiem traucējumiem masā.
Molibdēna atomu skaits ir 42, savukārt tehnēcija atomu skaits ir 43.
Tādējādi var redzēt, ka sabrukšanas laikā 99Mo ražošanai 99 mTc notika masas saglabāšana un atomskaitļa palielināšanās par vienu vienību. Tas ir raksturīgs negatīvo beta daļiņu emisijai, jo šīm daļiņām ir niecīga masa un atomskaitlis ir vienāds ar -1, tāpat kā elektrons.
Autors Stefano Araújo Novais
Ķīmijas skolotājs



