Spirti var oksidēties, ja tie tiek pakļauti oksidējošam aģentam, piemēram, kālija dihromāta (K) ūdens šķīdumam2Kr2O7) vai kālija permanganāts (KMnO4) skābā vidē.
Topošais skābeklis [O] vidū uzbruks ogleklim, kas saistīts ar spirta funkcionālo grupu (hidroksilgrupa) OH), veidojot ļoti nestabilu savienojumu, ko sauc par dvīņu diolu, kurā ir divi hidroksili, kas saistīti ar vienu un to pašu. ogleklis. Tā kā šis savienojums ir nestabils, tas atbrīvo ūdeni un rada jaunu produktu.
Šis produkts būs atkarīgs no oksidētā spirta veida, neatkarīgi no tā, vai tas ir primārais, sekundārais, terciārais vai metanols.
Īsumā, mums ir:
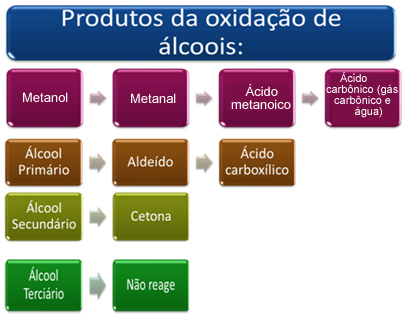
Skatiet katru gadījumu zemāk:
- Metanols (H3C─ OH):
Metanols ir vienīgais spirts, kurā ir trīs ūdeņraži, kas saistīti ar oglekli, kas oksidējas. Šajā gadījumā, tā kā molekulā ir trīs punkti, kuriem topošais skābeklis var uzbrukt, notiks trīs secīgas oksidācijas, kā parādīts zemāk esošajā diagrammā:
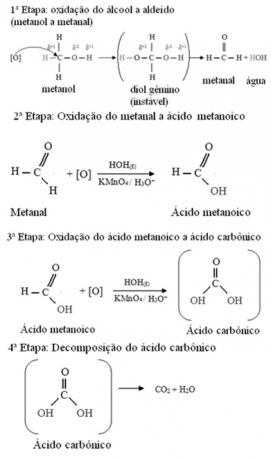
- Primārie spirti:
Šajos savienojumos hidroksilogleklis ir saistīts tikai ar vienu oglekļa atomu, tas ir, divi pārējie ligandi ir ūdeņraži, un topošajam skābeklim ir divas uzbrukuma vietas.
Pirmkārt, veidosies aldehīds, kā parādīts zemāk:
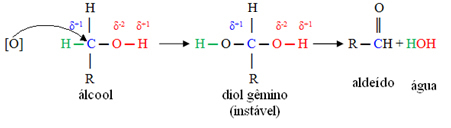
Bet oksidēšana turpinās, jo spirta oksidēšanai izmantotie reaģenti ir spēcīgāki nekā tie, ko izmanto aldehīda oksidēšanai. Tad cits topošais skābeklis uzbrūk karbonilogleklim un ražo karbonskābi.
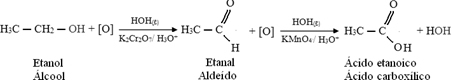
Tālāk ir sniegts piemērs etanola oksidēšanai, vispirms par etanālu un pēc tam par etānskābi (etiķskābi). Šī kopējā reakcija ir vīna pārvēršana etiķī.
Nepārtrauciet tagad... Pēc reklāmas ir vēl kas ;)
Etanola daļēja oksidēšanās par etanālu notiek, kad alkoholiķis veic vienreizējās lietošanas alkometra pārbaudi. Šīs ierīces iekšpusē ir ciets kālija dihromāta un silīcija dioksīda maisījums skābā vidē, un notiek šāda reakcija:
K2Kr2O7(aq) + 4H2TIKAI4(aq) + 3 CH3CH2ak(g) → Kr2(TIKAI4)3(aq) + 7 no rīta2O(1) + 3 CH3CHO(g) + K2TIKAI4(aq)
apelsīnsetanols (bezkrāsains)zaļšetanāls (bezkrāsains)
Ņemiet vērā, ka papildus etanola (spirta) oksidēšanai par etanālu (aldehīdu) vienlaikus tiek reducēts dihromāts, kas ir oranžs, līdz hromam (III) vai pat hromam (II), kas ir zaļš. Krāsas maiņa liecinās, ka cilvēka asinīs ir vairāk alkohola nekā atļauts.
- Sekundārie spirti:
Tie ir savienojumi, kuros hidroksilgrupas ogleklis ir saistīts ar diviem citiem oglekļa atomiem un tikai vienu ūdeņraža atomu. Tāpēc molekulā būs tikai viena vieta, kur topošais skābeklis var uzbrukt, un veidosies tikai viena veida produkts, kas vienmēr būs ketons:
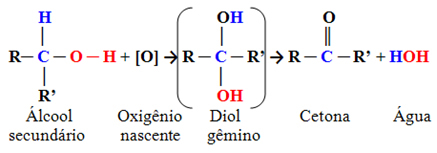
Tā kā ketona karbonilogleklim nav tieši ar to saistīts ūdeņradis, vairs nav iespējama turpmāka oksidēšanās. Tāpēc reakcija apstājas pie ketona.
- Terciārie spirti:
Terciārie spirti ir tie, kuros ogleklis, kurā ir -OH grupa, veido trīs saites ar citiem oglekļa atomiem. Tā kā tie nesaistās ar ūdeņražiem, molekulai nav nekādas jēgas, ko varētu uzbrukt topošais skābeklis. Šī iemesla dēļ terciārie spirti netiek oksidēti.
* Avots un attēla autors: CostaPPPR.
Autore: Dženifera Fogača
Beidzis ķīmiju
Vai vēlaties atsaukties uz šo tekstu kādā skolā vai akadēmiskajā darbā? Skaties:
FOGAÇA, Dženifera Roča Vargasa. "Spirtu oksidēšana"; Brazīlijas skola. Pieejams: https://brasilescola.uol.com.br/quimica/oxidacao-dos-alcoois.htm. Skatīts 2021. gada 27. jūlijā.
Ķīmija

Kā darbojas alkometrs, alkohola koncentrācija, alkometrs, reakcijas ar etilspirtu, veidi alkometri, kālija dihromāts, degvielas šūna, katalizators, elektronu atbrīvošana, etiķskābe, ūdeņradis, konce