Oksidācija ir nosaukums, kas dots elektronu zuduma procesam atoma, grupas vai jonu sugas laikā a ķīmiskā reakcija. To nosaka pēc pieauguma NOX sugas vai atoma (oksidācijas numurs), salīdzinot reaģentu un produktu.
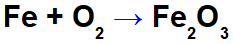
Dzelzs oksidācijas vienādojums.
Piemēram, augstāk esošajā vienādojumā mēs varam norādīt katra dalībnieka NOX:
Dzelzs reaģents (Fe): satur NOX 0, jo tas ir a vienkārša viela;
Skābeklis reaģentā (O): satur NOX 0, jo tā ir vienkārša viela;
Skābeklis produktā: tajā ir NOX-2, jo tas nav saistīts ar sārmu metālu, sārmzeme vai ūdeņraža veidošanās peroksīdi vai superoksīdi;
Dzelzs produktā: tajā ir NOX +3, jo dzelzs NOX summai, kas reizināta ar 2 (atomu skaits) + skābekļa NOX, reizinātai ar 3, ir jābūt 0, jo tā ir salikta viela:
x.2 + 3.(-2) = 0
2x - 6 = 0
2x = +6
x = + 6
2
x = +3
Salīdzinot reaģenta dzelzs (0) NOX ar produktu (+3), mēs novērojām pieaugumu, tas ir, tas tika pakļauts procesam oksidēšanās. Ir vērts atzīmēt, ka rašanās oksidēšanās to vienmēr pavada reducēšanās fenomens (kas nozīmē elektronu pieaugumu), ko identificē ar NOx samazināšanos, kā tas notiek piemērā ar skābekli.
Nepārtrauciet tagad... Pēc reklāmas ir vēl kas ;)
Izlasi arī:Oksidācijas skaita (NOX) noteikšana
Situāciju piemēri, kad notiek oksidēšanās:
1. Degšana

Materiāla sadegšana arī liecina par oksidēšanos.
Degšana ir katra ķīmiskā reakcija, kas notiek a klātbūtnē degviela jebkura un oksidējošā skābekļa gāze (O2), kā rezultātā tiek ražots siltums un gaisma. Katrā degšanas reakcijā notiek oksidēšanās.
2. Dažas organiskas reakcijas
Katrā organiskajā reakcijā, kas notiek tālāk uzskaitīto līdzekļu klātbūtnē, process oksidēšanās:
Kālija dihromāts (K2Kr2O7) vai kālija permanganāts (KMnO4);
spēcīgas skābes vai stipras bāzes klātbūtne;
Ozona gāze (O3) metāliska cinka (Zn) un ūdens (H2O).
3. Baterijas vai baterijas

Baterijas ir ierīces, kurās vienmēr notiek oksidēšanās.
Stacks vai baterijas ir elektroķīmiskas ierīces, kas uzglabā ķīmiskās vielas. Viena no šīm vielām tiks oksidēta, bet otra - reducēta, kā rezultātā veidojas elektriskā strāva.
4. Elektrolīze
Elektrolīze ir ķīmisks process, kurā ūdens šķīdums, kas satur sāli, tiek pakļauts elektriskās strāvas iedarbībai, kas veicina šajos materiālos esošo anjonu oksidēšanos. Visā elektrolīzē ir oksidēšanās.
Es. Diogo Lopes Dias
Vai vēlaties atsaukties uz šo tekstu kādā skolā vai akadēmiskajā darbā? Skaties:
DIENAS, Diogo Lopes. "Kas ir oksidēšana?"; Brazīlijas skola. Pieejams: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-oxidacao.htm. Skatīts 2021. gada 27. jūlijā.