Organiskā ķīmija ir plaša ķīmijas joma, kas pēta oglekļa savienojumus.
Organiskās ķīmijas zināšanas tiek tuvinātas vairākos veidos, un, domājot par tām, mēs esam salikuši jums piedāvātos vingrinājumus, iestājeksāmenus un Enem jautājumus, lai pārbaudītu savas zināšanas.
Izmantojiet arī rezolūciju komentārus, lai uzzinātu vēl vairāk par šo tēmu.
Piedāvātie vingrinājumi
jautājums 1
Apskatiet zemāk esošos organiskos savienojumus un identificējiet organiskās funkcijas atbilstoši iezīmētajām funkcionālajām grupām. Pēc tam nosauciet vielas.
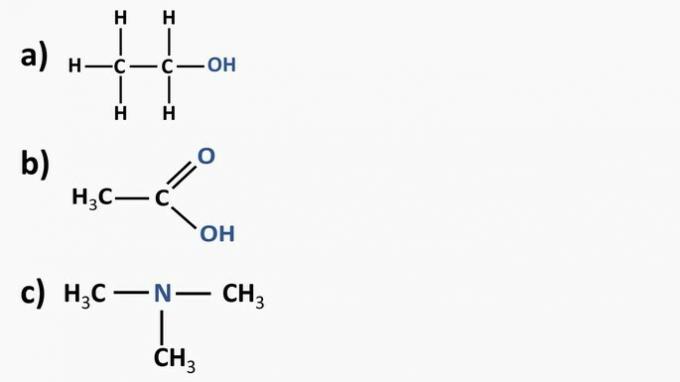
Atbildēt:
a) Organiskais savienojums: etanols
- organiskā funkcija: alkohols
- Vispārīgā formula: R — OH
- Identifikācija: hidroksilgrupa (OH), kas saistīta ar oglekļa ķēdi
b) Organiskais savienojums: etānskābe.
- Organiskā funkcija: karbonskābe
- Vispārīgā formula: R — COOH
- Identifikācija: karboksilgrupa (COOH), kas saistīta ar oglekļa ķēdi
c) Organiskais savienojums: trimetilamīns
- Organiskā funkcija: amīns (terciārs)
- Vispārīgā formula:
- Identifikācija: slāpeklis ir saistīts ar trim oglekļa ķēdēm
2. jautājums
Organiskajā ķīmijā savienojumus atpazīst pēc ķēdēm, kuras veido ogleklis un ūdeņradis. Tomēr citi elementi var būt daļa no šo savienojumu ķīmiskās struktūras, piemēram, skābeklis.
Atlasiet alternatīvu, kur abiem organiskajiem savienojumiem ir organiskas skābekļa piedevas.
a) hloroforms un etilmetanāts
b) propanols un propānskābe
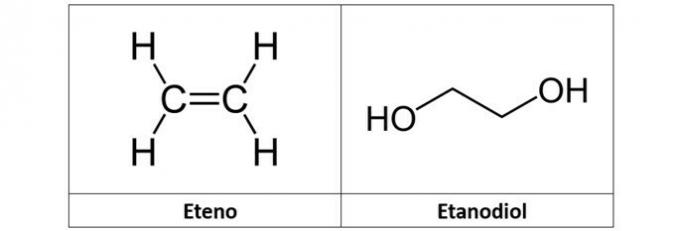
c) etēns un etāndiols
d) etanamīds un benzols
Pareiza atbilde: b) propanols un propānskābe
a) nepareizi. Mums ir hloroforms (CHCl3), kas ir alkilhalogenīds, un etilmetanoāta esteris (C.3H6O2), kura struktūra satur skābekli.
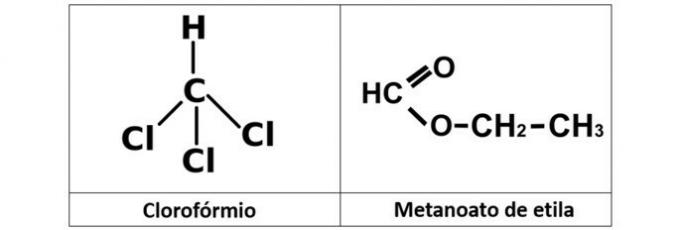
b) PAREIZI. Šajā alternatīvā mums ir divi savienojumi, kuriem ir organiskās funkcijas ar skābekli. Propanols (C.3H8O) ir spirts, ko veido trīs ogles. Propānskābe (C.3H6O2) ir karbonskābe.
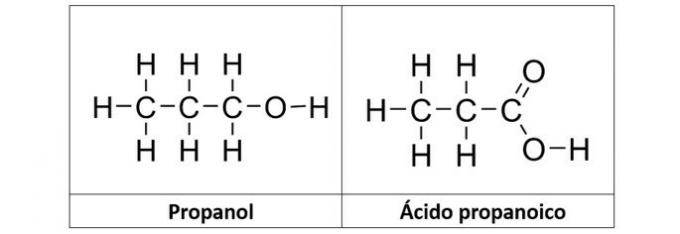
c) nepareizi. Etilēns (C.2H4), saukts arī par etilēnu, ir alkēna tipa ogļūdeņradis. Jau etāndiols (C.2H6O2) ir spirts ar diviem hidroksiliem savā struktūrā.
d) nepareizi. Etanamīds (C.2H5NO) ir amīds, un benzols ir aromātisks ogļūdeņradis, un tāpēc to veido tikai ogleklis un ūdeņradis.

3. jautājums
Apskatiet zemāk esošo organisko savienojumu struktūru un pārbaudiet patiesos apgalvojumus.

(01) Savienojumam ir organiskā slāpekļa funkcija.
(02) Tas ir primārais amīns, jo tas ir saistīts tikai ar vienu ūdeņradi.
(03) Savienojuma nosaukums ir dietilamīns.
Pareiza atbilde:
(01) PAREIZI. Organiskā slāpekļa funkcija savienojumā ir amīns.
(02) nepareizi. Tas ir sekundārs amīns, jo slāpeklis ir saistīts ar divām oglekļa ķēdēm.
(03) nepareizi. Savienojuma nosaukums ir dimetilamīns, jo slāpeklim ir pievienoti divi metilgrupas.
4. jautājums
Eugenols, fenilpropanoīdu grupas pārstāvis, ir aromātisks organisks savienojums, kas atrodas krustnagliņās - garšviela, ko lieto kopš seniem laikiem.

Ievērojiet savienojuma strukturālo formulu un identificējiet esošās organiskās funkcijas.
a) Alkohols un ēteris
b) fenols un ēteris
c) Alkohols un esteris
d) fenols un esteris
e) Alkohols un ogļūdeņradis
Pareiza alternatīva: b) fenols un ēteris.
Eugenola ķēdē ir skābekļa organiskās funkcijas, tas ir, papildus oglekļa un ūdeņraža atomiem, skābeklis ir heteroatoms.
Organisko fenola funkciju raksturo hidroksilgrupa (-OH), kas pievienota aromātiskajam gredzenam. Ētera funkcijā skābeklis atrodas starp divām oglekļa ķēdēm.
5. jautājums
EDTA, kura pilnais nosaukums ir etilēndiamīntetraetiķskābe, ir organisks savienojums, kam ir daudz pielietojumu. Tā spēja saistīt metāla jonus padara to par helātu veidojošu līdzekli, ko plaši izmanto gan laboratorijā, gan rūpnieciski.
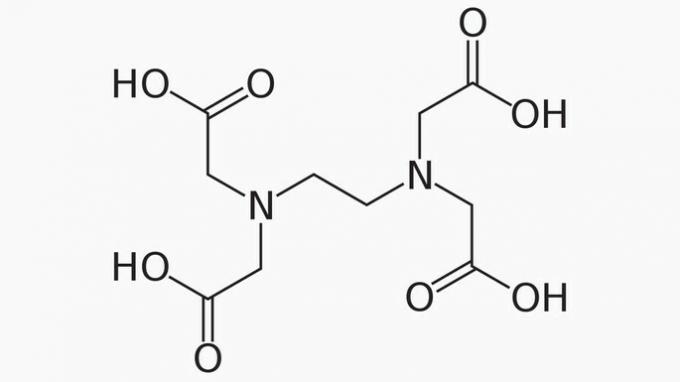
Par EDTA ir pareizi apgalvot, ka oglekļa ķēde ir:
a) atvērts, viendabīgs un nepiesātināts.
b) slēgts, neviendabīgs un piesātināts.
c) atvērts, neviendabīgs un nepiesātināts.
d) slēgts, viendabīgs un piesātināts.
e) atvērts, neviendabīgs un piesātināts.
Pareiza atbilde: e) atklāta, neviendabīga un piesātināta.
EDTA ķēde tiek klasificēta:
ATVĒRTS. Saskaņā ar oglekļa atomu izvietojumu EDTA struktūrā mēs varam redzēt, ka galu klātbūtnes dēļ savienojuma ķēde tiek atvērta.
HETEROGĒNI. Papildus oglekļa un ūdeņraža savienojumiem oglekļa ķēdē ir slāpekļa un skābekļa heteroatomi.
PATIESA. Saites starp oglekļa atomiem ir piesātinātas, jo ķēdei ir tikai atsevišķas saites.
Uzziniet vairāk vietnē: Organiskā ķīmija.
iestājeksāmena jautājumi
jautājums 1
(UFSC) Novērojiet nepilnīgas organiskās struktūras un identificējiet pareizo (-os) vienumu (-us):
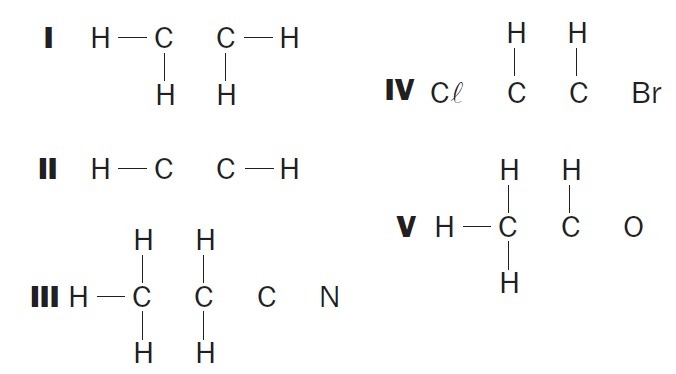
(01) I struktūrā trūkst vienas saites starp oglekļa atomiem.
(02) II struktūrā trūkst trīskāršās saites starp oglekļa atomiem.
(03) III struktūrā trūkst divu atsevišķu saišu starp oglekļa atomiem un trīskāršu starp oglekļa un slāpekļa atomiem.
(04) IV struktūrā trūkst divu atsevišķu saišu starp oglekļa atomiem un halogēniem un divkāršas saites starp oglekļa atomiem.
(05) V struktūrā trūkst vienas saites starp oglekļa atomiem un vienas saites starp oglekļa un skābekļa atomiem.
Pareizas alternatīvas: 02, 03 un 04.
Papildus ogleklim, kas ir obligāts organisko savienojumu ķīmiskais elements, struktūrās var būt arī citi elementi un tie ir saistīti ar kovalentām saitēm, kur elektroni ir kopīgi.
Elementu valence nosaka izveidojamo saišu skaitu, kā parādīts zemāk esošajā tabulā.
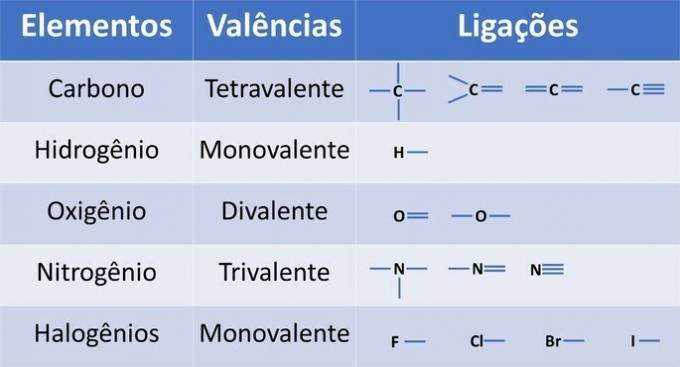
No šīs informācijas mums ir:
(01) nepareizi. Struktūrai trūkst dubultās saites starp oglekļa atomiem, veidojot etēna savienojumu.
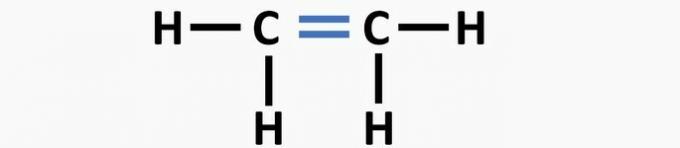
(02) PAREIZI. Struktūrai nav trīskāršas saites starp oglekļa atomiem, lai izveidotu etīna savienojumu.
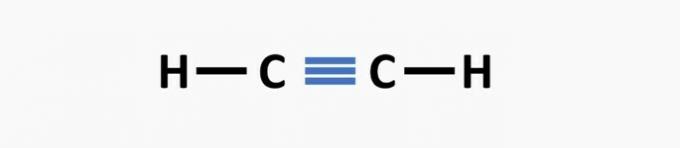
(03) PAREIZI. Struktūrai trūkst atsevišķu saišu starp oglekļiem un trīskāršu saišu starp oglekli un slāpekli, lai izveidotu savienojumu propanenitrilu.
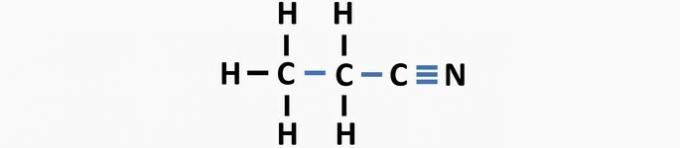
(04) PAREIZI. Struktūrai trūkst atsevišķu saikņu starp oglekli un halogēnu, un divkāršās saites starp ogļiem, lai izveidotu dihloretēna savienojumu.
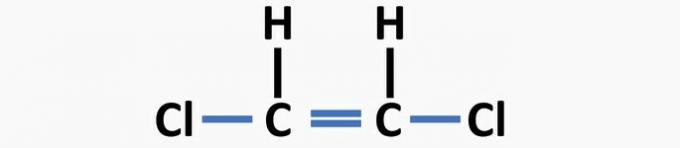
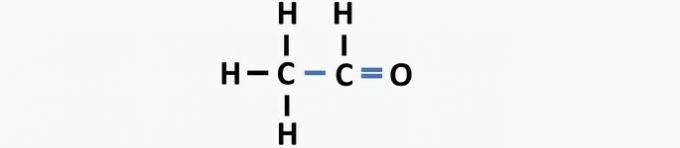
(05) nepareizi. Struktūrai trūkst vienas saites starp oglekļiem un divkāršās saites starp oglekli un skābekli, lai izveidotu etanāla savienojumu.
2. jautājums
Organiskā savienojuma ar molekulāro formulu C struktūra5H8Sazarota, nepiesātināta, neviendabīga un alicikliska ķēde ir šāda:

Pareiza alternatīva: d.
Oglekļa ķēdes var klasificēt šādi:
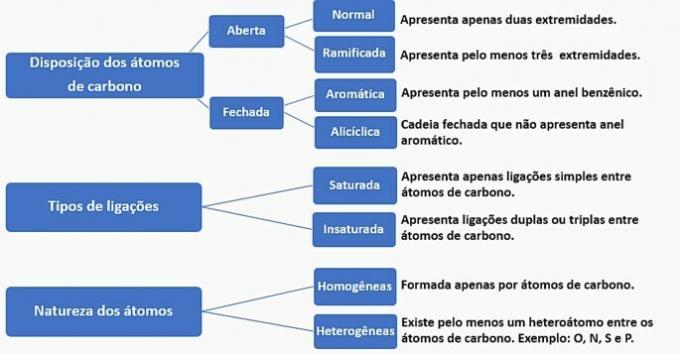
Saskaņā ar šo informāciju mums ir:
a) nepareizi. Ķēde tiek klasificēta kā normāla, piesātināta, viendabīga un alicikliska.
b) nepareizi. Ķēde ir klasificēta kā normāla, nepiesātināta, viendabīga un atvērta.
c) nepareizi. Ķēde tiek klasificēta kā sazarota, nepiesātināta, viendabīga un atvērta.
d) PAREIZI. Ķēde tiek klasificēta kā sazarota, nepiesātināta, neviendabīga un alicikliska, kā
- Tam ir filiāle: metilgrupa;
- Ir nepiesātinājums: dubultā saite starp oglekļiem;
- Tam ir heteroatoms: skābeklis, kas saistīts ar diviem ogļiem;
- Tam ir slēgta ķēde: ogles ir savienotas lokā bez aromātiska gredzena klātbūtnes.
e) nepareizi. Ķēde tiek klasificēta kā sazarota, nepiesātināta, neviendabīga un atvērta.
3. jautājums
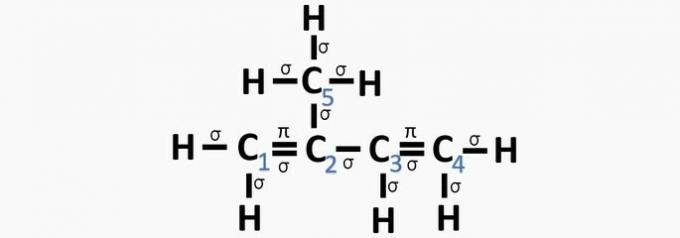
(Centec-BA) Zemāk parādītajā struktūrā numurētie ogļi ir attiecīgi:
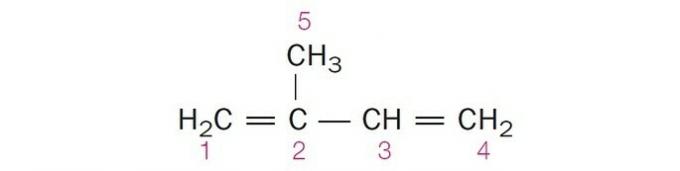
a) sp2, sp, sp2, sp2, sp3.
b) sp, sp3, sp2, sp, sp4.
c) sp2, sp2, sp2, sp2, sp3.
d) sp2, sp, sp, sp2, sp3.
e) sp3, sp, sp2, sp3, sp4.
Pareiza alternatīva: c) sp2, sp2, sp2, sp2, sp3.
Tā kā valences apvalkā ir 4 elektroni, ogleklis ir četrvērtīgs, tas ir, tam ir tendence veidot 4 kovalentās saites. Šīs obligācijas var būt vienas, dubultas vai trīskāršas.
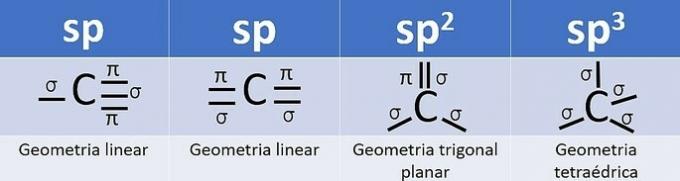
Hibrīdo orbitāļu skaits ir oglekļa sigmas saišu (σ) summa kopš saites hibridizējas.
- sp: 2 sigmas saites
- sp2: 3 sigmas saites
- sp3: 4 sigmas saites
Saskaņā ar šo informāciju mums ir:
a) nepareizi. Carbon 2 ir sp hibridizācija2, jo tam ir 3 σ saites un viena saite .
b) nepareizi. Ogleklim nav sp hibridizācijas4 un sp hibridizācija notiek, ja starp oglekļiem ir trīskāršā saite vai divas dubultās saites.
c) PAREIZI. Katra oglekļa σ saišu summa dod alternatīvu hibridizāciju.
d) nepareizi. Sp hibridizācija notiek, ja starp oglekļiem ir trīskāršā saite vai divas dubultās saites.
e) nepareizi. Ogleklim nav sp hibridizācijas4 un sp hibridizācija notiek, ja starp oglekļiem ir trīskāršā saite vai divas dubultās saites.
4. jautājums
(UFF) Ir gāzveida paraugs, ko veido viens no šiem savienojumiem: CH4; Ç2H4; Ç2H6; Ç3H6 vai C3H8. Ja 22 g šī parauga aizņem 24,6 L tilpumu pie 0,5 atm spiediena un 27 ° C temperatūrā (ņemot vērā: R = 0,082 L .atm. K–1.mol–1), tiek secināts, ka tā ir gāze:
a) etāns.
b) metāns.
c) propāns.
d) propēns.
e) etēns.
Pareiza alternatīva: c) propāns.
1. solis: pārveidojiet temperatūras mērvienību no Celsija uz Kelvinu.
2. solis: aprēķiniet savienojuma molu skaitu, izmantojot vispārējo gāzes vienādojumu.
3. solis: aprēķiniet savienojuma molisko masu.
4. solis: atrodiet ogļūdeņradi, kura molmasa ir 44 g / mol.
Metāns
Etēns
Etāns
propilēns
Propāns
Tādējādi tiek secināts, ka gāze, kas atbilst paziņojumā norādītajai informācijai, ir propāns.
5. jautājums
(ITA) Apsveriet šādas vielas:
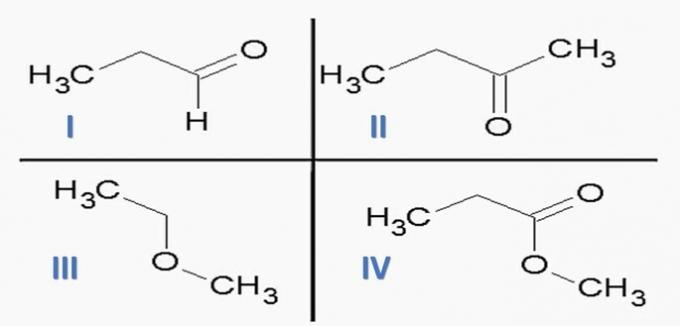
un šādas ķīmiskās funkcijas:
The. karbonskābe;
B. alkohols;
ç. aldehīds;
d. ketons;
un. esteris;
f. ēteris.
Iespēja, ka PAREIZI saista vielas ar ķīmiskajām funkcijām, ir:
a) Id; IIc; IIIe; IVf.
b) Ic; IId; IIIe; PVN
c) Ic; IId; IIIf; IVe.
d) Id; IIc; IIIf; IVe.
e) Ia; IIc; IIIe; IVd.
Pareiza alternatīva: c) Ic; IId; IIIf; IVe.
Organiskās funkcijas nosaka struktūras un grupu organiskie savienojumi ar līdzīgām īpašībām.
Alternatīvās ir šādas ķīmiskās funkcijas:
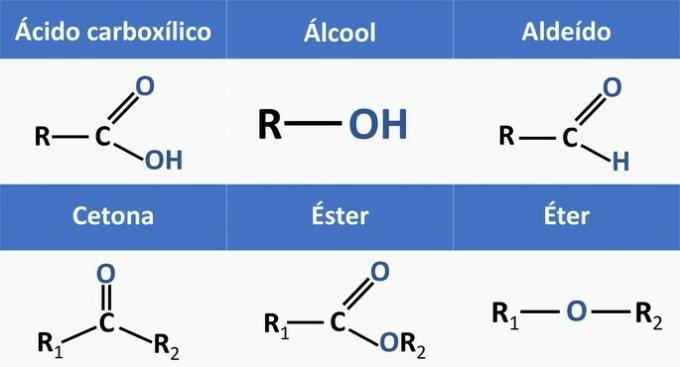
Analizējot iepriekš minētās struktūras un paziņojumā esošos savienojumus, mums ir:
a) nepareizi. Orgānu funkcijas ir pareizas, bet secība ir nepareiza.
b) nepareizi. Starp savienojumiem nav karbonskābes.
c) PAREIZI. Savienojumos esošās funkcionālās grupas pārstāv šādas ķīmiskās funkcijas.

d) nepareizi. Es esmu aldehīds un II ir ketons.
e) nepareizi. Starp savienojumiem nav karbonskābes.
Uzziniet vairāk vietnē: Organiskās funkcijas.
Enem jautājumi
jautājums 1
(Enem / 2014) Viena metode etanola satura noteikšanai benzīnā sastāv no zināmu ūdens un benzīna tilpumu sajaukšanas noteiktā pudelē. Pēc kolbas kratīšanas un noteiktu laika gaidīšanu mēra divu iegūto nesajaucošo fāžu tilpumus: vienu organisko un otru ūdens. Kādreiz etanols, kas sajaucās ar benzīnu, tagad sajaucas ar ūdeni.
Lai izskaidrotu etanola uzvedību pirms un pēc ūdens pievienošanas, ir jāzina
a) šķidrumu blīvums.
b) molekulu lielums.
c) šķidrumu viršanas temperatūra.
d) molekulās esošie atomi.
e) molekulu mijiedarbības veids.
Pareiza alternatīva: e) molekulu mijiedarbības veids.
Starpmolekulārie spēki ietekmē organisko savienojumu šķīdību. Vielas mēdz izšķīst viena ar otru, ja tām ir vienāds starpmolekulārais spēks.
Zemāk esošajā tabulā skatiet dažus organisko funkciju piemērus un molekulu mijiedarbības veidu.
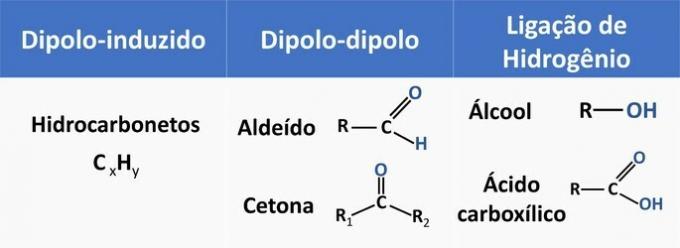
Etanolu uzskata par polāru šķīdinātāju, jo tā struktūrā ir polārā grupa (—OH). Tomēr tā oglekļa ķēde, būdama nepolāra (CH), spēj mijiedarboties ar nepolāriem šķīdinātājiem. Tāpēc etanols izšķīst gan ūdenī, gan benzīnā.
Saskaņā ar šo informāciju mums ir:
a) nepareizi. Blīvums ķermeņa masu saista ar aizņemto tilpumu.
b) nepareizi. Molekulu lielums ietekmē savienojumu polaritāti: jo lielāka ir oglekļa ķēde, jo viela kļūst nepolārāka.
c) nepareizi. Vārīšanās temperatūra ir noderīga molekulu atdalīšanai: destilējot atdala savienojumus ar dažādām viršanas temperatūrām. Jo zemāka viršanas temperatūra, jo vieglāk molekula tiek iztvaikota.
d) nepareizi. Aldehīda struktūrā ir ogleklis, ūdeņradis un skābeklis. Šis savienojums veic mijiedarbību ar dipolu un dipolu, savukārt spirts, kam ir vienādi elementi, spēj veidot ūdeņraža saites.
e) PAREIZI. Etanola mijiedarbība ar ūdeni (ūdeņraža savienošana) ir intensīvāka nekā ar benzīnu (diplo izraisīta).
2. jautājums
(Enem / 2013) Molekulas nanoputians tie atgādina cilvēku figūras un tika izveidoti, lai stimulētu jauniešu interesi saprast valodu, kas izteikta strukturālajās formulās, ko plaši izmanto organiskajā ķīmijā. Piemērs ir NanoKid, kas attēlots attēlā:
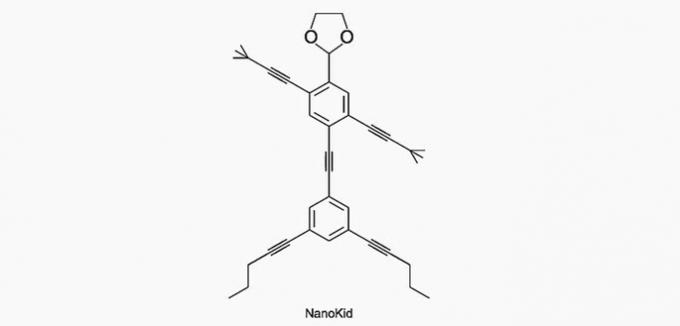
Kur NanoKid ķermenī ir kvaternārais ogleklis?
a) Rokas.
b) Galva.
c) Krūtis.
d) Vēders.
e) Pēdas.
Pareiza alternatīva: a) rokas.
Ogleklis tiek klasificēts šādi:
- Primārais: saistās ar oglekli;
- Sekundārā: saistās ar diviem ogļiem;
- Terciārā: saistās ar trim oglekļiem;
- Kvartārs: saistās ar četriem oglekļiem.
Skatiet piemērus zemāk.

Saskaņā ar šo informāciju mums ir:
a) PAREIZI. Rokā esošais ogleklis ir saistīts ar četriem citiem oglekļiem, tāpēc tas ir kvartārs.
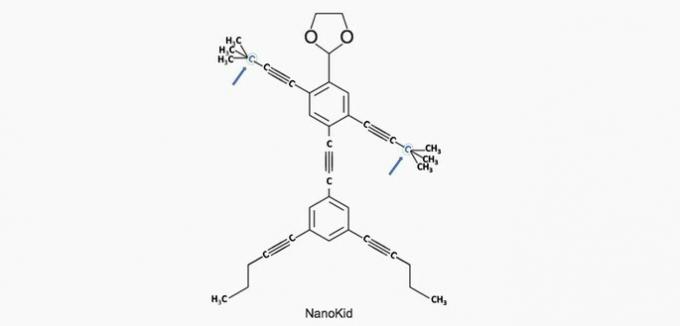
b) nepareizi. Galva sastāv no primārajiem oglekļiem.
c) nepareizi. Lāde sastāv no sekundārajiem un terciārajiem ogļiem.
d) nepareizi. Vēders sastāv no sekundāriem oglekļiem.
e) nepareizi. Kājas ir izgatavotas no primārajiem oglekļiem.
3. jautājums
(Enem / 2014) Dažus polimērmateriālus nevar izmantot arī noteiktu veidu artefaktu ražošanai mehānisko īpašību ierobežojumi, neatkarīgi no tā, cik viegli tie degradējas, radot tam nevēlamus blakusproduktus pieteikumu. Tādēļ pārbaude kļūst svarīga, lai noteiktu artefakta ražošanā izmantotā polimēra īpašības. Viena no iespējamām metodēm ir balstīta uz polimēra sadalīšanos, lai radītu monomērus, kas to izraisīja.
Artefakta radīta diamīna H kontrolēta sadalīšanās2N (CH2)6NH2 un HO skābes2C (CH2)4CO2H. Tāpēc artefakts tika izgatavots no
a) poliesters.
b) poliamīds.
c) polietilēns.
d) poliakrilāts.
e) polipropilēns.
Pareiza alternatīva: b) poliamīds.
a) nepareizi. Poliesteris veidojas reakcijā starp dikarboksilskābi (—COOH) un dialkolu (—OH).
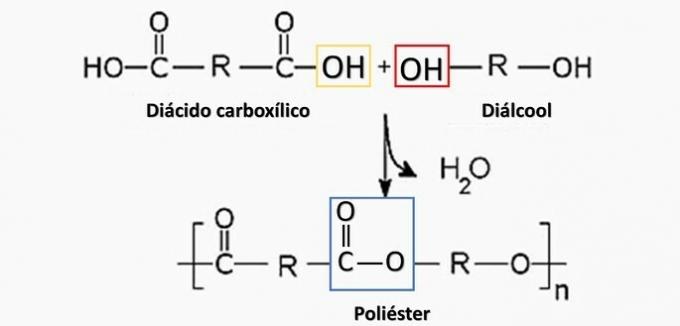
b) PAREIZI. Poliamīdu veido, polimerizējot dikarboksilskābi (–COOH) ar diamīnu (–NH2).
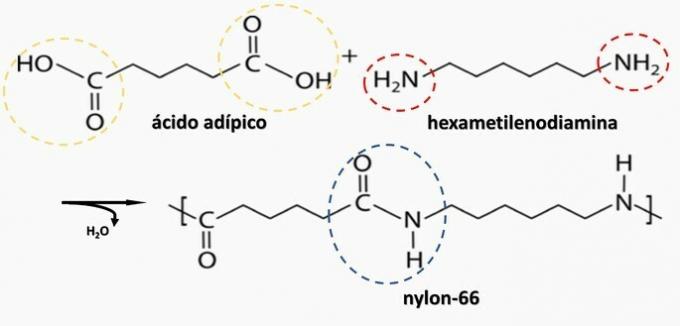
c) nepareizi. Polietilēns veidojas etilēna monomēra polimerizācijā.
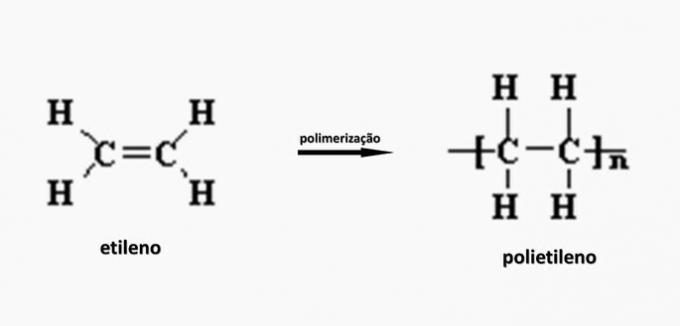
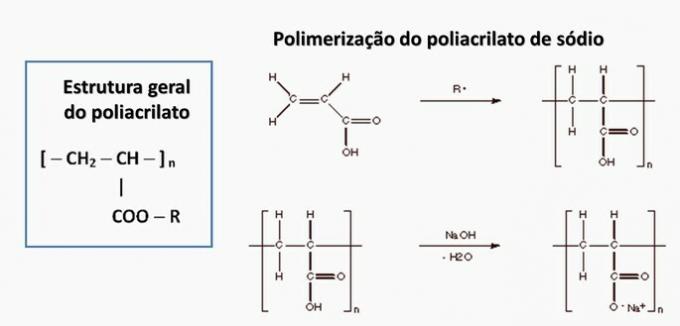
d) nepareizi. Poliakrilātu veido sāls, kas iegūts no karbonskābes.
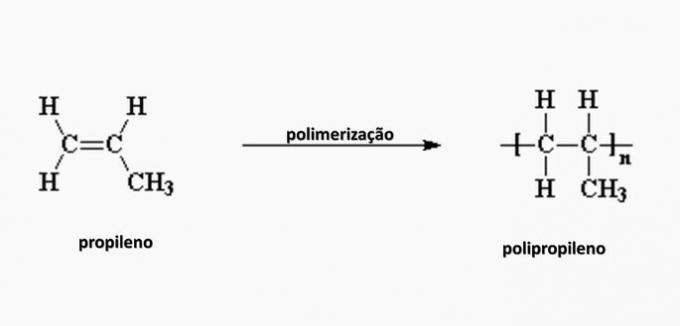
e) nepareizi. Polipropilēns veidojas propilēna monomēra polimerizācijā.
4. jautājums
(Enem / 2008) Ķīna ir apņēmusies kompensēt Krievijai nozares benzola noplūdi Ķīniešu naftas ķīmijas produkti Songhua upē, Amūras upes pietekā, kas veido robežu starp abiem valstīs. Krievijas Federālās ūdens resursu aģentūras prezidents apliecināja, ka benzols netiks sasniegts dzeramo ūdeni, bet lūdza iedzīvotājus uzvārīt tekošu ūdeni un izvairīties no makšķerēšanas Amūras upē un tās upēs pietekas. Vietējās varas iestādes uzglabā simtiem tonnu ogļu, jo minerālu uzskata par efektīvu benzola absorbētāju. Internets: (ar pielāgojumiem). Ņemot vērā pasākumus, kas pieņemti, lai mazinātu kaitējumu videi un iedzīvotājiem, ir pareizi to apgalvot
a) ogles, ievietotas ūdenī, reaģē ar benzolu, to novēršot.
b) benzols ir vairāk gaistošs nekā ūdens, un tāpēc to vajag vārīt.
c) orientācija, lai izvairītos no makšķerēšanas, ir saistīta ar nepieciešamību saglabāt zivis.
d) benzols nepiesārņotu dzeramā ūdens caurules, jo tas dabiski tiktu dekantēts upes dibenā.
e) Ķīnas rūpniecības benzola noplūdes radītais piesārņojums būtu ierobežots līdz Songhua upei.
Pareiza alternatīva: b) benzols ir gaistošāks par ūdeni, tāpēc ir nepieciešams to vārīt.
a) nepareizi. Akmeņogļu struktūra satur vairākas poras un tiek izmantota kā adsorbents, jo tā spēj mijiedarboties ar piesārņotājiem un noturēt tos uz virsmas, bet tos nenovērš.
b) PAREIZI. Jo lielāka ir vielas svārstīgums, jo vieglāk tā mainās gāzveida stāvoklī. Kamēr ūdens viršanas temperatūra ir 100 ° C, benzola - 80,1 ° C. Tas ir tāpēc, ka ūdens ir polārs savienojums un benzols ir nepolārs savienojums.
Mijiedarbības molekulu veids ir atšķirīgs, un tas ietekmē arī vielu viršanas temperatūru. Ūdens molekula spēj radīt ūdeņraža saites, kas ir daudz spēcīgāka mijiedarbība nekā tā, ko spēj veikt benzols ar inducēto dipolu.
c) nepareizi. Pārtikas ķēdē viena būtne kļūst par citas barību atbilstoši sugu mijiedarbībai kādā vietā. Kad toksiska viela tiek izlaista vidē, notiek pakāpeniska uzkrāšanās un zivis piesārņots, norijot cilvēku, var paņemt benzolu sev līdzi un izraisīt DNS mutācijas un pat pat vēzis.
d) nepareizi. Benzolam ir mazāks blīvums nekā ūdenim. Tādējādi tendence ir tāda, ka pat zem ūdens tas turpina izplatīties.
e) nepareizi. Sezonas izmaiņas var vēl vairāk palielināt problēmu, jo zemas temperatūras ietekmē saule vai baktērijas ietekmē samazinās ķīmisko vielu bioloģiskās sadalīšanās spējas.
5. jautājums
(Enem / 2019) Ogļūdeņraži ir organiskas molekulas ar virkni rūpniecisku pielietojumu. Piemēram, tie lielā daudzumā atrodas dažādās naftas frakcijās un parasti tiek atdalīti ar frakcionētu destilāciju, pamatojoties uz to viršanas temperatūru. Tabulā norādītas galvenās frakcijas, kas iegūtas, destilējot eļļu dažādos temperatūras diapazonos.
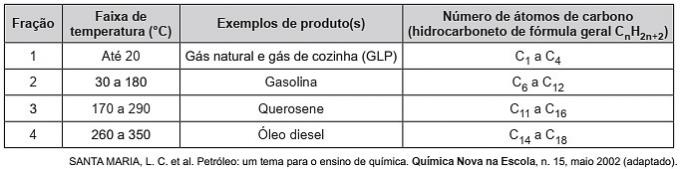
4. frakcijā savienojumu atdalīšana notiek augstākā temperatūrā, jo
a) to blīvums ir lielāks.
b) zaru skaits ir lielāks.
c) tā šķīdība eļļā ir lielāka.
d) starpmolekulārie spēki ir intensīvāki.
e) oglekļa ķēdi ir grūtāk pārtraukt.
Pareiza alternatīva: d) starpmolekulārie spēki ir intensīvāki.
Ogļūdeņraži mijiedarbojas ar inducētu dipolu, un šāda veida starpmolekulārais spēks tiek pastiprināts, palielinoties oglekļa ķēdei.
Tāpēc smagākajām naftas frakcijām ir augstāka viršanas temperatūra, jo ķēdes spēcīgāk mijiedarbojas ar inducētu dipolu.
Vairāk vingrinājumu ar komentētu izšķirtspēju skatiet arī:
- Vingrinājumi ogļūdeņražiem
- Organisko funkciju vingrinājumi
- Ķīmijas jautājumi Enem