Enem Sciences un tā tehnoloģiju pārbaude sastāv no 45 objektīvi jautājumi atbilžu varianti, kopā 100 punktu vērtībā. Tajā īpašas zināšanas par Bioloģija, fizika un ķīmija.
Zemāk skatiet to priekšmetu sarakstu un īsu kopsavilkumu par priekšmetiem, kas satur dažādāko saturu, kas visvairāk atbilst Dabaszinātņu un tā tehnoloģiju pārbaudei.
Bioloģija
Molekulas, šūnas un audi
- Šūna: Mazākā dzīvo būtņu vienotība ar noteiktām formām un funkcijām.
- šūnu teorija: Apgalvo, ka visas dzīvās būtnes veido šūnas.
- Šūnu organoīdi: Tie ir kā mazi orgāni, kas veic šūnām būtiskas darbības.
- Šūnas kodols: Kur atrodams organismu ģenētiskais materiāls (DNS) un tas atrodas eikariotu šūnās.
- šūnu dalīšanās: Process, kurā mātes šūna rada meitas šūnas.
- Vielmaiņa: Ķīmisko reakciju kopums, kas notiek šūnā un ļauj tai palikt dzīvam, augt un sadalīties.
- Olbaltumvielu sintēze: Olbaltumvielu ražošanas mehānisms.
- Histoloģija: Pētiet bioloģiskos audus, analizējot to struktūru, izcelsmi un diferenciāciju.
- Citoloģija: Bioloģijas nozare, kas pēta šūnas un to struktūras.
- Biotehnoloģija: Tehnoloģiju izmantošana dzīvo organismu radīšanai vai modificēšanai.
iedzimtība un dzīves daudzveidība
- Iedzimtība: Bioloģiskais mehānisms, kurā katras dzīvās būtnes īpašības tiek pārnestas no vienas paaudzes uz otru.
- Gēni un hromosomas: Gēni ir sīkas struktūras, kas sastāv no DNS. Savukārt šo struktūru kopums veido hromosomas.
- Mendela likumi: Tie ir pamatu kopums, kas izskaidro iedzimtas pārnešanas mehānismu paaudzēs.
- Ievads ģenētikā: Pamatjēdzieni bioloģijas jomā, kas pēta iedzimtības vai bioloģiskās mantošanas mehānismus.
- Ģenētiskā mainība: Attiecas uz gēnu atšķirībām starp indivīdiem populācijā.
- gēnu inženierija: Gēnu manipulācijas un rekombinācijas paņēmieni, kas pārveido, atjauno, reproducē un pat rada dzīvas būtnes.
- asins grupas: Vissvarīgākās ir ABO sistēma un Rh faktors.
- ABO sistēma un Rh koeficients: ABO sistēma cilvēka asinis klasificē četros esošajos veidos: A, B, AB un O. Savukārt Rh faktors ir antigēnu grupa, kas nosaka, vai asinīs ir pozitīvs vai negatīvs Rh.
Dzīvo būtņu identitāte
- dzīvo būtņu klasifikācija: Sistēma, kas organizē dzīvās būtnes kategorijās atbilstoši to kopīgajām īpašībām un evolucionārajām radniecības attiecībām.
- Vīruss: Tie ir infekcijas izraisītāji, mikroskopiski un acelulāri (tiem nav šūnu).
- prokariotu šūnas: Viņu iekšpusē nav kodola membrānas vai membrānas struktūru.
- eikariotu šūnas: Sastāv no plazmas membrānas, citoplazmas un kodola.
- Autotrofi un heterotrofi: Autotrofi ir dzīvas būtnes, kas fotosintēzes ceļā iegūst barības vielas un enerģiju, izmantojot saules gaismas priekšrocības, bet heterotrofi iegūst barības vielas un enerģiju, patērējot citas dzīvās būtnes.
- Filogēnija: Tā ir sugas ģenealoģiskā vēsture un tās hipotētiskās attiecības starp senčiem un pēcnācējiem.
- Embrioloģija: Izpētiet visus embrija attīstības posmus, sākot no apaugļošanās, zigotas veidošanās, līdz visi jaunās būtnes orgāni ir pilnībā izveidoti.
- Cilvēka anatomija: Pētiet ķermeņa struktūras, kā tās veidojas un kā tās darbojas kopā ķermenī (sistēmās).
- Fizioloģija: Pētījums par vairākām ķīmiskajām, fizikālajām un bioloģiskajām funkcijām, kas garantē organismu pareizu darbību.
Ekoloģija un vides zinātnes
- ekosistēma: Kopa, ko veido biotiskas kopienas un abiotiski faktori, kas mijiedarbojas noteiktā reģionā
- Brazīlijas ekosistēmas: Galvenās Brazīlijas ekosistēmas ir: Amazon, Caatinga, Cerrado, Atlantijas mežs, Mata dos Cocais, Pantanal, Araucaria mežs, Mangue un Pampas.
- Biotiskie un abiotiskie faktori: Vides fizikālie un ķīmiskie elementi (abiotiskie faktori) lielā mērā nosaka dzīvo kopienu struktūru un darbību (biotiskie faktori).
- Biotops un ekoloģiskā niša: Dzīvotne ir vieta, kur dzīvo dzīvnieks, un niša ir tā, kā viņš tur dzīvo.
- pārtikas tīkls: Pārtikas ķēžu kopums, kas saistīts ar ekosistēmu.
- Barības ķēde: Atbilst barošanās attiecībām, tas ir, barības vielu un enerģijas absorbcijai starp dzīvajām būtnēm.
- ekoloģiskās piramīdas: Tie ir grafiski attēlo trofisko mijiedarbību starp sugām kopienā.
- Bioģeoķīmiskie cikli: Attēlojiet ķīmisko elementu kustību starp dzīvām būtnēm un planētas atmosfēru, litosfēru un hidrosfēru.
- Pasaules biomiAtrakcijas: Ir septiņi galvenie: Tundra, Taiga, Mērens mežs, Tropu mežs, Savannas, Prērija un Tuksnesis.
- Brazīlijas bioms: Ir seši: Amazon, Cerrado, Caatinga, Atlantic Forest, Pantanal un Pampa.
- Dabas resursi: Tie ir dabas piedāvātie elementi, kurus cilvēks izmanto izdzīvošanai.
- Klimata izmaiņas: Vai visā pasaulē notiek klimata izmaiņas?
- siltumnīcas efekts un globālā sasilšana: Siltumnīcas efekts ir dabisks process, ko pastiprina cilvēka darbība un kas izraisa globālo sasilšanu.
Dzīves izcelsme un attīstība
- Dzīves izcelsme: Izskaidrots ar vairākām teorijām, kas izstrādātas, meklējot atbildes.
- Abioģenēze un bioģenēze: Divas teorijas, kas formulētas, lai izskaidrotu dzīvības izcelsmi uz Zemes.
- Kas ir Visums?: Atbilst visu esošo vielu un enerģijas kopumam.
- Lielā sprādziena teorija: Uzskata, ka Visums ir radies no vienas daļiņas - pirmatnējā atoma - eksplozijas, izraisot kosmisko kataklizmu.
- Evolūcija: Atbilst sugu modifikācijas un adaptācijas procesam laika gaitā.
- Cilvēka evolūcija: Atbilst pārmaiņu procesam, kas radīja cilvēkus un tos diferencēja kā sugu.
- Evolūcijas teorija: Pašreizējās sugas ir cēlušās no citām sugām, kuras laika gaitā ir mainījušās un nodod pēcnācējiem jaunas īpašības.
- Darvinisms: Tas ir pētījumu un teoriju kopums, kas saistīts ar sugu attīstību, kuru izstrādājis angļu dabaszinātnieks Čārlzs Darvins.
- Neodarvinisms: Tieši mūsdienu evolūcijas teorija balstās uz Čārlza Darvina evolūcijas pētījumiem kopā ar ģenētikas atklājumiem.
- Dabiskā izlase: Rodas sakarā ar izdzīvošanas nepieciešamību un sugu pielāgošanu videi.
Cilvēku dzīves kvalitāte
- Cilvēka attīstības indekss (HDI): Cilvēces attīstības novērtējums, pamatojoties uz informāciju par teritorijas dzīves kvalitāti un ekonomiku.
- Sociālā nevienlīdzība: Sociālā problēma, kurā pastāv iedzīvotāju dzīves līmeņa nesamērīgums.
- Iekšzemes kopprodukts (IKP): Veids, kā izmērīt produkciju noteiktā laika periodā.
- STS - seksuāli transmisīvās slimības: Tās ir slimības, kuras var pārnest no vienas personas uz otru seksuāla kontakta laikā.
- narkotikas: Tās ir vielas, kas maina ķermeņa funkcijas, kā arī cilvēku uzvedību
- Pusaudžu grūtniecība: Pēc PVO domām, tiek uzskatīta grūtniecība vecumā no 10 līdz 19 gadiem.
- Brazīlijas sociālās problēmas: Galvenie no tiem ir: bezdarbs, veselība, izglītība, mājokļi, vardarbība un piesārņojums.
- Fizisko aktivitāšu nozīme veselībai: Uzlabo dzīves kvalitāti un kopā ar sabalansētu uzturu rada veselīgu ķermeni, novēršot slimības.
- Veselīga ēšana: Pārtikas patēriņš ar daudzveidību, mērenību un līdzsvaru.
Bioloģijas jautājumi, kas iekrita Enem
1. (Enem / 2016) Eikariotu šūnu olbaltumvielās ir signāla peptīdi, kas ir sekvences aminoskābes, kas atbildīgas par to pievēršanos dažādiem organoīdiem, saskaņā ar to aminoskābēm funkcijas. Pētnieks ir izstrādājis nanodaļiņu, kas spēj proteīnus pārvadāt noteiktos šūnu tipos. Tagad viņš vēlas uzzināt, vai ar Krebsa ielādēta nanodaļiņa bloķē olbaltumvielu in vitro tas spēj veikt savu darbību vēža šūnā, spējot samazināt enerģijas piegādi un iznīcināt šīs šūnas.
Kurai organellai, izvēloties šo bloķējošo proteīnu nanodaļiņu ielādēšanai, jāņem vērā adresējošā signāla peptīds?
a) Kodols.
b) mitohondriji.
c) peroksisoma.
d) Golgiense komplekss.
e) Endoplazmatiskais tīklojums.
Pareiza alternatīva: b) mitohondriji.
Enerģijas iegūšana notiek, pārraujot molekulu saites.
Izmantojot aerobo elpošanu, tas ir, skābekļa klātbūtnē, glikozes saites tiek sadalītas trīs posmos:
- Glikolīze
- Krebsa cikls
- Oksidatīvā fosforilēšana
Pirmais solis notiek citozolā, bet pārējie divi - mitohondrijos.
Tādējādi mitohondrijiem ir funkcija veikt šūnu elpošanu, kas rada lielāko daļu enerģijas, kas tiek izmantota šūnu funkcijās.
Signālpeptīdam jābūt novirzītam uz mitohondrijiem, jo, bloķējot Krebsa ciklu, ir iespējams samazināt enerģijas padevi un iznīcināt šūnas.
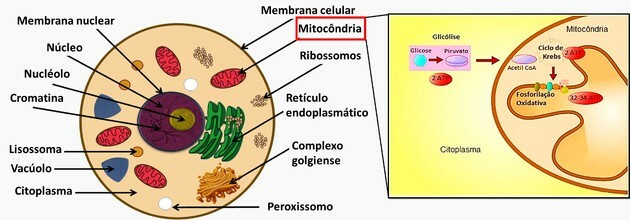
Citoplazma ir apjomīgs reģions, kas satur kodolu un šūnu organellus.
Kodols satur ģenētisko materiālu (DNS un RNS).
Organelles darbojas kā orgāni šūnās, un katrs no tiem veic noteiktu funkciju.
Pārējo organellu funkcijas, kas atrodas jautājuma alternatīvās, ir:
- Endoplazmatiskais tīklojums: gludā endoplazmatiskā tīklojuma funkcija ir ražot lipīdus, kas veidos šūnu membrānas, savukārt raupjam endoplazmas retikulam ir sintēzes funkcija olbaltumvielas.
- Golgi komplekss: golgi kompleksa galvenās funkcijas ir pārveidot, uzglabāt un eksportēt rupjā endoplazmatiskajā tīklā sintezētos proteīnus.
- Peroksisomas: funkcija ir taukskābju oksidēšana holesterīna sintēzei un šūnu elpošanai.
2. (Enem / 2017) Pelēkie delfīni (Sotalia guianensis), delfīnu dzimtas zīdītāji, ir lieliski piesārņojuma rādītāji apgabalos, kuros viņi dzīvo, jo viņi visu savu dzīvi - apmēram 30 gadus - pavada tajā pašā reģionā. Turklāt suga savā ķermenī uzkrāj vairāk piesārņotāju, piemēram, dzīvsudrabu, nekā citi dzīvnieki barības ķēdē.
MARCOLINO, B. Jūras sargi. Pieejams: http://cienciahoje.uol.com.br. Piekļuve: 1. augusts 2012. gads (pielāgots).
Pelēkajos delfīnos uzkrājas lielāka šo vielu koncentrācija, jo:
a) ir zālēdāji dzīvnieki.
b) ir nelabvēlīgi dzīvnieki.
c) ir lieli dzīvnieki.
d) sagremot pārtiku lēnām.
e) atrodas pārtikas ķēdes augšdaļā.
Pareiza alternatīva: e) ir pārtikas aprites augšdaļā.
Ir iespējams uzzināt par ekosistēmu, kurā dzīvo pelēkie delfīni, jo šie dzīvnieki savu dzīvi pavada tajā pašā reģionā. Tādēļ jebkuras izmaiņas, kuras var novērot šiem dzīvniekiem, rodas no izmaiņām viņu dzīves vietā.
Pārtikas ķēdē viena būtne kļūst par citas barību, parādot sugu mijiedarbību kādā vietā.
Pārtikas ķēdes sastāvdaļas tiek ievietotas trofiskos līmeņos, kas atbilst uzturvielu uzsūkšanās un enerģijas iegūšanas kārtībai starp dzīvajām būtnēm.
Ekosistēmā, kurā dzīvo cūkdelfīns, tas tiek ievietots pārtikas ķēdes augšdaļā.
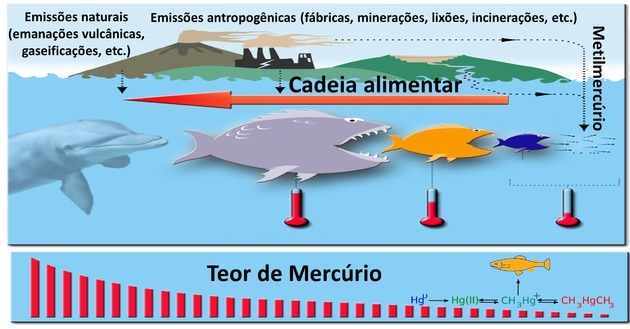
Kad delfīns barojas, dzīvnieki, kas atrodas iepriekšējā trofiskajā līmenī, jau ir absorbējuši vairākus citus organismus.
Smagie metāli, piemēram, dzīvsudrabs, nav bioloģiski noārdāmi un ir sastopami rūpnieciskajā darbībā, vulkānos, elektronisko atkritumu un raktuvēs.
Bioakumulācija notiek, kad šīs toksiskās vielas pakāpeniski uzkrājas trofiskajā līmenī. Tādējādi visaugstākais dzīvsudraba saturs tiks atrasts visattālākajos trofiskajos līmeņos.
Šī metāla koncentrācija delfīnu plēsējā būs lielāka nekā tā laupījumā, piemēram, zivīs, garnelēs un kalmāros.
Lai gan tie ir lieli dzīvnieki, tas neattaisno bioakumulāciju un lēna gremošana netraucē, jo dzīvsudrabs nav bioloģiski noārdāms.
Zālēdāji dzīvnieki patērē autotrofiskas būtnes, piemēram, aļģes, savukārt detektīvēdāji barojas ar organiskajiem atkritumiem.
Skatīt arī:Bioloģija Enem.
3. (Enem / 2017) Atlantijas mežam raksturīga liela epifītu daudzveidība, piemēram, bromeliādes. Šie augi ir pielāgoti šai ekosistēmai un spēj uztvert gaismu, ūdeni un barības vielas pat dzīvojot uz kokiem.
Pieejams: www.ib.usp.br. Piekļuve: 23. februāris 2013 (pielāgots).
Šīs sugas uztver ūdeni no (a)
a) kaimiņu augu organisms.
b) augsne caur tās garajām saknēm.
c) lietus uzkrājas starp tās lapām.
d) saimniekaugu neapstrādātas sulas.
e) kopiena, kas dzīvo tās interjerā.
Pareiza alternatīva: c) starp lapām uzkrājas lietus.
Ekoloģiskās attiecības parāda attiecības starp dzīvajām būtnēm un vidi, kurā viņi dzīvo, nosakot, kā viņi izdzīvo un vairojas.
Epifītisms ir harmoniskas ekoloģiskas attiecības starp divām sugām, kur tāda suga kā bromeliāde izmanto kokus, lai iegūtu patvērumu, nekaitējot tam.
Tā kā tiem ir dažādi izmēri, bromeliādes atrod aizsardzību uz lielāku koku virsmām, nostiprinot saknes uz saimniekkoku.
Lapu forma ļauj uzkrāties lietus ūdenim, un mikro svari veicina ūdens un barības vielu uzsūkšanos.
Bromeliadu saknes tiek izmantotas tikai, lai piesaistītos augiem, tādējādi izveidojot īrnieku attiecības, kurās epifīts gūst labumu, bet nekaitē kokam.
Lai iegūtu vairāk jautājumu par Enology bioloģiju, mēs esam sagatavojuši šo sarakstu: Bioloģijas jautājumi Enem.
Fizika
enerģija, darbs un spēks
- darbs fizikā: Enerģijas pārnešana spēka iedarbības dēļ.
- Enerģija: Pārstāv spēju radīt darbu.
- Enerģijas veidi: Mehāniskā, termiskā, elektriskā, ķīmiskā un kodolenerģija.
- Kinētiskā enerģija: Enerģija, kas saistīta ar ķermeņu kustību.
- Potenciālā enerģija: Enerģija, kas saistīta ar ķermeņu stāvokli.
- Spēks: Darbība, kas izdarīta uz ķermeni, kas spēj mainīt atpūtas stāvokli vai mainīt kustību apjomu.
- Elektroenerģija: Cik ātri tiek veikts darbs.
- Elektriskais potenciāls: Elektriskā spēka darbs ar elektrificētu lādiņu, pārvietojoties starp punktu attiecībā pret atskaites punktu.
- Fizikas formulas: Attiecības starp lielumiem, kas saistīti ar vienu un to pašu fizisko parādību.
Mehānika, kustību pētījumi un Ņūtona likumu pielietojumi
- Kustības daudzums: Vektora daudzums, kas definēts kā ķermeņa masas un tā ātruma reizinājums.
- vienveidīga kustība: Atspoguļo ķermeņa nobīdi no noteikta atsauces rāmja ar nemainīgu ātrumu.
- vienmērīgi daudzveidīga kustība: Ātrums laika gaitā ir nemainīgs un ir nulle.
- Vienveidīga taisnvirziena kustība: Ķermenis atrodas nemainīgā ātrumā, tomēr ķermeņa virzītā trajektorija ir taisnā līnijā.
- Vienmērīgi daudzveidīga taisnvirziena kustība: To veic taisnā līnijā, un ātruma izmaiņas vienmēr notiek vienādos laika intervālos.
- Ņūtona likumi: Pamatprincipi, ko izmanto, lai analizētu ķermeņu kustību.
- Smagums: Fundamentāls spēks, kas regulē objektus miera stāvoklī.
- Inerce: Matērijas īpašība, kas norāda uz izturību pret izmaiņām.
Viļņu parādības un viļņi
- viļņi: Traucējumi, kas izplatās kosmosā, nenododot vielu, tikai enerģiju.
- mehāniskie viļņi: Traucējumi, kas pārvieto kinētisko un potenciālo enerģiju caur materiālu barotni.
- Elektromagnētiskie viļņi: Elektrisko un magnētisko enerģijas avotu izdalīšanās rezultāti kopā.
- Skaņas viļņi: Šīs ir vibrācijas, kas rada dzirdes sajūtas, kad tās iekļūst mūsu ausī.
- gravitācijas viļņi: Tie ir viļņi laiktelpas izliekumā, kas izplatās telpā.
Elektriskās un magnētiskās parādības
- Elektrība: Fizikas joma, kas pēta parādības, kuras izraisa elektrisko lādiņu darbs.
- elektrostatika: Pētiet elektriskos lādiņus bez kustības, ti, miera stāvoklī.
- Elektrodinamika: Pētiet elektrības dinamisko aspektu, tas ir, elektrisko lādiņu pastāvīgu kustību.
- Elektromagnētisms: Pēta attiecības starp elektrības spēkiem un magnētismu kā unikālu parādību.
- Elektrifikācijas procesi: Metodes, kurās ķermenis vairs nav elektriski neitrāls un kļūst pozitīvi vai negatīvi uzlādēts.
- Ohma likumi: Nosakiet vadītāju elektrisko pretestību.
- Kirhofa likumi: Nosakiet strāvu stiprumu elektriskajās ķēdēs, kuras nevar samazināt līdz vienkāršām shēmām.
Siltuma un siltuma parādības
- siltums un temperatūra: Siltums apzīmē enerģijas apmaiņu starp ķermeņiem, savukārt temperatūra raksturo molekulu uzbudinājumu ķermenī.
- siltuma izplatīšanās: Siltuma pārnešana, kas var notikt vadīšanas, konvekcijas vai starojuma ietekmē.
- termometriskās svari: Tos izmanto, lai norādītu temperatūru, tas ir, kinētisko enerģiju, kas saistīta ar molekulu kustību.
- Kalorimetrija: Pēta parādības, kas saistītas ar siltumenerģijas apmaiņu.
- īpašs karstums: Fiziskais daudzums, kas saistīts ar saņemtā siltuma daudzumu un tā siltuma izmaiņām.
- saprātīgs karstums: Fiziskais lielums, kas saistīts ar ķermeņa temperatūras izmaiņām.
- latentais karstums: Fiziskais daudzums, kas apzīmē ķermeņa saņemto vai piešķirto siltuma daudzumu, mainoties tā fiziskajam stāvoklim.
- siltuma jauda: Daudzums, kas atbilst siltuma daudzumam, kas atrodas ķermenī, attiecībā pret temperatūras svārstībām, ko tas cieš.
- Termodinamika: Fizikas joma, kas pēta enerģijas pārneses.
Optika, optiskās parādības, gaismas laušana
- Gaisma: Elektromagnētiskais vilnis, kas jutīgs pret neapbruņotu aci.
- gaismas refrakcija: Optiska parādība, kas rodas, ja gaisma izmainās izplatīšanās vidē.
- gaismas atstarošana: Gaismas parādīšanās optiskā parādība uz atstarojošās virsmas, atgriežoties sākuma punktā.
- Gaismas ātrums: Ātrums, ar kādu gaisma pārvietojas vakuumā un izplatās dažādos vidēs.
Hidrostatika
- Hidrostatika: Šķidruma īpašības, piemēram, hidrostatiskais spiediens, blīvums un peldošais spēks.
- hidrostatiskais spiediens: Koncepcija un formulas hidrostatiskā spiediena un kopējā spiediena aprēķināšanai.
- Stevina teorēma: Atmosfēras un šķidruma spiediena izmaiņu saistība.
- Arhimēda teorēma: Rezultātā iegūtā spēka, ko šķidrums iedarbojas uz konkrēto ķermeni, aprēķins (peldspējas teorēma).
Fizikas jautājumi, kas iekrita Enem
1. (Enem / 2017) Drošinātājs ir pārslodzes aizsardzības ierīce ķēdēs. Kad strāva, kas iet caur šo elektrisko komponentu, ir lielāka par tā maksimālo nominālo strāvu, drošinātājs izdeg. Tādā veidā tas novērš lielo strāvu no ķēdes ierīču bojāšanas. Pieņemsim, ka parādīto elektrisko ķēdi darbina sprieguma avots U un ka drošinātājs atbalsta nominālo strāvu 500 mA.
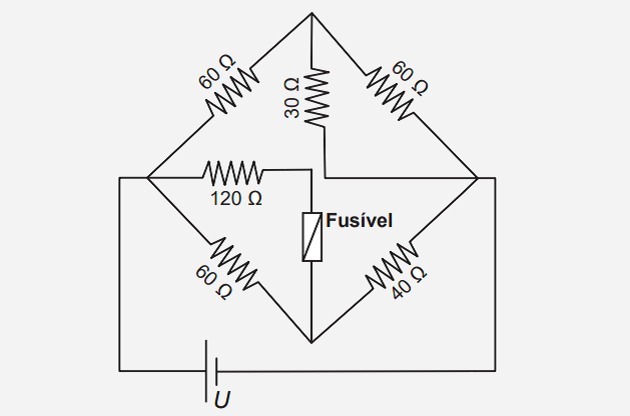
Kāda ir maksimālā sprieguma vērtība U tātad drošinātājs neizdegas?
a) 20 V
b) 40 V
c) 60 V
d) 120 V
e) 185 V
Pareiza alternatīva: d) 120 V
Jautājumā piedāvāto shēmu veido jaukta rezistoru apvienība. Mēs arī zinām, ka maksimālā drošinātāja atbalstītā strāva ir 500 mA (0,5 A).
Lai uzzinātu akumulatora sprieguma maksimālo vērtību, mēs varam izolēt ķēdes daļu, kurā atrodas drošinātājs, kā parādīts zemāk redzamajā attēlā.
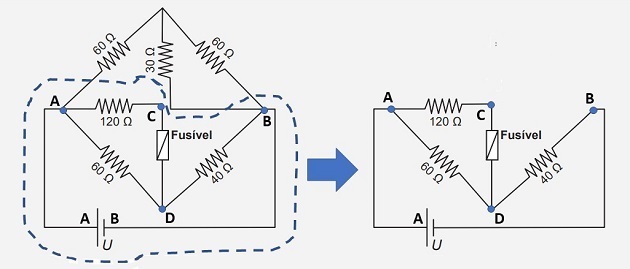
Tas ir iespējams, jo ķēdes “augšējā” daļa tiek pakļauta tādam pašam spriegumam kā “apakšējā” daļa (attēlā iezīmētā daļa), jo tās spailes ir savienotas ar tiem pašiem punktiem (A un B).
Sāksim ar sprieguma vērtības atrašanu pie 120 rezistora spailēm. Strāva, kas iet caur šo rezistoru (t.i.1) ir tas pats, kas iet caur drošinātāju. Tāpēc mums ir:
UBC= 0,5 120 = 60 V
Tas būs tāds pats spriegums kā 60 rezistora spailēm. tiek pakļauti, jo tas ir savienots paralēli 120 rezistoram.
.
Tādējādi mēs varam atrast pašreizējo vērtību (t.i.2), kas iet caur šo rezistoru:
Pašreizējais i3 kas šķērso 40 rezistoru ir vienāds ar summu i1 Hei2, t.i.
i3 = 1 + 0,5 = 1,5 A
Zinot šo vērtību, mēs varam aprēķināt sprieguma vērtību rezistora spailēs 40 :
Udb= 1,5,40 = 60 V
Tādējādi ķēdes spriegums būs vienāds ar U summuBC ar Tevidb, tas ir:
U = 60 + 60 = 120 V
2. (Enem / 2017) Dažās mājās tiek izmantoti elektrificēti žogi, lai novērstu iespējamos iebrucējus. Elektrificēts žogs darbojas ar elektriskā potenciāla starpību aptuveni 10 000 V. Lai nebūtu letāls, strāva, ko var pārraidīt caur cilvēku, nedrīkst būt lielāka par 0,01 A. Ķermeņa elektriskā pretestība starp cilvēka rokām un kājām ir aptuveni 1 000 1.
Lai strāva nebūtu letāla personai, kura pieskaras elektrificētajam žogam, sprieguma ģeneratoram jābūt iekšējai pretestībai, kas attiecībā pret cilvēka ķermeņa pretestību ir
a) praktiski nulle.
b) aptuveni vienāds.
c) tūkstošiem reižu lielāks.
d) par kārtību, kas ir 10 reizes lielāka.
e) skriet 10 reizes mazāk.
Pareiza alternatīva: c) tūkstošiem reižu lielāka.
Lai atrisinātu šo problēmu, mums jāsalīdzina ģeneratora iekšējā pretestība ar cilvēka ķermeņa pretestību. Šim nolūkam mēs izmantosim šādus vienādojumus:
(ģeneratora vienādojums)
U = R.i (Ohma likums)
Ņemiet vērā, ka r ir ģeneratora iekšējā pretestība un R ir vienāda ar ķermeņa pretestību. Vienādojot abus vienādojumus un aizstājot vērtības, mums ir:
Tagad mums jānoskaidro, cik reizes ģeneratora iekšējai pretestībai jābūt lielākai par ķermeņa pretestību. Šim nolūkam dalīsim viens otru, tas ir:
Tāpēc ģeneratora iekšējai pretestībai vajadzētu būt aptuveni 1000 reizes lielākai par cilvēka ķermeņa pretestību.
3. (Enem / 2017) Autovadītājs, kurš atbild uz mobilā tālruņa zvanu, tiek novirzīts uz neuzmanību, palielinot negadījumu iespējamību reakcijas laika palielināšanās dēļ. Apsveriet divus autovadītājus, no kuriem pirmais ir uzmanīgs, bet otrs - braucot ar mobilo tālruni. Viņi sākotnēji paātrina savas automašīnas līdz 1,00 m / s2. Reaģējot uz ārkārtas situāciju, viņi bremzē ar palēninājumu, kas vienāds ar 5,00 m / s2. Uzmanīgais vadītājs bremzi iedarbina ar ātrumu 14,0 m / s, savukārt neuzmanīgajam vadītājam līdzīgā situācijā bremzēšanas sākšana prasa 1,00 sekundes ilgāk.
Cik tālu neuzmanīgs vadītājs brauc vairāk nekā uzmanīgs vadītājs, līdz automašīnas pilnībā apstājas?
a) 2,90 m
b) 14,0 m
c) 14,5 m
d) 15,0 m
e) 17,4 m
Pareiza alternatīva: e) 17,4 m
Atrodīsim 1. braucēja veikto attālumu, izmantojot Torricelli vienādojumu, tas ir:
v2 = v02 + Pirmdienas
Pirmās automašīnas sākotnējais ātrums ir vienāds ar 14 m / s, tā galīgais ātrums ir vienāds ar nulli, jo automašīna ir apstājusies un tās paātrinājums ir vienāds ar - 5 m / s2. Aizstājot šīs vērtības vienādojumā, mums ir:
Tagad aplūkosim 2. braucēja situāciju. Tā kā pirms bremzes nospiešanas bija nepieciešams 1 s ilgāk, šajā laika intervālā veikto attālumu var atrast, izmantojot vienādojumu:
v = v0 + pie
Ņemot vērā, ka tā paātrinājums bija 1 m / s2 un tā sākotnējais ātrums bija arī 14 m / s, mēs atradām:
v = 14 + 1,1 ⇒ v2 = 15 m / s
Lai atrastu šajā laika intervālā veikto attālumu, izmantosim Torricelli vienādojumu:
Pieliekot bremzi, tā ātrums bija vienāds ar 15 m / s, bet paātrinājums bija vienāds ar -5 m / s2. Lai atrastu nobraukto attālumu līdz apstāšanās brīdim, mēs atkal izmantosim Torricelli vienādojumu:
2. automašīnas kopējais nobrauktais attālums būs vienāds ar:
plkst2 = Δs '+ Δs "
plkst2 = 14,5 + 22,5
plkst2 = 37,0 m
Lai uzzinātu attālumu, kuru neuzmanīgs vadītājs ir veicis visvairāk, vienkārši rīkojieties šādi:
37,0 - 19,6 = 17,4 m
Skatīt arī:Fizika Enem.
Ķīmija
ķīmiskās pārvērtības
- ķīmiskās pārvērtības: Darbības, kuru rezultātā veidojas jaunas vielas
- Ķīmiskās saites: Savienojumi starp viena un tā paša elementa atomiem.
- Ķīmiskās reakcijas: Atomu pārkārtošana, veidojot jaunas vielas.
- Ķīmiskais līdzsvars: Parādība, kas notiek atgriezeniskās ķīmiskās reakcijās, kad tiešās un apgrieztās reakcijas ātrums ir vienāds.
- Atomu modeļi: Viņi apvieno Daltona, Tomsona, Rezerforda un Bora atomu modeļus.
- atomu struktūra: Sastāv no trim pamatdaļiņām: protoniem (ar pozitīvu lādiņu), neitroniem (neitrālām daļiņām) un elektroniem (ar negatīvu lādiņu).
- Ķīmiskie elementi: Matērijas pamatelements, ko veido atomu grupa ar tādu pašu atomu skaitu.
- Periodiskā tabula: Ķīmisko elementu klasifikācija augošā atomu skaita secībā.
- Stehiometriskie aprēķini: Ķīmiskā reakcijā patērēto un veidoto vielu sastāva kvantitatīva analīze.
Materiāli, to īpašības un pielietojums
- matērijas īpašības: Materiālu fizikālās vai ķīmiskās īpašības.
- matērijas fiziskie stāvokļi: Ciets, šķidrs, gāzes, plazmas un Bose-Einšteina kondensāts.
- Fiziskā stāvokļa izmaiņas: Ir kondensācija vai sašķidrināšana, sacietēšana, saplūšana, iztvaikošana un sublimācija.
- jonu, katjonu un anjonu: Jons ir elektriski uzlādēta ķīmiska viela. Katjonam ir pozitīvs lādiņš, anjonam - negatīvs lādiņš.
- starpmolekulārie spēki: Vai spēki tiek veikti, lai noturētu divas vai vairākas molekulas kopā.
- Molekula: Tā ir stabila divu vai vairāku identisku vai dažādu atomu grupa, kas savienota ar kovalentu saišu starpniecību.
- Molekulārā ģeometrija: Tas ir veids, kas parāda, kā atomi sakārtojas molekulā.
- molekulārā formula: Tā ir molekulas sastāvdaļu ķīmisko simbolu un indeksu izpausme.
- strukturālā formula: Atspoguļo to, kā atomi saista kopā.
Ūdens
- Ūdens: Viens no vissvarīgākajiem cilvēces dabas resursiem. To veido viens skābekļa atoms un divi ūdeņraža atomi.
- ūdens īpašības: Tas ir lielisks šķīdinātājs, jo tas spēj izšķīdināt milzīgu daudzumu vielu.
- ūdens blīvums: Tas ir 1 g / cm3 (tas rakstīts: viens grams uz kubikcentimetru). Šī vērtība atbilst ūdenim 25 ° C temperatūrā.
- ūdens nozīme: Ūdens ir planētas dzīvības avots. Šajā ziņā, ja trūkst ūdens, tiek apdraudēta dzīvība.
- Ūdens fizikālie stāvokļi: Dabā tas ir sastopams trīs fizikālos stāvokļos: šķidrā, cietajā un gāzveida.
ķīmiskie šķīdumi
- ķīmiskie šķīdumi: Tie ir viendabīgi maisījumi, ko veido divas vai vairākas vielas.
- Koloidālie šķīdumi: Tie ir maisījumi, kas rada homogēna maisījuma izskatu, jo izkliedēto daļiņu lielums ir no 1 līdz 100 nm.
- Šķīdība: Vielu fizikālā īpašība ir izšķīst vai nešķīst noteiktā šķidrumā.
- Risinājumu koncentrācija: Atbilst izšķīdušās vielas daudzumam noteiktā šķīdinātāja daudzumā.
- Šķīdumu atšķaidīšana: Tas sastāv no šķīdinātāja pievienošanas šķīdumam, nemainot izšķīdušās vielas daudzumu.
Savienojumi un ķīmiskās vielas
- Skābes: Tās ir vielas, kas ūdens šķīdumā atbrīvo pozitīvos ūdeņraža jonus vai protonus.
- Bāzes: Tās ir vielas, kas veidojas savienojot katjonu un anjonu, un kas atbrīvo hidroksiljonus (OH anjonus–) ūdens šķīdumā.
- sāļi: Sāļi ir skābes un bāzes reakcijas rezultāts.
- Oksīdi: Tie ir binārie jonu vai molekulārie savienojumi, kur skābekļa molekulas ir saistītas ar citiem elementiem.
Ķīmiskās pārvērtības un enerģija
- Termoķīmija: Tā ir ķīmijas daļa, kas pēta siltuma (enerģijas) daudzuma iesaistīšanos ķīmiskajās reakcijās.
- Endotermiskas un eksotermiskas reakcijas: Ķīmisko reakciju laikā absorbētā vai izdalītā siltuma daudzums.
- entalpija: Tā ir enerģija, kas tiek apmainīta enerģijas absorbcijas un atbrīvošanās reakcijās.
- Hesa likums: Entalpijas izmaiņas (ΔH) ķīmiskā reakcijā ir atkarīgas tikai no reakcijas sākuma un beigu stāvokļiem, neatkarīgi no reakciju skaita.
- Elektroķīmija: Tā ir ķīmijas joma, kas pēta reakcijas, kas saistītas ar elektronu pārnesi un ķīmiskās enerģijas savstarpēju pārveidošanu elektriskajā enerģijā.
- Elektrolīze: Spontāna ķīmiskā reakcija, kas ietver oksidēšanās-reducēšanās reakciju, ko izraisa elektriskā strāva.
- Faradejas likums: Kad notiek ķēdes magnētiskās plūsmas variācijas, tajā rodas inducēts elektromotors.
- Radioaktivitāte: Kodolenerģijas parādība, kas rodas no atomiem izdalītās enerģijas, ko izraisa ķīmisko elementu sadalīšanās vai nestabilitāte.
- Kodola skaldīšana: Tas ir nestabila atoma kodola sadalīšanas process citos stabilākos kodolos.
- Kodolsintēze: Tas ir atomu savienojums, kam ir gaismas kodoli. Šo atomu savienošanās rezultātā rodas atoms ar smagāku kodolu.
oglekļa savienojumi
- Organiskā ķīmija: Ķīmijas nozare, kas pēta oglekļa savienojumus, kurus veido oglekļa atomi.
- Organiskās funkcijas: Organisko savienojumu grupu ar līdzīgām īpašībām klasifikācija.
- oglekļa ķēdes: Organisko savienojumu struktūra atbilstoši atomu un saišu izvietojumam.
- Ogļūdeņraži: Oglekļa un ūdeņraža savienojumi ar vispārējo formulu CxHy.
- Neorganiskā ķīmija: Ķīmijas nozare, kas pēta vielas, kuras veido ķīmiskie elementi, izņemot oglekli.
- Neorganiskās funkcijas: Neorganisko savienojumu grupas, kurām ir līdzīgas īpašības.
Ķīmijas attiecības ar tehnoloģijām, sabiedrību un vidi
- Piesārņojums: Vielu vai enerģijas nejauša vai tīša ievadīšana vidē, kas negatīvi ietekmē dzīvās būtnes.
- Piesārņojuma veidi: Veidi ir atkarīgi no ietekmētā resursa un radīto atkritumu veida, no kuriem galvenie ir: gaiss, augsne, ūdens, termiskais, skaņas, gaismas, vizuālais un radioaktīvais.
- Ozona slānis: Tā ir ozona gāzes sega, kas atrodas stratosfērā, kas aizsargā planētu no dzīvajām būtnēm kaitīgā ultravioletā starojuma.
- rūpnieciskie atkritumi: Tas nāk no procesiem, kas izstrādāti nozarēs, tas ir, no sekundārā sektora.
Ķīmiskās enerģijas ikdienas dzīvē
- Nafta: Dabiska viela, kas sastāv no vairākiem organiskiem komponentiem, īpaši ogļūdeņražiem.
- Dabasgāze: Tās cēlonis ir organisko vielu noārdīšanās, pazemes nogulumos, kas sajaukti vai nav sajaukti ar eļļu. Tas sastāv no metāna, lielākā daudzumā, un citu alkānu maisījuma papildus CO2, H2Y un N2.
- Minerālu ogles: Tas ir neatjaunojams dabas resurss, kuru izcelsme ir augu atliekas miljoniem gadu.
- Fosilais kurināmais: Tie ir neatjaunojami dabas resursi, kuru izcelsme ir organiski gruži, kas miljoniem gadu laikā uzkrāti zemes garozā.
- biomasa: Visas augu vai dzīvnieku izcelsmes organiskās vielas, ko izmanto enerģijas ražošanā.
- Biodegviela: Tas ir viss materiāls, ko izmanto enerģijas ražošanai no organiskās biomasas.
- Atjaunojamā enerģija: Tā ir enerģija, kas iegūta no avotiem, kas atjaunojas spontāni vai ar adekvātu cilvēka iejaukšanos.
Ķīmijas jautājumi, kas iekrita Enem
1. (Enem / 2016) 2003. gada vidū Brazīlijā nomira vairāk nekā 20 cilvēki, uzņemot bārija sulfāta suspensiju, ko radioloģiskajos izmeklējumos izmantoja kā kontrastu. Bārija sulfāts ir ļoti slikti šķīstoša cietviela, kas nešķīst pat skābju klātbūtnē. Nāves gadījumi notika tāpēc, ka farmācijas laboratorija piegādāja produktu, kas bija piesārņots ar bārija karbonātu, kas šķīst skābā vidē. Vienkāršs tests, lai pārbaudītu šķīstošos bārija jonus, varēja novērst traģēdiju. Šis tests sastāv no parauga apstrādes ar HCl ūdens šķīdumu un pēc filtrēšanas, lai atdalītu nešķīstošos bārija savienojumus, pievieno H ūdens šķīdumu.2TIKAI4 uz filtrāta un novēro 30 minūtes.
TURBINO, M.; SIMONI, J. A. Pārdomājot Celobar® lietu. Jaunā ķīmija, Nr. 2, 2007 (pielāgots).
Šķīstošo bārija jonu klātbūtni paraugā norāda ar
a) siltuma izdalīšanās.
b) krāsas maiņa uz rozā.
c) baltas cietas vielas nogulsnēšanās.
d) slāpekļa gāzes veidošanās.
e) hlora gāzes iztvaikošana.
Pareiza alternatīva: c) baltas cietas vielas nogulsnēšanās.
Bārija sulfāts, ko eksāmenos izmanto kā kontrastu, pateicoties tā zemajai šķīdībai, izdalās organismā. Bārija karbonātam ir paaugstināta šķīdība skābā vidē.
Mūsu organisms ražo kuņģa sulu, lai uzturētu kuņģa skābumu un veicinātu fermentu darbību gremošanā.
Ķermenī esošā skābe ir sālsskābe, kas palielina bārija karbonāta šķīdību un līdz ar to tā nāvi bārija jonu absorbcijas dēļ.
1. solis: nosaka tekstā minēto savienojumu formulas.
| Savienojums | Katijons | anjons | Formula |
| Bārija sulfāts | Ba2+ | TIKAI42- | BASO4 |
| bārija karbonāts | Ba2+ | CO32- | Liesa3 |
2. solis: dubultas apmaiņas reakcija ar HCl.
Šāda veida reakcijās, kad divi savienojumi reaģē savā starpā, tie apmainās ar elementiem vai radikāļiem šādi:
Šajā posmā vienīgais, kas reaģē ar skābi, ir bārija karbonāts.
Ogļskābe ir vāja un nestabila skābe, kas veidojas, atšķaidot oglekļa dioksīdu ūdenī.
Divkāršās apmaiņas reakcija ar sālsskābi ir šāda:
Tāpēc var izdalīties oglekļa dioksīds.
3. solis: dubultas apmaiņas reakcija ar H2TIKAI4.
Veicot filtrēšanu, filtrā paliek bārija sulfāts, kas nav reaģējis, un šķīstošo bārija hlorīda sāli filtrē.
Pievienojot sērskābi šķīdumam, notiek reakcija:
Sākotnējais šķīdums norāda uz bārija karbonāta klātbūtni, jo testa laikā izveidojās bārija sulfāts - baltas nogulsnes.
Skatīt arī:Ķīmija Enem.
2. (Enem / 2017) Galvenais pagrieziena punkts mūsdienu lauksaimniecības vēsturē notika pēc Otrā pasaules kara. Pēc kara valdības bija saskārušās ar milzīgu amonija nitrāta pārpalikumu - sastāvdaļu, ko izmanto sprāgstvielu ražošanā. No turienes munīcijas rūpnīcas tika pielāgotas, lai sāktu ražot mēslošanas līdzekļus, kuru galvenā sastāvdaļa ir nitrāti.
SOUZA, F.. Dabiskā / organiskā lauksaimniecība kā līdzeklis slāpekļa bioloģiskai fiksēšanai un uzturēšanai augsnē: ilgtspējīgs CDM modelis. Pieejams: www.planetaorganico.com.br. Piekļuve: 17. jūlijā 2015. gads (pielāgots).
Dabiskā slāpekļa ciklā šo rūpniecisko mēslošanas līdzekļu galvenās sastāvdaļas ekvivalents tiek iegūts
a) nitrēšana.
b) nitrozēšana.
c) amonifikācija.
d) denitrifikācija.
e) N bioloģiskā fiksācija2.
Pareiza alternatīva: a) nitrēšana.
Slāpeklis ir gāze, kas atrodas gaisā lielos daudzumos.
N2 atmosfēras atmosfēra ir ļoti stabila trīskāršās saites dēļ, kas saista nitrogēnus, un tāpēc tā nav ķīmiski reaktīva.
Slāpeklis ir ļoti svarīgs dzīvajām būtnēm, jo tas ir daļa no bioķīmiskajiem savienojumiem, piemēram, aminoskābēm un nukleīnskābēm, ko iegūst ar pārtiku.
Augsnē un pākšaugu saknēs esošās baktērijas spēj fiksēt slāpekli ciklā, kurā notiek vielas un enerģijas plūsma.
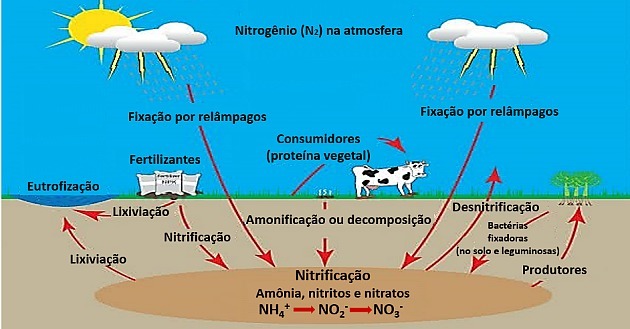
Pirmajā posmā notiek slāpekļa bioloģiskā fiksācija ar baktērijām Rhizobium, pārvēršot to amonjakā.
Fiksācija notiek arī ar fiziskām parādībām, piemēram, zibeni, radot nelielu daudzumu amonjaka.
Amonizējot, dzīvnieku metabolisma atkritumi, piemēram, urīnviela, augsnes baktērijas tiek pārveidoti par amonjaku.
Nitrifikācija pārveido amonjaku nitrātā, veicot divas darbības:
Pirmkārt, notiek nitrozēšana, kur baktērijas nitromonas oksidēt amonjaku par nitrītu.
Tad nitrēšana, baktēriju iedarbībā Nitrobaktērija, nitrīts tiek pārveidots par nitrātu arī oksidējoties.
Pēc tam lielākā daļa augu asimilē nitrātu.
Tāpēc nozares ir pielāgojušas nitrātu izmantošanu tādiem lietojumiem kā mēslošana.
Nitrātu pārpalikumu pārveido pseidonomas slāpekļa gāzē un denitrifikācijas posmā atgriežas atmosfērā.
3. (Enem / 2017) Bieži sastopams fakts, gatavojot rīsus, ir vārāmā ūdens daļas liešana uz uguns zilās liesmas, mainot to uz dzeltenu liesmu. Šīs krāsas izmaiņas var izraisīt dažādas interpretācijas, kas saistītas ar vārāmajā ūdenī esošajām vielām. Papildus galda sālim (NaCl) tas satur ogļhidrātus, olbaltumvielas un minerālsāļus.
Zinātniski ir zināms, ka šīs liesmas krāsas izmaiņas notiek
a) vārīšanas gāzes reakcija ar sāli, gaistoša hlora gāze.
b) fotonu emisija no nātrija, ko ierosina liesma.
c) dzeltenā atvasinājuma ražošana, reaģējot ar ogļhidrātiem.
d) vārīšanas gāzes reakcija ar ūdeni, veidojot ūdeņraža gāzi.
e) olbaltumvielu molekulu ierosināšana, veidojoties dzeltenai gaismai.
Pareiza alternatīva: b) nātrija fotonu emisija, ko ierosina liesma.
Kad sāls ir saskarē ar ūdeni, jonu disociācija notiek šādi:
Un nātrija un hlora jonus izšķīdina ūdens molekulas.
Kad daļa vārāmā ūdens izlijusi, nātrija joni nonāk saskarē ar liesmā saražoto enerģiju, un to, kas notiks tālāk, izskaidro Rutherford-Bohr atomu modelis:
Saņemot enerģiju, elektroni tiek ierosināti uz ārējo slāni, ti, enerģiskāku. Atgriežoties mazāk enerģētiskā stāvoklī, notiek enerģijas izdalīšanās labi definētas krāsas vai elektromagnētiskā starojuma veidā - fotoni.
Šī kustība ir pazīstama kā kvantu lēciens, tas ir, notiek atomu elektroniskā pāreja.
Lai iegūtu vairāk jautājumu par ķīmiju Enem, mēs esam sagatavojuši šo sarakstu: Ķīmijas jautājumi Enem.
Viktorīna Enem: Dabas zinātne
Lasiet arī par:
- Enem jautājumi
- Simulētais Enem (jautājumus komentē eksperti)
- Cilvēkzinātnes un tās tehnoloģijas
- Valodas, kodi un to tehnoloģijas
- Priekšmeti, kas visvairāk krīt Enem

