Pārvērtības, kas notiek materiālos, tiek klasificētas kā ķīmiskās un fizikālās.
Fiziskās pārvērtības, kaut arī uztveramas pēc materiāla izskata izmaiņām, notiek īsākā laikā, cieši nemainot vielas dabu.
Savukārt ķīmiskās transformācijas ir tik intensīvas, ka maina materiāla sastāvu, izraisot transformāciju, kas rada ķīmiski atšķirīgu vielu no tās, kas tai bija sākumā.
Fizikālā transformācija atšķiras no ķīmiskās transformācijas, jo: jaunā ķīmiskā transformācijā Vielas tiek veidotas, savukārt fiziskā pārveidošana maina materiāla formu, bet tā sastāvs ir vienāds.
Fiziskās pārvērtības
Kad mēs mainām materiāla izmēru vai formu, tas mainās, bet to nevar mainīt citā.
Skatoties mikroskopiski, mēs redzam, ka atomi, joni vai molekulas iziet uzbudinājumu vai pārkārtojumu, taču tie netiek mainīti.
Mēs to varam redzēt mainās fiziskais stāvoklis.

Ievērojiet, ka:
- Ciets: daļiņas paliek fiksētās pozīcijās, tāpēc tilpums un forma ir precīzi definēti.
- Šķidrums: daļiņas pārvietojas brīvāk un tāpēc šķidrumam ir noteikts tilpums, bet tā forma mainās atkarībā no trauka.
- Gāzveida: daļiņas pārvietojas visos virzienos un lielā ātrumā, aizpildot visu trauku, tāpēc tilpums un forma ir mainīgi.
Visizplatītākais fizisko pārveidojumu piemērs ir ūdens fizikālie stāvokļi.

Kad mēs sildām ūdeni, tas iztvaiko, ja mēs sasaldējam ūdeni, kas tas sacietē, un, ievietojot to istabas temperatūrā, tas atgriežas šķidrā stāvoklī.
Dažādos štatu ūdeņos molekulas tiek pārkārtotas, taču tā sastāvs ir vienāds. Tātad mums ir fiziska transformācija.
ķīmiskās pārvērtības
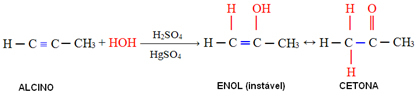
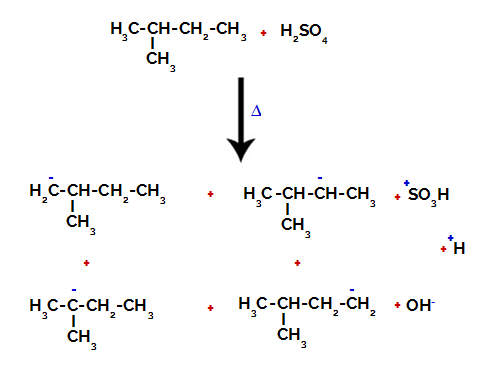
Ja matērija tiek ķīmiski pārveidota, rodas jaunas vielas. Reaģenti reakciju rezultātā tiek pārvērsti produktos.
Reakcijas izraisa ķīmisko saišu pārrāvumu vai veidošanos, bet atomi, kas piedalās reakcijā, ir vienādi, tikai pārkārtoti.
Mēs pamanījām ķīmiskas transformācijas rašanos gaismas parādīšanās, gāzes burbuļu parādīšanās, cieto daļiņu veidošanās, krāsu maiņas un smaržas uztveres dēļ.
Apskatīsim šo piemēru:

Nātrijs ir sārmu metāls, un tas kā šīs ģimenes raksturojums spēcīgi reaģē ar ūdeni.
Reakcija starp nātriju un ūdeni rada metāla hidroksīdu un atbrīvo ūdeņraža gāzi.
Jaukšana vai ķīmiska pārveidošana?
Ja mēs sajaucam divas vielas, transformācija ne vienmēr notiek.
Piemēram, ja mēs sajaucam dzelzi un sēru, mēs iegūstam citu krāsu vielu maisījumu, ja tos novēro atsevišķi.
Izmantojot magnētu, mēs spējām piesaistīt dzelzi un atdalīt to no sēra tā dēļ magnētisms. Tas ir, mēs sajaucam abus, bet tie nav zaudējuši savas sākotnējās īpašības.

Tomēr, ja mēs sajaucam dzelzi un sēru noteiktā proporcijā attiecīgi 7g un 4g un liekam to karsēt, rodas melnas krāsas viela, tas ir dzelzs II sulfīds.
Tādā veidā dzelzi vairs nevar atdalīt, jo tas ir pārveidots par citu vielu.
Mēs nonācām pie secinājuma, ka: maisījums ir fiziska parādība, turpretī reakcija ir ķīmiska parādība.
Fizikālās un ķīmiskās parādības
Pārvērtības, kuras jautājums cieš, kad notiek kādas izmaiņas, sauc arī par fizikālām un ķīmiskām parādībām.
Apskatīsim šos divus piemērus:
ūdens un cukurs
Cukurs ir kovalents savienojums, un, izšķīdinot ūdenī, molekulas izkliedējas, bet nemaina savu identitāti. Tas ir fiziska parādība.

Ūdens un sāls
Ievietojot sāli ūdenī, joni disociējas, kā parādīts ķīmiskajā vienādojumā:
Tā kā tas ir jonu un ūdenī šķīstošs savienojums, nātrija hlorīds tiek pārveidots, sadaloties tā jonos. Tas ir ķīmiskā parādība.

Katjonus un anjonus izšķīdina, ja negatīvajā ūdens polā ir nātrija joni (katijoni) un pozitīvajā ūdens polā ir hlorīda joni (anjoni).
Gan daba, gan cilvēki spēj pārveidot materiālus. Dabiski, ka augļi puvi un dzelzs rūsas. Bet arī mēs provocējam pārvērtības, kad vārām ūdeni vai cepam gaļu. Šie ir materiālu parādību piemēri, kuriem mēs esam liecinieki ikdienas dzīvē.
Skatīt arī: Fizikālās un ķīmiskās parādības
Viktorīna - fizikālās un ķīmiskās pārvērtības
Tagad, kad zināt, kā atšķirt fizikālās un ķīmiskās transformācijas, pārbaudiet savas zināšanas šajā viktorīnā:
Izmantojiet šos vingrinājumus, lai pārbaudītu savas zināšanas.:
- Vingrinājumi par vielas īpašībām
- Vingrinājumi maisījumu atdalīšanai
- Vingrinājumi ar viendabīgiem un neviendabīgiem maisījumiem