Sp tipa oglekļa hibridizācija2 tas notiek, ja tam ir dubultā saite un divas atsevišķas saites vai pi saite (π) un trīs sigmas saites (σ). Patiesībā sp hibridizācija2 tas rodas starp atomiem, kas izveido dubulto saiti.
Šādas molekulas piemērs ir formaldehīds (CH2O). Ievērojiet tā struktūru zemāk:
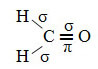
Kā redzams tekstā "sp tipa hibridizācija3”, Oglekļa hibridizācija notiek, kad elektrons no 2. apakšlīmeņa saņem enerģiju un tiek“ transportēts ”uz 2p apakšlīmenis un tādējādi 4 hibridizētas orbitāles rodas no atomu orbitāļu "sajaukuma" tīrs.
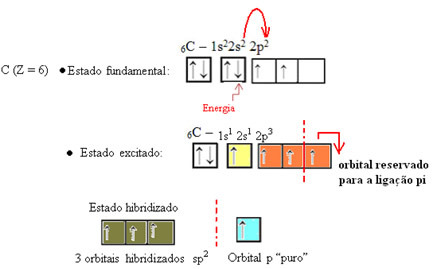
Formaldehīda gadījumā mēs zinām, ka būs pi saite, tāpēc viena no šīm hibridizētajām orbitālēm ir rezervēta šai saitei, bet pārējās trīs satur sigmas saites:
Ūdeņraža atomi, kas veido vienu saiti ar oglekli, veido to ar orbitālu:
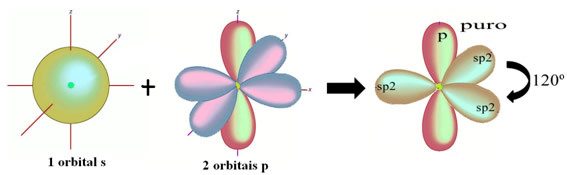
Atlikušajai "tīrajai" orbitālai ir divkārša saite ar skābekļa atomu un formaldehīda molekulai ir šāda struktūra:
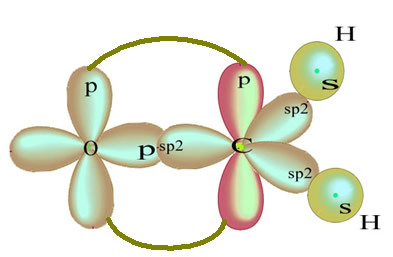
Attiecībā uz obligāciju veidu, kas pastāv šajā formaldehīda struktūrā, mums ir:

Savienojumi: 1 = 2 = σs-sp2
3 = σp-sp2
4 =πp-p
Autore Jennifer Fogaça
Beidzis ķīmiju
Avots: Brazīlijas skola - https://brasilescola.uol.com.br/quimica/hibridizacao-tipo-sp2.htm
