Antuāns Lorāns no Lavoisier viņš dzimis 1743. gada 26. augustā Parīzē.Viņa tēvs bija bagāts advokāts, un viņa māte nomira viņa dzīves sākumā. Tēvs un tante nosūtīja viņu uz Kolegio Mazzarino studēt tiesību zinātnes.Tomēr viņam bija lielāka interese par zinātnes jomu.
22 gadu vecumā viņš jau ir parādījis savu lielo atjautību, izstrādājot Parīzes ielu apgaismojuma projektu, par kuru viņš ieguva Zinātņu akadēmijas zelta medaļu.25 gadu vecumā viņš tika ievēlēts par prestižās Francijas Karaliskās Zinātņu akadēmijas biedru.
Tajā pašā vecumā viņš nopirka Ferme Générale akcijas, asociējoties ar šo privāto iestādi, kas Francijas kronas vārdā no cilvēkiem iekasēja nodokļus. Viņa mērķis bija segt eksperimentu un pētījumu izmaksas.
26 gadu vecumā viņš iepazinās ar Mariju Annu Pjeretu Paulzi (1758-1836), kura bija viena no Ferme Générale galvenajām partnerēm meita. Lavoisier un Marie Anne apprecējās, kad viņai bija tikai 13 gadi, un viņš bija 29 gadus vecs. Bet šī laulība pārvērtās par lielisku savienību starp viņiem, jo Marija Anne palīdzēja Lavoizjē pētījumos, būdama viņa partnere un asistente.
Viņa palīdzēja viņam, samontējot aparātu viņa eksperimentiem, kā arī tulkot zinātniskos un filozofiskos darbus.

Lavoizjē un viņa sieva un asistente Marija Anne
Lavoizjē bija viens no lielākajiem vēstures zinātniekiem, ko daudzi uzskatīja par mūsdienu ķīmijas tēvs. Viņš veica detalizētus novērojumus un, atšķirībā no vairuma, rūpīgi plānoja eksperimentus, izmērot materiālu masu pirms un pēc ķīmiskās pārvērtības.

Ilustrācija Lavoisier laboratorijai, kurā viņš eksperimentēja ar sievas palīdzību (kura sēž pa labi, veic piezīmes)
Starp galvenajiem atklājumiem mēs varam izcelt:
* Skābekļa atklāšana un saistība starp elpošanu un sadegšanas reakciju:1774. gadā Priestlijs bija atklājis jaunu gāzi, kuru Lavoizjē sāka pētīt un eksperimentēt. Ar iegūtajiem datiem viņš parādīja, ka sadegšanai ir nepieciešama jauna gāze, tas ir, bez tās klātbūtnes nav dedzināšanas.
Lavoizjē sauca šo gāzi skābeklis, vārds, kas nāk no grieķu valodas vērsis, kas nozīmē "skābe", un ģen, “Ģenerators vai ražotājs”. Viņš to nosauca, jo eksperimentu rezultātā viņš secināja, ka šī jaunā gāze ir klāt visas skābes, kas vēlāk izrādījās nepareizs secinājums, bet tomēr nosaukums palika.
Lai uzzinātu, cik patiess ir šis Lavoisier atklājums, iededziet sveci un pēc tam pārklājiet to ar stikla flakonu. Ar laiku jūs redzēsiet, ka svece nodziest, jo viss skābeklis pudeles iekšpusē tiks patērēts, sveci dedzinot, un beigsies.
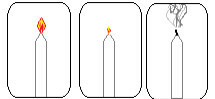
Sveces eksperiments, lai apstiprinātu Lavoisier atklājumu
* Sastāvs gaiss: Lavoisier parādīja, ka šī pati gāze (skābeklis) bija daļa no atmosfēras gaisa un tā bija gāze, kuru mēs elpojam. Viņš arī parādīja, ka atmosfēras gaiss ir skābekļa maisījums ar citu gāzi, kas nepiedalījās degšanas reakcijā. Šodien mēs zinām, ka šī cita gāze ir slāpeklis.
Šie Lavoisier atklājumi parādīja tā laika ideju revolūciju par ķīmiskām transformācijām un noraidīja teoriju flogistons, kas bija teorija, ka katra uzliesmojoša (dedzinoša) viela satur flogistonu - noslēpumainu šķidrumu, kas zaudēts šajā brīdī. degšanas.
* Masu saglabāšanas likums vai Lavoisier likums: Lavoisier parādīja, ka degšanas reakcijās visu iesaistīto vielu masas nemainījās, tas ir, ka viņš bija nosvērts sākumā, pirms reakcijas, bija tāds pats kā reakcijas beigās, ja vien reakcija tika veikta traukā slēgts. Ar to viņš sasniedza slaveno Masas saglabāšanas likums, kas saka, ka ķīmiskā reakcijā reaģentu masa ir vienāda ar produktu masu.
Šodien šis likums ir vislabāk pazīstams ar šādu paziņojumu:
"Dabā nekas netiek radīts, nekas netiek zaudēts, viss tiek pārveidots."
* Ūdens sastāvs: Lavoisier 1783. gadā parādīja, ka ūdens ir divu ūdeņraža daļu un vienas skābekļa (H2O);
* Dzīvnieku vielmaiņa: Antoine Lavoisier parādīja, ka dzīvnieku vielmaiņa bija iekšēja sadegšana, kurā ogleklis un ūdeņradis, kas iegūts no pārtikas, reaģēja ar skābekli un radīja oglekļa dioksīdu un Ūdens.
* Mūsdienu elementu nomenklatūra: 1789. gadā Lavoisier izdeva darbu ar nosaukumu Ķīmijas pamatlīgums, kurā viņš nodrošināja modernu nomenklatūru 33 elementiem, kas saskaņā ar šodienas pareizo koncepciju faktiski ir vielas. Tas bija svarīgi, jo alķīmija mēdza izmantot neskaidru valodu, lai atsauktos uz elementiem.
Diemžēl Lavoisieram beidzās traģiski. Tajā pašā 1789. gadā notika Francijas revolūcija, kas sagrāva pastāvošo politisko kārtību. Cilvēki sacēlās pret vainaga pārmērībām, un Ferme Générale locekļi tika uzskatīti par ienaidniekiem, tostarp Lavoisier.
Viņš tika arestēts 1793. gada novembrī un 1794. gada 8. maijā tika giljotinēts Parīzes Revolucijas laukuma vidū, tagad Konkordes laukumā.

Ēģiptes obelisks revolucionārajā giljotīnas vietā Konkordes laukuma centrā 2014. gada 9. jūnijā Parīzē, Francijā *
* Attēls ar redakcijas kredītu: Veniamin Kraskov / Shutterstock.com
Autore Jennifer Fogaça
Beidzis ķīmiju



