Dažreiz tas var notikt minimālā formula jābūt tādam pašam kā savienojuma molekulārajai formulai; tomēr tas ne vienmēr ir taisnība.
Piemēram, empīriskā vai minimālā ūdens formula ir H2O, norādot, ka starp elementiem, kas veido ūdens molekulas, ir 2: 1 attiecība. Un nejauši tā ir arī ūdens molekulārā formula. Tomēr, lai redzētu, ka tas ne vienmēr notiek, apskatiet šādus divus piemērus:
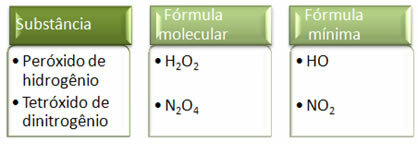
Tā kā minimālā formula ir tikai katra elementa atomu attiecība, nevis faktiskais to daudzums molekulārajā formulā, tas var notikt dažādu savienojumu ar tādu pašu empīrisko formulu un pat savienojuma minimālā formula var būt tāda pati kā molekulas formula cits. Ņemiet vērā, kā tas var notikt šajā piemērā:
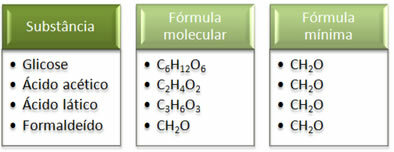
Skatiet, ka minimālā formula CH2Tas pats attiecas uz visām vielām, tas ir, šī minimālā formula izsaka, ka visos gadījumos oglekļa, ūdeņraža un skābekļa atomi molekulārajās formulās ir proporcijā 1:2:1. Turklāt vienīgais, kam ir tāda pati molekulārā formula kā empīriskajai formulai, ir formaldehīds.
- Minimālās vai empīriskās formulas aprēķins:
Lai noteiktu savienojuma empīrisko formulu, vispirms ir jāzina, kāda ir tā procentuālā vai tuvākā formula. To var izdarīt, izmērot katra elementa masu 100 g parauga. Teksts "Procentuālā vai Centesimālā formula”Precizē šo jautājumu labāk.
Nepārtrauciet tūlīt... Pēc reklāmas ir vairāk;)
Piemēram, pieņemsim, ka noteiktā savienojuma aptuveno sastāvu norāda: 40,00% C, 6,67% H un 53,33% O. Šīs vērtības mēs izsniedzam gramos, ņemot vērā 100 g komposta parauga masu. Tādējādi mums ir: 40 g C, 6,67 g H un 53,33 g O.
Tagad ir nepieciešams nodot šīs vērtības vielas daudzumam (mol). Mēs to darām, dalot katru no atrastajām vērtībām ar to attiecīgajām molārajām masām:
C: 40/12 = 3,33
H: 6,67 / 1 = 6,67
O: 53,33 / 16 = 3,33
Tā kā vērtības nav veseli skaitļi, mēs izmantojam šādu ierīci: mēs visas vērtības dalām ar mazāko no tām, lai proporcija starp tām netiktu mainīta.
Šajā gadījumā mazākā vērtība ir 3,33, tāpēc rezultāts būs:
C: 3,33 / 3,33 = 1
H: 6,67 / 3,33 = 2
O: 3,33 / 3,33 = 1
Tādējādi šīs nezināmās vielas minimālā formula ir vienāda ar: Ç1H2O1 vai CH2O.
Īsāk sakot, nepieciešamās darbības, lai atrastu vielas empīrisko vai minimālo formulu, ir šādas:

Autore Jennifer Fogaça
Beidzis ķīmiju
Vai vēlaties atsaukties uz šo tekstu skolas vai akadēmiskajā darbā? Skaties:
FOGAÇA, Jennifer Rocha Vargas. "Minimālā vai empīriskā formula"; Brazīlijas skola. Pieejams: https://brasilescola.uol.com.br/quimica/formula-minima-ou-empirica.htm. Piekļuve 2021. gada 28. jūnijam.