O Le Chatelier princips stāsta mums, ka tad, kad līdzsvara sistēmai tiek radīti traucējumi, tā mainīsies virzienā, kas samazina šo traucējumu radītos spēkus un atjauno jaunu ķīmisko līdzsvaru.
Viens no šiem traucējumiem ir temperatūras svārstības. Šī variācija ir svarīga, jo papildus līdzsvara nobīdes izraisīšanai tā mainīs arī līdzsvara konstantes vērtību Kç.
Lai jūs labāk saprastu, kā tas notiek, apskatīsim piemēru:
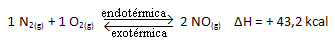
Kç = _[ PIE]2___
[N2]. [O2]
Iepriekš minētā reakcija notiek tiešā virzienā ar enerģijas absorbciju, tā ir endotermiska. Savukārt apgrieztais process notiek ar enerģijas atbrīvošanu, kas ir eksotermiska reakcija.
Tādējādi, ja mēs paaugstinām sistēmas temperatūru, ķīmiskais līdzsvars mainīsies uz endotermisko reakciju, kas šajā reakcijā ir pa labi. Tas ir tāpēc, ka siltums tiek absorbēts un tiek atjaunots līdzsvars.
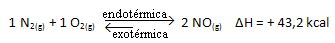
Ir arī pretējs; ja mēs pazeminām šīs sistēmas temperatūru, reakcija mainīsies virzienā, kurā tā atbrīvos siltumu, jo reakcijas kopējā enerģija samazināsies. Tas nozīmē, ka līdzsvars mainīsies uz eksotermisko reakciju, kas šajā gadījumā ir pa kreisi:
Nepārtrauciet tūlīt... Pēc reklāmas ir vairāk;)
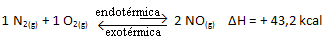
Īsumā:

Saistībā ar līdzsvara konstanti (Kç), kad temperatūra paaugstinās, tā veicina endotermisko reakciju un vairāk NOg) veidojas, palielinot tā koncentrāciju un samazinot reaģentu koncentrāciju. Zemāk esošajā formulā ņemiet vērā, ka NO koncentrācijag) ir tieši proporcionāls konstante Kçtāpēc tas arī palielinās:
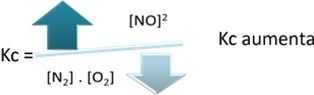
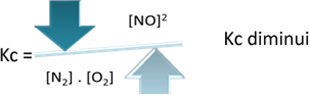
Bet, ja mēs pazemināsim temperatūru, novirzot reakciju uz eksotermisko reakciju, NO produkta koncentrācija samazināsies un reaģentu koncentrācija palielināsies. Tā kā reaģentu koncentrācijas ir apgriezti proporcionālas konstante Kc, tad tās samazināsies:
Autore Jennifer Fogaça
Beidzis ķīmiju
Vai vēlaties atsaukties uz šo tekstu skolas vai akadēmiskajā darbā? Skaties:
FOGAÇA, Jennifer Rocha Vargas. "Temperatūras svārstības un ķīmiskā līdzsvara nobīde"; Brazīlijas skola. Pieejams: https://brasilescola.uol.com.br/quimica/variacao-temperatura-deslocamento-equilibrio-quimico.htm. Piekļuve 2021. gada 28. jūnijam.
Ķīmija

Pārbaudiet savas zināšanas un uzziniet vairāk, izmantojot šo ķīmisko līdzsvara problēmu risinājumu sarakstu. Izmantojot šo materiālu, jūs varēsiet labāk saprast, kā darboties līdzsvara konstantēm (Kp, Kc un Ki), līdzsvara nobīdei, pH un pOH, kā arī līdzsvaram tā sauktajos buferšķīdumos.


