Mūs ieskauj aprīkojums, kam darbībai nepieciešamas šūnas vai baterijas. Tomēr daudzas no šīm pārnēsājamajām ierīcēm kļūst mazākas, un līdz ar to rodas ļoti vajadzīgas miniatūras baterijas.
Šāda veida akumulatoru piemērs ir dzīvsudrabs vai arī to sauc dzīvsudraba-cinka kaudze.
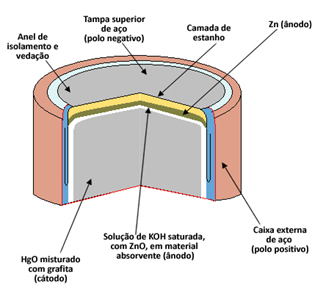
Katra šūna sastāv no diviem elektrodiem, anoda (negatīvais pols) un katoda (pozitīvais pols) un elektrolīta. Dzīvsudraba elementa gadījumā anodu veido kapsula ar metāla cinks (Zns)) tas ir katods par dzīvsudraba oksīds II (HgOs)). Gan Zn, gan HgO tiek sasmalcināti pulverī un saspiesti, lai kaudze būtu pēc iespējas mazāka. O elektrolīts ir izgatavots no šķīduma piesātināts kālija hidroksīds (KOH(šeit)).
Zn oksidējas, ziedojot savus elektronus HgO, kā parādīts zemāk šīs šūnas pusreakcijās un globālajā reakcijā:
Anoda pusreakcija: Zns) + 2 OH1-(šeit) → ZnOs) + 2 H2O(1) + 2e-
Katoda pusreakcija: HgOs) + H2O(1) + 2e- → Hg(1) + 2 OH1-(Theq)
Globālā reakcija: HgOs) + Zns) → ZnOs) + Hg(1)
Dzīvsudraba šūnas tiek izmantotas digitālajos pulksteņos, rokas pulksteņos, kamerās, kalkulatoros, elektroniskajos organizatoros, dzirdes aparāti un citas pārnēsājamas elektriskās ierīces, kurām nepieciešams efektīvs darbs un izturība, jo šīm baterijām ir spriegums no 1,35V.

Diemžēl nepareiza šo bateriju iznīcināšana var nopietni apdraudēt vidi, jo tās satur dzīvsudrabu, kas ir smagais metāls. Dzīvsudrabs var piesārņot augsni, gruntsūdeņus, ezeru un upju ūdeni un sasniegt dzīvniekus un cilvēkus. Tas ir toksisks pat nelielos daudzumos. Starp veselības problēmām, kuras var izraisīt dzīvsudrabs, ir: gļotādu, ādas, nieru bojājumi, vardarbīga slikta dūša, vemšana, sāpes vēderā, asiņaina caureja, un tas var izraisīt nāvi.
Lai uzzinātu vairāk par to, kāpēc baterijas ir toksiski atkritumi, kā dzīvsudrabs ir piesārņots un kas mums jādara ar izlietotajām baterijām, izlasiet tālāk minētos tekstus.
Autore Jennifer Fogaça
Beidzis ķīmiju
Avots: Brazīlijas skola - https://brasilescola.uol.com.br/quimica/pilhas-mercurio.htm
