Rūgštys ir bazės yra dvi cheminės funkcijos, kurios laikomos priešingomis., taip yra todėl, kad jų savybės paprastai yra atvirkštinės. Pavyzdžiui, jei atsižvelgsime į kasdieniame gyvenime esančius maisto produktus, kurie yra rūgštūs, pamatysime, kad jų skonis apskritai yra rūgštus, kaip būna su citrina. Tačiau pagrindiniai maisto produktai turi sutraukiantį skonį (kuris „suriša“ burną), pavyzdžiui, žalias bananas.
Tačiau nustatant medžiagą kaip rūgštinę ar bazinę vien pagal skonį, taip pat kaip metodą, kuris turi daug galimybių žlugti, jis taip pat yra labai pavojingas, nes yra daug stiprių, toksiškų ir netgi žudančių rūgščių ir bazių, pavyzdžiui, rūgštis. sieros (H2TIK4), naudojamą automobilių akumuliatoriuose, ir natrio hidroksidą (NaOH), komerciškai vadinamą kaustine soda.
Taigi organoleptinės savybės (savybės, susijusios su mūsų pojūčiais, pvz., Skonis ir kvapas) nėra tos, kurios naudojamos rūgštims ir bazėms nustatyti. Toliau atkreipkite dėmesį į kitas šių organinių funkcijų savybes, kurios padeda jas palyginti ir atskirti:
- Tirpumas vandenyje:
Tu rūgštys paprastai būna gerai tirpus vandenyje, tuo tarpu dauguma pagrindai é netirpus. Šarminių metalų bazės yra tirpaus, šarminių žemių metalų bazės yra blogai tirpios, o kitų metalų - netirpsta (išimtis yra amonio hidroksidas, NH4OH, kuris egzistuoja tik vandeniniame tirpale, burbuliuodamas amoniako dujas vandenyje ir todėl jame tirpsta).
Sakydami „netirpi“, turime omenyje, kad šios medžiagos praktiškai netirpsta, nes nė viena medžiaga nėra visiškai netirpi vandenyje.
- Struktūra:
Visi rūgštys yra molekulinės, tai yra, susidaro kovalentiniais ryšiais, kuriuose dalijasi elektronai. Pavyzdys yra druskos dujos, kurios susidaro dalijant elektronų porą tarp vandenilio ir chloro:

jau bazės gali būti joninės arba molekulinės. Turintys šarminių ir šarminių žemės metalų yra joniniai, o kiti - molekuliniai.
Pavyzdžiai:
NaOH: joninė bazė, kurią sudaro Na jonai+ o o-;
NH4OH: molekulinė amoniako bazė vandenyje.
Nesustokite dabar... Po reklamos yra daugiau;)
- Elektrinis laidumas:
Viskas rūgštys elektrą praleidžia tik ištirpusios vandenyje, nes būdami vandeninėje terpėje, jie jonizuojasi, tai yra išskiria jonus.
Pavyzdys:
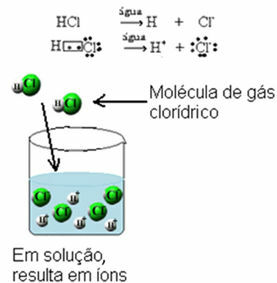
Viskas pagrindai tirpale taip pat praleidžia elektros srovę., nes joniniai disocijuojasi (išskiria jau formulėje esančius jonus), o molekuliniai - jonizuojasi, reaguodami su vandeniu ir išskirdami jonus. At Šarminio metalo pagrindai taip pat praleidžia elektros srovę, kai yra skystos (išlydytos) būsenos.
- Veiksmai dėl rodiklių:
Tu rūgščių ir šarmų rodikliai yra natūralios arba sintetinės medžiagos, kurių spalva pasikeičia, kai jos liečiasi su rūgštimi ar baze. Jei dėl rūgšties indikatorius keičia spalvą, bazė grąžins indikatoriui pradinę spalvą ir atvirkščiai.
Pavyzdžiui, fenolftaleinas yra plačiai naudojamas rūgščių ir šarmų rodiklis, o bazinėje terpėje jis tampa labai intensyvus rausvas; jau rūgščioje terpėje jis tampa bespalvis. Lakmuso popierius taip pat yra geras rodiklis, nes rūgštyje jis tampa raudonas; o ant vieno pagrindo jis tampa mėlynas.
Tai taip pat nurodo pH skirtumą tarp rūgščių ir bazių.
- PH:
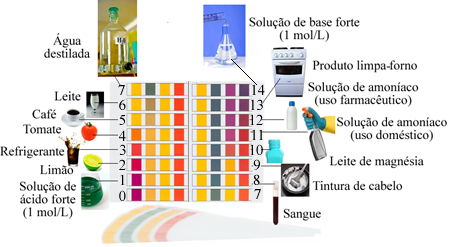
Neutralios laikomos terpės pH yra lygus 7, kaip tai yra distiliuotame vandenyje.
Rūgščių pH yra mažesnis nei 7, Nors bazių pH yra didesnis nei 7.
Tirpalų, kurių pH artimas skalei, pavyzdžiai:
- Abipusis veiksmas:
Susilietusios rūgštys ir bazės reaguoja tarpusavyje, neutralizuoja viena kitą, tai yra, terpės pH daro neutralų. Taip yra todėl, kad H katijonas+ iš rūgšties reaguoja su OH anijonu- nuo pagrindo, formuojant vandenį. Šis reakcijos tipas vadinamas a neutralizavimo reakcija taip pat gamina druską.
Jennifer Fogaça
Baigė chemiją

