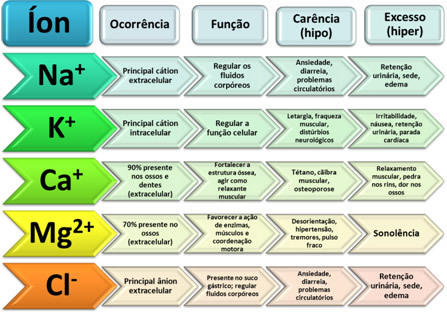
Kad įvyktų cheminė reakcija, būtina įvykdyti keturias pagrindines sąlygas:
1. Reagentai turi susisiekti;
2. Tarp reagentų turi būti cheminis afinitetas;
3. Reagento dalelių susidūrimas turi būti veiksmingas;
4. Turi būti pasiekta aktyvavimo energija.
Trumpai peržiūrėkite kiekvieną atvejį:
1.Reagentų kontaktas:
Ši sąlyga yra akivaizdi, nes net jei reagentai turi didelį afinitetą vienas kitam, kaip rūgščių ir bazių atveju, jei jie yra atskirti, reakcija neįvyks. Jie turi liestis, kad jų dalelės galėtų susidurti, nutraukdamos reagentų ryšius ir formuodamos produktų jungtis.

2.Cheminis afinitetas:
Kaip matėme, reagentų sąlytis yra būtinas, bet nepakankamas. Pavyzdžiui, jei natrio druską liečiame su vandeniu, įvyksta itin smarki reakcija, tačiau įdėję aukso nematysime jokio skirtumo. Taip yra todėl, kad skirtingos medžiagos turi skirtingą cheminį afinitetą viena kitai, arba jos gali neturėti jokio afiniteto. Kuo didesnis cheminis afinitetas, tuo greitesnė reakcija.
Minėtuose pavyzdžiuose natris turi didelę giminingumą vandeniui, todėl, kad metalas natris būtų kaupiamas žibale, kad jis nesiliestų su ore esančia drėgme. Auksas yra inertiškas, todėl aukso paminklai taip ilgai tarnauja, kaip Egipto sarkofagai.

3.Susidūrimo teorija:
Net ir junginiuose, turinčiuose cheminį afinitetą, norint, kad reakcija vyktų, būtina, kad jų dalelės, atomai ar molekulės veiksmingai susidurtų. Ne visos susidūrusios dalelės tai daro efektyviai, tačiau sukrėtimai, dėl kurių suskaidoma reagentų ryšiai ir naujų ryšių susidarymas yra tie, kurie atsiranda teisingoje orientacijoje ir su energija pakanka.
Nesustokite dabar... Po reklamos yra daugiau;)
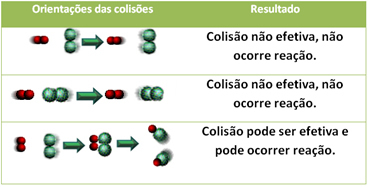
Žemiau parodytas dviejų neveiksmingų susidūrimų ir vieno veiksmingo susidūrimo atvejis, dėl kurio įvyksta reakcija.
4.Aktyvinimo energija ir aktyvuotas kompleksas:
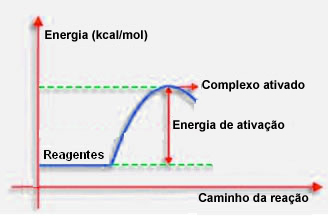
Kaip minėta ankstesniame punkte, veiksmingam susidūrimui, be palankių nurodymų, taip pat reikia pakankamai energijos. Mažiausias energijos kiekis, reikalingas kiekvienai reakcijai įvykti, vadinamas aktyvacijos energija.
Jei reagentų energija yra lygi arba didesnė už aktyvavimo energiją, gerai nukreipto šoko metu susidarys iš pradžių aktyvuotas kompleksas, kuris yra tarpinė struktūra tarp reagentų ir Produktai. Aktyvuotame komplekse susidaro susilpnėję reagentų ryšiai ir naujų produktų ryšiai.
Taigi aktyvacijos energija veikia kaip tam tikras barjeras reakcijai atsirasti, nes kuo ji didesnė, tuo sunkiau bus įvykti reakciją. Kai kuriais atvejais būtina tiekti energiją reagentams. Pavyzdžiui, virimo dujos yra linkusios sąveikauti su ore esančiu deguonimi, tačiau mes turime tiekti energiją, kai sujungiame rungtynes, kitaip reakcija nevyksta. Bet prasidėjus, pati reakcija išskiria pakankamai energijos, kad suaktyvintų kitas molekules ir išlaikytų reakciją.
Jennifer Fogaça
Baigė chemiją
Ar norėtumėte paminėti šį tekstą mokykloje ar akademiniame darbe? Pažvelk:
FOGAÇA, Jennifer Rocha Vargas. „Cheminių reakcijų atsiradimo sąlygos“; Brazilijos mokykla. Yra: https://brasilescola.uol.com.br/quimica/condicoes-para-ocorrencia-reacoes-quimicas.htm. Žiūrėta 2021 m. Birželio 27 d.