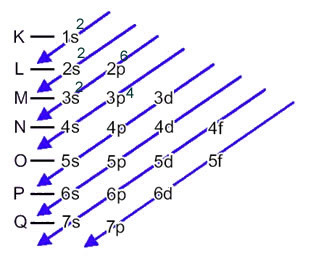
Elektroninis atomo elektronų paskirstymas neutralioje arba pagrindinėje būsenoje paprastai atliekamas su Paulingo diagrama, nurodyta apačioje:
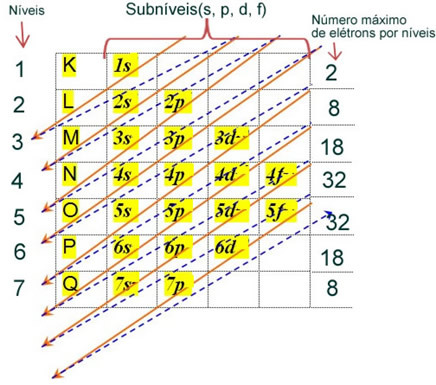
Išsamias šio platinimo taisykles galite rasti šiuose dviejuose mūsų svetainės tekstuose: „Elektroninis elektronų pasiskirstymas"ir"Elektroninio platinimo taisyklės”.
Elektroninis jonų paskirstymas iš pradžių veikia taip pat, kaip ir neutralios būsenos atomų atveju; tik su vienu skirtumu. Kadangi jonas yra atomas, įgijęs ar praradęs elektronus, turime į tai atsižvelgti ir atlikti šiuos veiksmus:

Svarbus pastebėjimas yra: pokytis atliekamas atokiausiame poskyryje ir nėra pats energingiausias.
jei jonas yra a katijonas, mes privalome pašalinkite elektronus kad jis prarado. Pažvelkime į pavyzdį:
Geležies atomas (atominis skaičius = 26) turi tokį elektroninį pasiskirstymą po lygiais energetine tvarka: 1s2 2s2 2p6 3s2 3p6 4s2 3d6. Kalbant apie elektroninius sluoksnius, turime: K =2; L = 8; M = 14; N = 2.
Šis pasiskirstymas parodytas toliau esančioje Paulingo diagramoje:
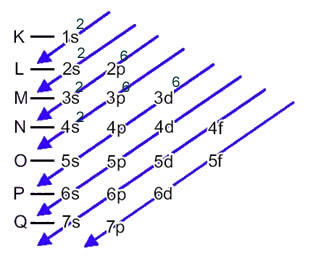
Kai geležies atomas praranda 2 elektronus, jis virsta Fe katijonu.2+. Taigi, vykdydami elektroninį platinimą, mes turime tai padaryti iš paskutinio apvalkalo pašalinkite 2 elektronus(N), o ne pats energingiausias pakopas, kaip parodyta žemiau:
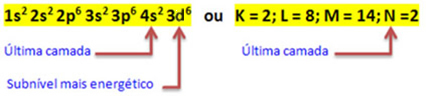
Taigi elektroninis Fe katijono platinimas2+ suteikia:
1s2 2s2 2p6 3s2 3p6 3d6 arba K = 2; L = 8; M = 14
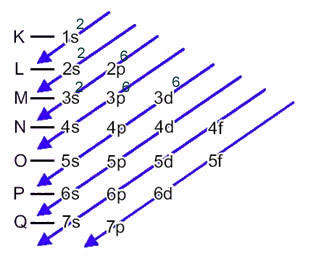
Dabar, jei mes turime atlikti elektroninį platinimą a anijonas, mes privalome pridėti gautus elektronus.Pažiūrėkite, kaip tai daroma, šiame pavyzdyje:
Sieros anijonas (16s2-) susidaro iš sieros atomo (16S) padidinus 2 elektronus, kaip parodyta krūviu 2- Jo pagrindinės būsenos elektroninį platinimą teikia:
1s2 2s2 2p6 3s2 3p4 arba K = 2; L = 8; M = 6
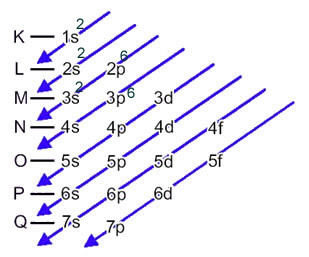
Šiuo atveju paskutinis pakopas yra tas pats, kas energijos lygmuo 3p. Taigi, pridedame du sieros anijono elektronus:
1s2 2s2 2p6 3s2 3p6 arba K = 2; L = 8; M = 8
Jennifer Fogaça
Baigė chemiją
Šaltinis: Brazilijos mokykla - https://brasilescola.uol.com.br/quimica/distribuicao-eletronica-ions.htm
