Vandens elektrolizė susideda iš šios medžiagos skaidymo naudojant elektros srovę ir pridedant elektrolito. Geriau supraskime, kaip tai vyksta?
Skaityk ir tu: Kas yra elektrolizė?
Kaip vyksta vandens elektrolizė?
Vandens molekulės sugeba savaime jonizuotis, generuodamos H jonus+ (arba H3O+) ir oh-:
H2O ↔ H+ + OH-
arba
2 valandos2O ↔ H3O+ + OH-
Tačiau vanduo yra labai silpnas elektrolitas ir, nepaisant šių jonų, jis negali vadovauti elektros srovė. Taigi norint atlikti jo elektrolizę, tai yra, suskaidymą elektros srovės pagalba, būtina pridėti elektrolitą, joninį tirpalą, kuris gali būti druska, bazė arba rūgštis.

Pirmenybinė atrankinio iškrovimo tvarka
Tačiau, kaip paaiškinta tekste Vandeninė elektrolizė, šiuo atveju jonus turėsime ne tik iš vandens, bet ir iš jame ištirpusios medžiagos. Elektrolizės metu prie elektrodo išsiskiria tik vienas katijonas ir vienas anijonas, tai yra atrankinis išmetimas pagal prioritetinę tvarką.
Taigi, norint, kad katodas ir anodas, kurie bus išleidžiami, būtų vandens, o ne ištirpusios medžiagos, reikia pasirinkti
rūgštis, bazė arba druska, kurios jonai yra mažiau lengvai išsiskiriantys iš elektrodų nei vandenyje esantys jonai. Norėdami tai padaryti, turime ieškoti toliau nurodytos prioritetinės eilės: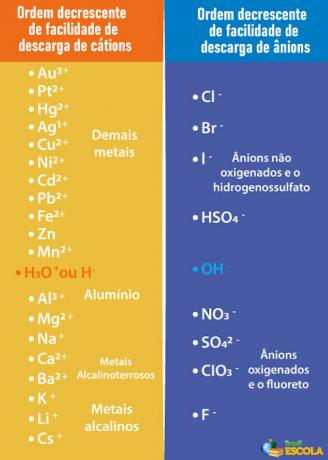
Atkreipkite dėmesį, kad katijonai, išvardyti žemiau H+ turėti mažiau nei lengvai iškrovimo. Dešinėje esančioje lentelėje matome, kad anijonai, esantys žemiau OH- mažiau iškrauti. Todėl galime pasirinkti, pavyzdžiui, drusą, bazę arba rūgštį, kuri sudaro Na jonus.+, K+, PRIE3-, TIK42- ir taip toliau, be to, kad susidaro tie patys jonai kaip ir vanduo, tai yra H+ o o-. Keletas pavyzdžių: sieros rūgšties (H2TIK4), natrio hidroksidas (NaOH) ir kalio nitratas (KNO3).
Pavyzdys su vandens elektrolizės reakcijomis
Tarkime, kad vandens elektrolizė atliekama pridedant sieros rūgšties. Tokiu atveju viduryje susidarysime šie jonai:
Rūgščių disociacija: 1 H2TIK4 → 2 H+ + 1 SO42-
Vandens automatizavimas: H2O → H+ + OH- arba 2 val2O → H3O+ + OH-
Atkreipkite dėmesį, kad vienintelis katijonas yra H.+, taigi jis patirs sumažėjimą (padidėjimas) elektronai) ant neigiamo elektrodo (katodo) ir susidarys vandenilio dujosO (H2).
Dabar, kalbant apie anijonus, viduryje yra du anijonai, kurie yra OS42- o o-. Kaip parodyta aukščiau pateiktoje lentelėje, OS42- jis yra reaktyvesnis ir mažiau lengvai išleidžiamas. Taigi, OH- bus išleidžiamas, oksiduojantis (prarandant elektronus) teigiamajame elektrode (anode) ir gamins dujas deguonies(O2):
Katodo pusinė reakcija: 4 H3O+ + 4 ir- → H2O + H2
Anodo pusinė reakcija: 4 OH- → 2 H2O + 1 O2 + 4 ir-
Susumavus visą šį procesą, gaunama visuotinė lygtis:
Vandens jonizacija: 8 H2O → 4 H3O+ + 4 OH-
Katodo pusinė reakcija: 4 H3O+ + 4 ir- → 4 H2O + 2H2
Anodo pusinė reakcija: 4 OH- → 2 H2O + 1 O2 + 4 ir-
Visuotinė lygtis: 2H2O → 2 H2 + 1 O2
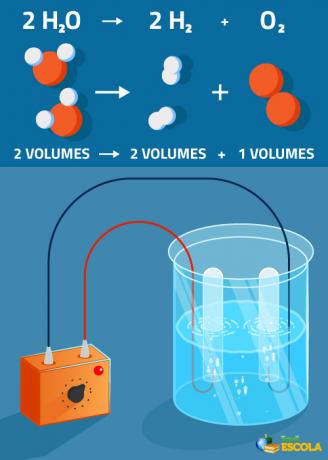
Atkreipkite dėmesį, kad pagaminto vandenilio tūris yra dvigubai didesnis nei deguonies. Tačiau praktiškai šis griežtas santykis nėra patikrintas, nes deguonis yra geriau tirpus nei dujos vandenilis.
Taip pat skaitykite: Aliuminio gavimas elektrolizės būdu
Vandens elektrolizės taikymai
Vandens elektrolizė yra labai svarbus procesas, atsižvelgiant į tai, kad vandenilis yra dujos, kurios gali būti naudojamos kaip kuras. Kaip iš naftos gautas kuras nėra atsinaujinantys, vandenilio dujos gali tapti svarbia alternatyva.
Be to, jau yra benzino gamybos metodų, kuriuose naudojamas vandens elektrolizės procesas. Pažiūrėkite, kaip tai daroma tekste Mokslininkai sugeba anglies dioksidą paversti benzinu.
Jennifer Fogaça
Chemijos mokytoja
Šaltinis: Brazilijos mokykla - https://brasilescola.uol.com.br/quimica/eletrolise-agua.htm