Pajėgumas, kurį jungtys turi pritraukti elektros krūviams, apibrėžiamas kaip poliškumas, kuris įgyja skirtingą pobūdį, priklausomai nuo ryšio, kuriame jis yra.
Dažniausiai organinius junginius jungia anglies atomai arba anglies ir vandenilio atomai: C ─ C ir C ─ H (angliavandeniliai). Tokį ryšį klasifikuojame kaip kovalentinį, jis yra visuose organinių junginių ryšiuose, kuriuos sudaro tik anglis ir vandenilis.
Kai organinio junginio molekulėje be anglies ir vandenilio yra dar vienas cheminis elementas, jo molekulės turės tam tikrą poliškumą. Mes vadiname šį elementą heteroatomu ir galime būti: azotas (N), deguonis (O), be kitų.
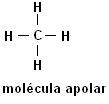
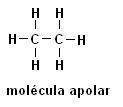
Metanas (CH4) Etanas (C.2H6)
Atkreipkite dėmesį, kad abiejose struktūrose nėra heteroatomų, šiuo atveju molekulės klasifikuojamos kaip nepolinės.


Dėl deguonies, kaip heteroatomo, molekulės demonstruoja poliškumą. Pirmoji molekulė yra junginys Etanolis (CH3CH2Oi), hidroksil-OH buvimas suteikia šiam junginiui polinį pobūdį, net jei jo struktūroje yra nepolinė dalis.
Autorius Líria Alves
Baigė chemiją
Brazilijos mokyklos komanda
Žiūrėti daugiau! plokščias izomeras
Organinė chemija - Chemija - Brazilijos mokykla
Šaltinis: Brazilijos mokykla - https://brasilescola.uol.com.br/quimica/moleculas-organicas-polares-apolares.htm