THE distiliavimas yra homogeninių mišinių atskyrimo būdas, tai yra, kai komponentai yra vienoje fazėje.
Yra du distiliavimo tipai. Paprastasis distiliavimas naudojamas kietojo skysčio atskyrimui ir frakciniam distiliavimui skysčių, kurie maišosi tarpusavyje, mišinyje.
Kad būtų galima išskirti tam tikrą mišinio komponentą, būtina modifikuoti kintamąjį. Distiliavimo atveju atskyrimas vyksta keičiant temperatūrą taip, kad dominantis komponentas pakeistų savo fizinę būseną.
Šiame procese naudojamų medžiagų savybė yra virimo taškas, tai yra, temperatūra, kurioje įvyksta pokytis iš skysčio į dujas.
distiliavimo procesas
Distiliavimo procesas susideda iš šilumos tiekimo į mišinį, kol pasiekiamas dominančio komponento virimo taškas ir jis pereina į dujinę būseną, atsiskirdamas nuo kitų.
Po to dujos praeina per aušinimo kolonėlę, kurioje iš medžiagos bus pašalinta šiluma, kol ji pasieks lydymosi tašką ir taip grįš į skystą būseną. Ši medžiaga nukreipiama į kitą talpyklą.
paprastas distiliavimas
Norėdami atskirti homogeninį mišinį nuo
skystyje ištirpusi kieta medžiaga naudojamas paprastas distiliavimas.Žemiau esančiame paveikslėlyje matome pagrindinę atskyrimo proceso įrangą.

Ar jie:
- Distiliavimo kolba (1), kurioje yra mišinys;
- Šildomoji antklodė (2), kuri suteikia mišiniui šilumos;
- Termometras (3), skirtas stebėti temperatūros pokytį;
- Kondensatorius (4), skirtas išgaravusiam komponentui atvėsinti ir
- Stiklinė (5), skirta atskirtam komponentui surinkti skystoje būsenoje.
Šis procesas gali būti naudojamas, pavyzdžiui, atskirti natrio chloridą (NaCl), žinomą kaip valgomoji druska, ir vandenį. Druskos virimo temperatūra yra 1465 °C ir ištirpsta vandenyje, kad susidarytų vienalytis mišinys.
Kadangi vandens virimo temperatūra yra 100 ºC, jis lengvai pereina į dujinę būseną ir atsiskiria nuo mišinio, o druska kristalizuojasi ir talpoje išlieka kieta.
Vandens garai išeina iš distiliavimo kolbos viršaus ir praeina per kondensatorių. Ant šios įrangos sienelių cirkuliuoja šaltas arba šaltas vanduo. Dėl šilumos mainų tarp skysčių atskirtas mišinio komponentas praranda šilumą ir grįžta į skystą būseną, kad būtų surenkamas į kitą talpyklą. Šis skystis vadinamas distiliatu.
frakcinis distiliavimas
Norėdami atskirti homogeninį mišinį nuo skysčiai maišosi vienas su kitu o esant dideliam virimo temperatūrų skirtumui, naudojamas frakcinis distiliavimas.
Šis metodas yra frakcionuojamas, nes komponentai atskiriami nuo mišinio virimo taško didėjimo tvarka, tai yra, pradedant nuo žemiausios iki tos, kuriai fazei pakeisti reikia aukščiausios temperatūros.
Žemiau esančiame paveikslėlyje pateikta metodui atlikti naudojama įranga.
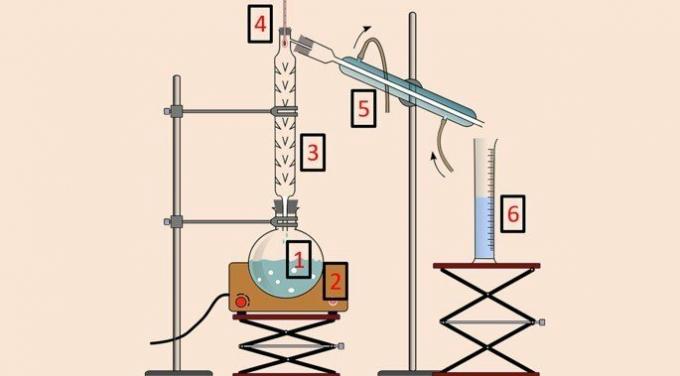
Kaip ir paprasto distiliavimo atveju, naudojama distiliavimo kolba (1), kaitinimo antklodė (2), termometras (4), kondensatorius (5) ir stiklinė (6). Tačiau, distiliavimo arba frakcionavimo kolonėlė (3) yra įranga, leidžianti atskirti pagal temperatūrą.
Distiliavimo kolonėlės viduje yra daugybė kliūčių, neleidžiančių visiems mišinio komponentams išgaruoti vienu metu.
Šis procesas plačiai naudojamas atskirti naftos frakcijas, kurios yra angliavandenilių mišinys. Kai kurie naftos komponentai ir atitinkamos jų virimo temperatūros (PE) yra: butanas (PE 20 ºC), benzinas (PE 150 ºC) ir žibalas (PE 300 ºC).
Frakcinio distiliavimo metu butanas yra pirmasis atskiriamas komponentas, nes jo virimo temperatūra yra žemiausia, tada benzinas, kurio virimo temperatūra yra vidutinė, ir galiausiai žibalas.
Distiliavimo programos
Distiliavimas yra plačiai naudojamas pramonės šakose, nes daugelis mišinių atlieka šį procesą. Šiuo metodu gaminami spiritiniai gėrimai, tokie kaip viskis, brendis ir degtinė.
Naftos chemijos pramonė naftos perdirbimui naudoja frakcinį distiliavimą. Distiliavimo bokštai yra didelės konstrukcijos, skirtos atskirti šio iškastinio kuro frakcijas.

Distiliavimo pratimai
Klausimas 1
Distiliavimas yra savybėmis pagrįstas atskyrimo metodas.
chemija
b) Fizika
c) Biologiniai
d) Bendras dalykas
Alternatyva: b) Fizika.
Virimo temperatūra yra specifinė fizinė medžiagos savybė, nes ji būdinga tam tikrai medžiagai. Tai temperatūra, kurioje medžiaga iš skystos būsenos virsta dujine, tai yra, ji išgaruoja.
2 klausimas
Tai mišinių, atskirtų distiliavimo būdu, pavyzdžiai, IŠSKYRUS
a) vanduo + acetonas
b) sūrymu
c) vanduo + aliejus
d) jūros vanduo
Teisinga alternatyva: c) vanduo + aliejus.
Vanduo ir aliejus yra nesimaišančios medžiagos. Šiuo atveju mišinio komponentams atskirti naudojamas dekantavimo metodas. Šis metodas pagrįstas tankio skirtumu.
Sūrymas (vanduo + druska) ir jūros vanduo, kuriame taip pat yra ištirpusių druskų, atskiriami paprastu distiliavimu. Vandeniui ir acetonui naudojamas frakcinis distiliavimas.
3 klausimas
(UFRGS) Dvifazę nevienalytę sistemą sudaro trys skirtingi skysčiai A, B ir C. Yra žinoma, kad:
A ir B maišosi vienas su kitu;
C nesimaišo su A ir su B;
A yra nepastovi nei B.
Remiantis šia informacija, tinkamiausi trijų skysčių atskyrimo būdai yra šie:
a) centrifugavimas ir dekantavimas.
b) dekantavimas ir dalinis lydymas.
c) filtravimas ir centrifugavimas.
d) filtravimas ir frakcinis distiliavimas.
e) dekantavimas ir frakcinis distiliavimas.
Tinkama alternatyva: e) dekantavimas ir frakcinis distiliavimas.
Heterogeniška klausimo sistema turi dvi fazes:
1 fazė: skysčiai A ir B, kurie maišosi vienas su kitu
2 fazė: skystis C, kuris nesimaišo su kitais komponentais
Todėl dėl tankio skirtumo 1 fazė atskiriama nuo 2 fazės naudojant dekantavimo metodą. Dėl virimo temperatūros skirtumo, kadangi A yra lakesnis nei B, ty lengvai pereina į dujinę būseną, naudojamas frakcinis distiliavimas.
Gaukite daugiau žinių apie turinį:
- Paprastas ir frakcinis distiliavimas
- Mišinių atskyrimas
- Mišinių atskyrimo pratimai