Oksidacija yra pavadinimas, suteiktas elektronų praradimo procesui, kurį sukelia atomas, grupė arba joninės rūšys cheminė reakcija. Jis nustatomas pagal padidėjimą NOX rūšies ar atomo (oksidacijos skaičius) lyginant reagentą ir produktą.
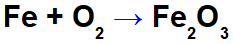
Geležies oksidacijos lygtis.
Pavyzdžiui, aukščiau pateiktoje lygtyje galime nurodyti kiekvieno dalyvio NOX:
Geležies reagentas (Fe): turi NOX 0, nes yra a paprasta medžiaga;
Deguonis reagente (O): turi NOX 0, nes tai paprasta medžiaga;
Deguonis gaminyje: turi NOX-2, nes nėra susietas su šarminiu metalu, šarminių žemių arba vandenilio susidarymas peroksidai arba superoksidai;
Geležis produkte: jame yra NOX +3, nes geležies NOx suma, padauginta iš 2 (atomų skaičius) + deguonies NOx, padauginta iš 3, turi gautis 0, nes tai yra sudėtinė medžiaga:
x.2 + 3.(-2) = 0
2x - 6 = 0
2x = +6
x = + 6
2
x = +3
Lyginant reagento geležies NOx (0) su produktu (+3), pastebėjome padidėjimą, tai yra, jis patyrė oksidacija. Verta paminėti, kad atsiradimas oksidacija jį visada lydi redukcijos reiškinys (tai reiškia elektronų padidėjimą), identifikuojamas NOx sumažėjimu, kaip pavyzdyje pasitaiko su deguonimi.
Taip pat skaitykite:Oksidacijos skaičiaus (NOX) nustatymas
Situacijų, kai vyksta oksidacija, pavyzdžiai:
1. Degimas

Medžiagos degimas taip pat rodo oksidaciją.
Degimas yra kiekviena cheminė reakcija, kuri vyksta dalyvaujant a kuro bet kokios ir oksiduojančios deguonies dujos (O2), todėl gaminasi šiluma ir šviesa. Kiekvienoje degimo metu vyksta reakcija oksidacija.
2. Kai kurios organinės reakcijos
Kiekvienoje organinėje reakcijoje, kuri vyksta dalyvaujant toliau išvardytoms priemonėms, vyksta procesas oksidacija:
Kalio dichromatas (K2Kr2O7) arba kalio permanganatas (KMnO4);
Stiprios rūgšties arba stiprios bazės buvimas;
Ozono dujos (O3) esant metaliniam cinkui (Zn) ir vandeniui (H2O).
3. Baterijos arba baterijos

Baterijos yra įrenginiai, kuriuose visada vyksta oksidacija.
Krūvos arba baterijos yra elektrocheminiai prietaisai, kuriuose kaupiamos cheminės medžiagos. Viena iš šių medžiagų bus oksiduojama, o kita – redukuojama, todėl susidarys elektros srovė.
4. Elektrolizė
Elektrolizė yra cheminis procesas, kurio metu vandeninis tirpalas, kuriame yra druskos, yra veikiamas elektros srovės, kuri skatina šiose medžiagose esančių anijonų oksidaciją. Visoje elektrolizėje yra oksidacija.
Aš. Diogo Lopes Dias
Šaltinis: Brazilijos mokykla - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-oxidacao.htm


