Koligatinės savybės apima fizinės tirpalų savybės, tiksliau, tirpiklio, esant ištirpusiai medžiagai.
Nors ne mums žinoma, koligatyvinės savybės yra plačiai naudojamos pramoniniuose procesuose ir net įvairiose kasdienėse situacijose.
Su šiomis savybėmis susiję fizinės konstantos, pavyzdžiui, tam tikrų medžiagų virimo ar lydymosi temperatūra.
Kaip pavyzdį galime pateikti automobilių pramonės procesą, pvz., Priedų pridėjimą į automobilių radiatorius. Tai paaiškina, kodėl šaltesnėse vietose vanduo radiatoriuje neužšąla.
Procesai, atliekami su maisto produktais, pavyzdžiui, mėsos ar net cukraus prisotinto maisto sūdymas, apsaugo nuo organizmų pablogėjimo ir dauginimosi.
Be to, vandens gėlinimas (druskos pašalinimas), taip pat druskos paskleidimas ant sniego vietomis ten, kur žiema labai atšiauri, patvirtina, kad svarbu žinoti koligatyvinį poveikį sprendimai.
Norite sužinoti daugiau apie sąvokas, susijusias su koligatyvinėmis savybėmis? Perskaitykite straipsnius:
- Fizinės vandens būsenos
- Lydymosi temperatūra ir virimo temperatūra
- Vandens gėlinimas
- Mišinių atskyrimas
Tirpiklis ir tirpumas
Pirmiausia turime atkreipti dėmesį į sąvokas tirpiklis ir ištirpusios medžiagos, abu tirpalo komponentai:
- Tirpiklis: medžiaga, kuri ištirpsta.
- Tirpus: ištirpusi medžiaga.
Kaip pavyzdį galime galvoti apie vandens tirpalą su druska, kur vanduo reiškia tirpiklį, o druska - ištirpusią medžiagą.
Norite sužinoti daugiau? Skaityk ir tu Tirpumas.
Koligatyviniai efektai: kolektyvinių savybių tipai
Koligiatyvus poveikis yra susijęs su reiškiniais, atsirandančiais tirpalams ištirpusios medžiagos ir tirpikliai, priskiriami:
Tonometrinis efektas
Tonoskopija, dar vadinama tonometrija, yra reiškinys, pastebimas, kai didžiausio skysčio garų slėgio sumažėjimas (tirpiklis).
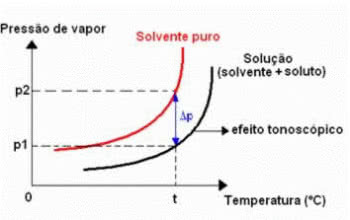
Tonometrinė efektų diagrama
Tai įvyksta ištirpstant nelakiai ištirpusiai medžiagai. Todėl ištirpusios medžiagos sumažina tirpiklio garavimo pajėgumą.
Šio tipo koligatyvinį poveikį galima apskaičiuoti pagal šią išraišką:
ΔP = p0 - P
Kur,
ΔP: absoliutus didžiausio garų slėgio sumažinimas iki tirpalo
P0: didžiausias gryno skysčio garų slėgis, esant t temperatūrai
P: didžiausias tirpalo garų slėgis, esant t temperatūrai
Ebulliometrinis efektas
Ebulioskopija, dar vadinama ebulliometrija, yra reiškinys, prisidedantis prie skysčio temperatūros kitimo padidėjimas verdant.
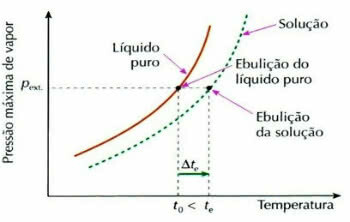
Ebuliometrinis efekto grafikas
Tai įvyksta ištirpus nelakiai ištirpusiai medžiagai, pavyzdžiui, kai į vandenį, kuris verda, įpilame cukraus, skysčio virimo temperatūra padidėja.
Vadinamasis ebulliometrinis (arba ebulioskopinis) poveikis apskaičiuojamas pagal šią išraišką:
tir = tir - t0
Kur,
tir: tirpalo virimo temperatūros pakilimas
tir: pradinė tirpalo virimo temperatūra
t0: gryno skysčio virimo temperatūra
Kriometrinis efektas
Krioskopija, dar vadinama kriometrija, yra procesas, kurio metu šalčio temperatūra sumažėjasprendimo.
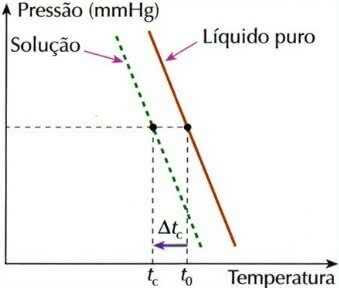
Kriometrinio efekto grafikas
Taip yra todėl, kad skystyje ištirpinus nelakų tirpalą, skysčio užšalimo temperatūra sumažėja.
Krioskopijos pavyzdys yra antifrizo priedai, dedami į automobilių radiatorius tose vietose, kur temperatūra yra labai žema. Šis procesas užkerta kelią vandens užšalimui, padėdamas automobilio variklių tarnavimo laikui.
Be to, druska, pasklidusi gatvėse tose vietose, kur žiema labai šalta, neleidžia ledams kauptis keliuose.
Šiam koligatyviniam poveikiui apskaičiuoti naudojama ši formulė:
tç = t0 - tç
Kur,
tç: sumažina tirpalo užšalimo temperatūrą
t0: gryno tirpiklio užšalimo temperatūra
tç: pradinė tirpiklio užšalimo temperatūra tirpale
Peržiūrėkite eksperimentą su šia nuosavybe: Chemijos eksperimentai
Raulo dėsnis
Vadinamąjį „Raulo įstatymą“ pasiūlė prancūzų chemikas François-Marie Raoult (1830–1901).
Jis tyrė koligatyvinį poveikį (tonometrinį, ebuliometrinį ir kriometrinį), padėdamas tyrinėti cheminių medžiagų molekulines mases.
Nagrinėdamas reiškinius, susijusius su vandens tirpimu ir virimu, jis padarė išvadą, kad: ištirpinant 1 molį bet kurio nepastovaus ir nejoninio tirpalo 1 kg tirpiklio, jūs visada turite tą patį tonometrinį, ebuliometrinį arba kriometrinis.
Taigi Raulo dėsnis gali būti išreikštas taip:
“Nepastoviame ir nejoniniame tirpinio tirpale koligatyvinis poveikis yra proporcingas tirpalo moliškumui.”.
Tai galima išreikšti taip:
Psprendimas = xtirpiklis. Pgrynas tirpiklis
Taip pat skaitykite apie Mol skaičius ir molinė masė.
osmometrija
Osmometrija yra koligatyvinės savybės rūšis, susijusi su tirpalų osmosinis slėgis.
Atminkite, kad osmosas yra fizikocheminis procesas, kurio metu vanduo praeina iš mažiau koncentruotos (hipotoninės) terpės į labiau koncentruotą (hipertoninę) terpę.
Tai vyksta per pusiau laidžią membraną, kuri leidžia tik vandenį.
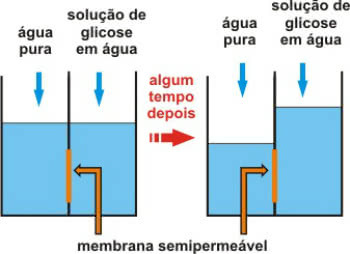
Pusiau pralaidi membranos veikla po kurio laiko
Skambutis osmoso slėgis būtent slėgis leidžia vandeniui judėti. Kitaip tariant, tai yra tirpalo slėgis, kuris neleidžia jo praskiesti, praleidžiant gryną tirpiklį per pusiau laidžią membraną.
Todėl osmometrija yra osmosinio slėgio tirpaluose tyrimas ir matavimas.
Atkreipkite dėmesį, kad vandens gėlinimo (druskos pašalinimo) technikoje vadinamas procesas atvirkštinė osmozė.
Skaitykite daugiau apie Osmosas.
Osmometrijos dėsniai
Olandijos fizikas ir chemikas Jacobus Henricus Van’t Hoffas (1852-1911) buvo atsakingas už dviejų įstatymų, susijusių su osmometrija, postulavimą.
Pirmasis dėsnis gali būti išreikštas taip:
“Esant pastoviai temperatūrai, osmosinis slėgis yra tiesiogiai proporcingas tirpalo moliarumui.”
Antrame jo paskelbtame įstatyme turime tokį teiginį:
“Esant pastoviam moliškumui, osmosinis slėgis yra tiesiogiai proporcingas absoliučiai tirpalo temperatūrai.”
Todėl, norint apskaičiuoti molekulinių ir praskiestų tirpalų osmosinį slėgį, naudojama formulė:
π = MRT
esamas,
π: tirpalo osmosinis slėgis (atm)
M: tirpalo moliarumas (mol / l)
R: visuotinė tobulų dujų konstanta = 0,082 atm. L / mol. K.
T: absoliuti tirpalo temperatūra (K)
Skaityk ir tu Molarizmas.
Stojamojo egzamino pratimai su grįžtamuoju ryšiu
1. Lyginant dvi keptuves, tuo pačiu metu ant dviejų identiškų degiklių toje pačioje viryklėje, pastebima, kad slėgis dujų verdančiame vandenyje uždaroje greitpuodyje yra didesnis nei verdančiame vandenyje greitpuodyje atviras.
Esant tokiai situacijai ir jei jose yra lygiai tas pats visų ingredientų kiekis, mes galime teigti, kad, palyginti su tuo, kas vyksta atviroje keptuvėje, kepimo laikas greitpuodyje uždarytas bus:
a) žemesnė, nes virimo temperatūra bus žemesnė.
b) žemesnė, nes virimo temperatūra bus aukštesnė.
c) mažesnis, nes virimo temperatūra nesikeičia priklausomai nuo slėgio.
d) lygus, nes virimo temperatūra nepriklauso nuo slėgio.
e) didesnis, nes slėgis bus didesnis.
B alternatyva
2. (UFRN) Sunkiomis žiemos vietomis įprasta į automobilių radiatorių vandenį įpilti tam tikrą kiekį etilenglikolio. Tirpalas vietoj vandens yra naudojamas kaip aušinimo skystis, nes tirpalas turi:
a) mažesnė sintezės šiluma.
b) žemesnė užšalimo temperatūra.
c) aukštesnė užšalimo temperatūra.
d) didesnė sintezės šiluma.
B alternatyva
3. („Vunesp“) Vienas iš būdų išgydyti žaizdas, pagal populiarų įsitikinimą, yra uždėti ant jų cukraus ar kavos miltelių. Koligatyvinę savybę, kuri geriausiai paaiškina skysčio pašalinimą aprašyta procedūra, skatinančia gijimą, tiria:
a) osmometrija.
b) krioskopija.
c) endoskopija.
d) tonoskopija.
e) ebulliometrija.
Alternatyva
4. (UFMG) Šaldiklyje yra penki būdai, kuriuose yra skirtingų skysčių, gaminti ledus ir citrinas. Jei formos dedamos į šaldiklį tuo pačiu metu ir iš pradžių yra toje pačioje temperatūroje, pirmiausia bus užšaldyta forma, kurioje yra 500 ml:
a) grynas vanduo.
b) tirpalas vandenyje, kuriame yra 50 ml citrinos sulčių.
c) tirpalas vandenyje, kuriame yra 100 ml citrinos sulčių.
d) tirpalas vandenyje, kuriame yra 50 ml citrinos sulčių ir 50 g cukraus.
e) tirpalas vandenyje, kuriame yra 100 ml citrinos sulčių ir 50 g cukraus.
Alternatyva
5. (Cesgranrio-RJ) Nustatyta medžiagos x lydymosi temperatūra, nustatant žemesnę nei lentelėje pateiktą šios medžiagos vertę. Tai gali reikšti, kad:
a) nustatant sunaudotas medžiagos kiekis buvo mažesnis nei būtina.
b) nustatant panaudotas medžiagos kiekis buvo didesnis nei būtina.
c) dalis medžiagos neištirpo.
d) medžiagoje yra priemaišų.
e) medžiaga yra 100% gryna.
Alternatyvus


