Halogenidas yra organinis junginys, turintis bent vieną halogeno atomą. - tai yra periodinės lentelės 17 arba VII šeimos cheminiai elementai (F, Cl, Br, I arba paprastai: X) prijungtas prie grupės, gaunamos iš angliavandenilio.
RX (kur X = F, Cl, Br arba I)
Kai kurie halogenidai rodomi žemiau:

Jodas yra reaktyviausias iš visų, o fluoras - mažiausiai, nes jungimosi energija tarp halogeno ir anglies didėja iš jodo krypties į fluorą.
Kitas dalykas yra tai, kad reaktyvumas taip pat didėja šia prasme:

Taigi šis reaktyvumas vyksta lengviau tretiniuose anglies halogeniduose dėl anglies, susijusios su organiniu halogenidu, charakterio:

Taigi pakaitinę grupę, pvz., OH, kuri sudarys alkoholį, labiau traukia tretinė anglis, turinti teigiamą charakterį (1+), ir pakaitalas yra lengvesnis.
Halogenidai gali vykti reakcijomis, kurios leidžia mums praktiškai atlikti visas kitas organines funkcijas (alkoholį, eterį, alkiną, cianidą ar nitrilą, aminą ir kt.). Tačiau praktiškai tai neįmanoma, nes halogenidai yra labai brangūs junginiai.
Pavyzdžiui, norint pagaminti alkoholį, halogenidas vandeninėje terpėje reaguoja su stipria baze, pavyzdžiui, natrio hidroksidu. Pažiūrėkime toliau pateiktą pavyzdį, kuriame šarminės etilo chlorido (chloretano) hidrolizės metu susidarys etanolis:
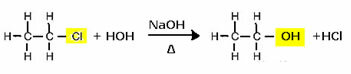
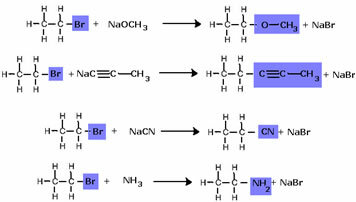
Atkreipkite dėmesį, kad halogenidų grupę pakeitė OH, alkoholio funkcinė grupė. Ta pati schema laikomasi formuojant kitas grupes, atskiriant tik reagentą:
Jennifer Fogaça
Baigė chemiją
Brazilijos mokyklos komanda
Šaltinis: Brazilijos mokykla - https://brasilescola.uol.com.br/quimica/reacoes-substituicao-haletos-organicos.htm
